CANCELA EL REGISTRO SANITARIO A LOS PRODUCTOS FARMACÉUTICOS QUE CONTIENEN EL PRINCIPIO ACTIVO SIBUTRAMINA
Núm. 1.549 exenta.- Santiago, 20 de mayo de 2013.- Visto estos antecedentes: La Res. Ex. Nº 2.993, de fecha 19 de octubre de 2010, del Instituto de Salud Pública de Chile, por medio de la cual se decidió suspender la importación, exportación, fabricación, comercialización y distribución de los productos farmacéuticos que contienen sibutramina en su formulación; el oficio ordinario Nº 578, de fecha 11 de marzo de 2013, del Instituto de Salud Pública de Chile, por medio del cual solicita al Ministerio de Salud su pronunciamiento para la cancelación de registros sanitarios que contienen el principio activo sibutramina; el oficio ordinario B35/Nº 1.254, de fecha 22 de abril de 2013, del Subsecretario de Salud Pública, pronunciándose favorablemente con respecto a la cancelación de los registros sanitarios que contienen como principio activo sibutramina, los que se mencionan en la parte resolutiva; la alerta de seguridad emanada de la Food and Drug Administration (FDA) de los Estados Unidos de Norteamérica, de fecha 10 de agosto de 2010, por medio de la cual se da a conocer la suspensión de la comercialización para productos farmacéuticos que contienen sibutramina, basándose en los resultados del estudio "Sibutramine Cardiovascular Outcomes Trial (SCOUT)", en el cual se demostró un aumento del 16% en el riesgo de eventos cardíacos severos, incluyendo infarto al miocardio no fatal, accidente vascular encefálico no fatal, paro cardíaco y muerte, en los pacientes expuestos a sibutramina, en comparación con placebo, demostrándose además una discreta diferencia en la pérdida de peso entre los grupos que recibieron placebo y sibutramina, evidenciando por lo tanto que los riesgos de su uso son mayores que los beneficios que se pueden lograr; las comunicaciones de otras agencias internacionales de medicamentos, tales como la European Medicines Agency (EMA) y la Therapeutic Goods Administration (TGA) de Australia, las que también prohibieron la comercialización de los productos que contienen sibutramina, decisión que también fue tomada por otros países, como Uruguay, México, Panamá, Colombia y Canadá.
Considerando: Que hasta la fecha no se cuenta con nuevos antecedentes que den cuenta que el uso de este principio activo esté asociado a mayores beneficios con respecto al riesgo; que, si bien la sibutramina está indicada para aquellos pacientes cuyo exceso de peso implica un riesgo para su salud (índice de masa corporal superior a 30 para pacientes obesos sin otras complicaciones y sobre 27 para pacientes que tienen enfermedades asociadas), en los cuales los métodos tradicionales no han surtido efecto para el tratamiento de la obesidad y sobrepeso, existen alternativas terapéuticas más seguras; y
Teniendo presente: Las disposiciones de los artículos 94º y 102º del Código Sanitario; del Reglamento del Sistema Nacional de Control de Productos Farmacéuticos, aprobado por el decreto supremo Nº 3, de 2010, del Ministerio de Salud y los artículos 59º letra b) y 61º letra b) del DFL Nº 1, de 2005, dicto la siguiente:
Resolución:
1.- Cancélanse, a contar de la entrada en vigencia de esta resolución, los registros sanitarios que se mencionan a continuación:
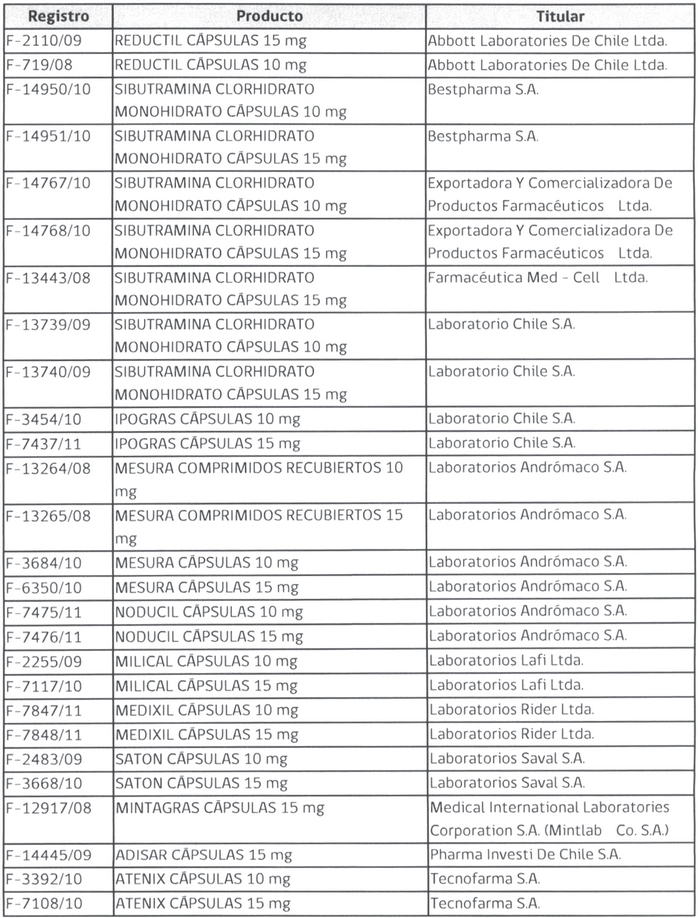 .
. 2.- Prohíbese la importación, distribución o venta en el país del principio activo sibutramina como materia prima y de todos los productos farmacéuticos que lo contengan.
3.- Establécese que en el futuro el Instituto de Salud Pública no concederá registros sanitarios a productos farmacéuticos en cuya formulación esté contenida la sibutramina.
4.- Dispónese que esta resolución entrará en vigencia a partir de su publicación en el Diario Oficial.
Anótese, comuníquese y publíquese en el Diario Oficial y en la página web del Instituto de Salud Pública de Chile.- María Teresa Valenzuela Bravo, Directora.