Artículo 1°.- Modifícase el decreto supremo Nº 977, de 1996, del Ministerio de Salud, que aprueba el Reglamento Sanitario de los Alimentos, en la forma que a continuación se indica:
1.- Reemplázase el artículo 493 por el siguiente:
"Artículo 493.- Las fórmulas para lactantes son aquellos productos que satisfacen los requerimientos nutricionales de los lactantes, cuando la alimentación con leche materna no es posible o es insuficiente.
Se entiende por lactantes a los niños que tengan hasta 12 meses de edad.
La información y rotulación nutricional de estas fórmulas deberán expresarse por cada 100g o 100ml, según corresponda, y por cada 100 kilocalorías (kcal) utilizables del producto, así como por 100 ml del producto listo para el consumo, de acuerdo a las instrucciones indicadas por el fabricante. Además, deberá declararse la cantidad total de cada vitamina, mineral y cuando corresponda los "ingredientes opcionales" referidos en el artículo 495".
2.- Reemplázanse las letras a) y b) del artículo 494 por las siguientes:
"a) fórmula de inicio: es el producto líquido o en polvo para reconstituir, especialmente fabricados para satisfacer por sí solo las necesidades nutricionales de los lactantes durante al menos los primeros seis meses de vida en reemplazo de la leche materna, cuando no sea posible o sea insuficiente la alimentación con ésta. Debe estar fabricada a base de leche de vaca o de otros animales, o de mezclas de la leche de éstos, o de otros ingredientes autorizados por este reglamento.
b) fórmula de continuación: es aquella que forma parte de un esquema de alimentación mixta destinada al consumo de los lactantes de más de seis meses hasta los 12 meses de edad".
3.- Reemplázase el artículo 495 por el siguiente:
"Artículo 495.- El producto debe haber sido elaborado exclusivamente por medios físicos y envasado de manera que se evite su alteración y contaminación en cualquier condición normal de manipulación, almacenamiento, distribución y venta.
Asimismo, deberá estar fabricada a base de leche de vaca o de otros animales o de mezclas de leches de distintos animales o de otros ingredientes sobre los cuales se haya demostrado que son idóneos para la alimentación de los lactantes. Deberá estar científicamente demostrada la inocuidad, así como la idoneidad nutricional, para favorecer el crecimiento y el desarrollo de los lactantes. Estas fórmulas deberán ser libres de gluten.
La fórmula de inicio reconstituida deberá presentar la siguiente composición:
a)
Energía mínimo máximo
60 kcal/100 ml 70 kcal/100 ml
b)
Proteínas mínimo máximo
1,8 g/100 kcal 3,0 g/100 kcal
Cuando las fórmulas a base de proteínas de la leche no hidrolizadas, contengan menos de 2 g de proteínas/100 kcal y, cuando las fórmulas para lactantes a base de proteínas hidrolizadas contengan menos de 2,25 g de proteínas/100 kcal, deberán mantener los antecedentes de las evaluaciones clínicas realizadas, disponibles para cuando la autoridad sanitaria los requiera.
El valor mínimo de proteínas de 1,8 g/100kcal se aplica a las proteínas de la leche de vaca o de otros animales o mezcla de la leche de éstos. En las fórmulas a base de aislados de proteínas de soya, en cambio, se aplica un valor mínimo de 2,25 g/100 kcal.
El cálculo del contenido de proteínas de la fórmula final preparada y lista para el consumo deberá basarse en N x 6,25, salvo que se proporcione una justificación científica para el uso de un factor de conversión diferente aplicable a un determinado producto.
La fórmula debe contener una cantidad disponible de cada aminoácido esencial y semiesencial igual, al menos, a la que contiene la proteína de referencia, según se define en la Tabla Nº 1 del presente artículo. No obstante, a efectos de cálculo, las concentraciones de tirosina y fenilalanina pueden sumarse. Las concentraciones de metionina y cisteína pueden sumarse si la proporción es inferior a 2:1; si la proporción se sitúa entre 2:1 y 3:1, la idoneidad de la fórmula debe demostrarse por medio de ensayos clínicos.
Podrán añadirse al preparado para lactantes aminoácidos aislados únicamente a fin de mejorar su valor nutritivo para los lactantes. Para mejorar la calidad de las proteínas, podrán añadirse aminoácidos esenciales y semiesenciales, pero sólo en las cantidades necesarias a tal efecto. Sólo podrán utilizarse las formas L de los aminoácidos.
Tabla Nº 1: Contenido de aminoácidos de la proteína de referencia de la leche humana*
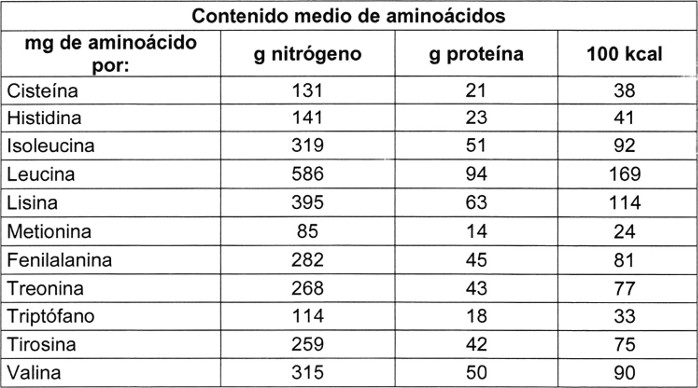 .
. * Adaptado del Codex Stan 72, revisado en 2016.
c)
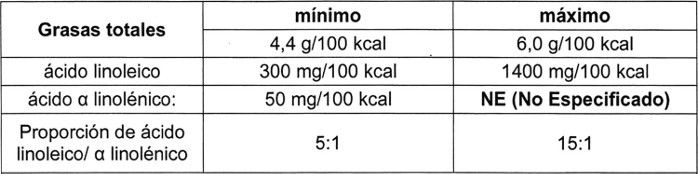 .
. Se prohíbe la utilización de aceite de sésamo y aceite de algodón.
Los ácidos láurico y mirístico en conjunto no deberán superar el 20% del contenido total de ácidos grasos.
Los ácidos grasos trans solamente serán de origen lácteo. El contenido de ácidos grasos trans no deberá ser superior al 3% del contenido total de ácidos grasos.
El contenido de ácido erúcico no deberá superar el 1% del contenido total de ácidos grasos.
El contenido total de fosfolípidos no deberá superar los 300mg/100kcal.
No se podrán utilizar aceites o grasas hidrogenadas comercialmente.
d)
mínimo máximo
Carbohidratos disponibles 9 g/100 kcal 14 g/100 kcal
La lactosa y los polímeros de glucosa deberán ser los carbohidratos preferentes para las fórmulas a base de proteínas de la leche de vaca y de proteínas hidrolizadas. Solo podrán añadirse almidones exentos de gluten precocidos o gelatinizados hasta un máximo de 30% del contenido total de carbohidratos y hasta un máximo de 2 g/100 ml de la fórmula reconstituida.
Deberá evitarse el uso de sacarosa y fructosa: La sacarosa sólo se puede añadir a fórmulas para lactantes con base en proteínas hidrolizadas. Si se añade, el contenido de sacarosa no deberá exceder el 20% del contenido total de hidratos de carbono. Este agregado deberá señalarse en forma destacada en la cara principal del envase.
e)
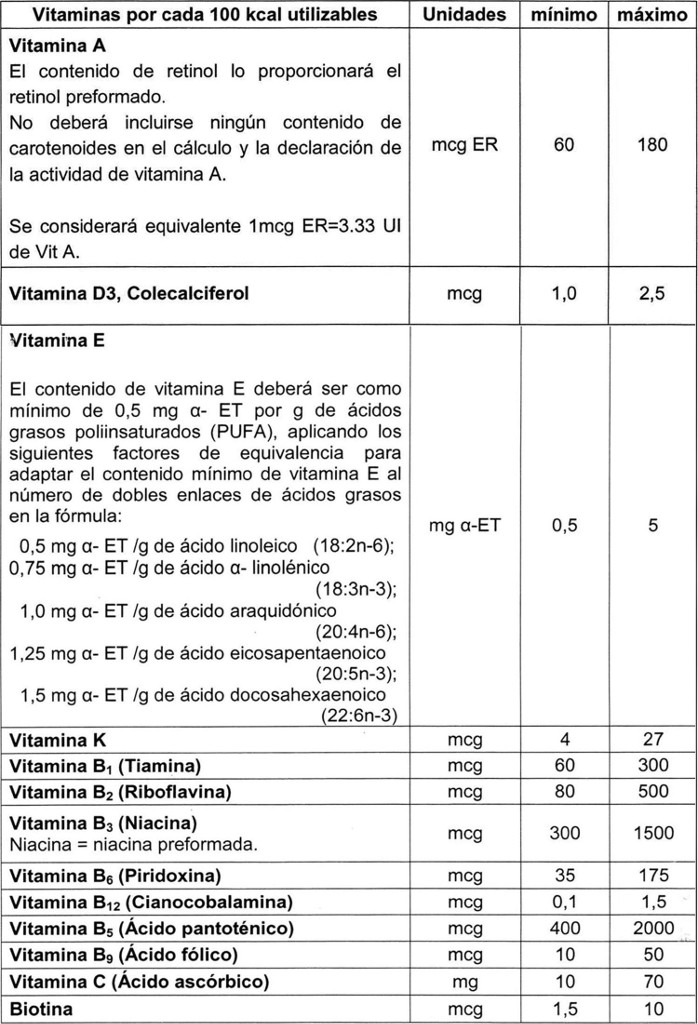 .
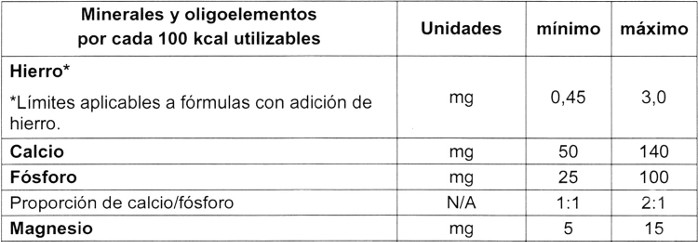
. f)
 .
.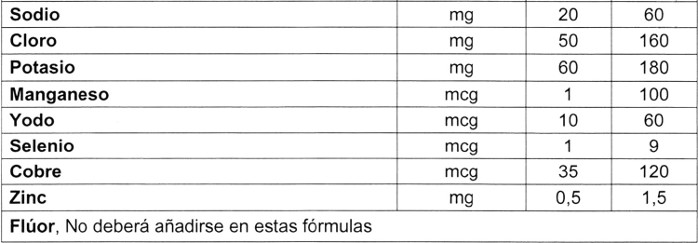 .
. g) Otras sustancias:
Deberán añadirse las sustancias que se indican a continuación, en cuyo caso su contenido por 100 kcal en la fórmula lista para el consumo deberá estar entre los límites siguientes:
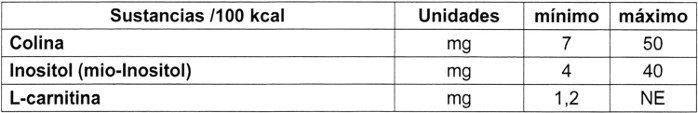 .
. h) Ingredientes opcionales
Se podrán adicionar los siguientes ingredientes opcionales de acuerdo a los límites de la siguiente tabla:
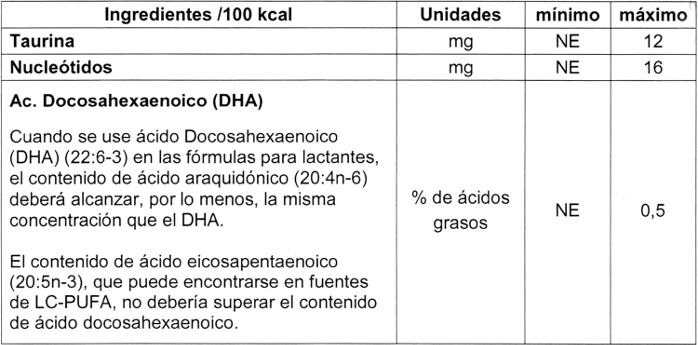 .
. Podrán añadirse otras sustancias que normalmente están presentes en la leche humana, para mejorar la calidad nutricional de las fórmulas. La idoneidad e inocuidad de estas sustancias deberán estar demostradas científicamente. La fórmula deberá contener las cantidades sobre la base de su presencia en la leche humana.
Podrán emplearse únicamente cultivos que produzcan ácido láctico L (+).
i) Aditivos
Sólo se podrán usar los siguientes aditivos en las cantidades señaladas:
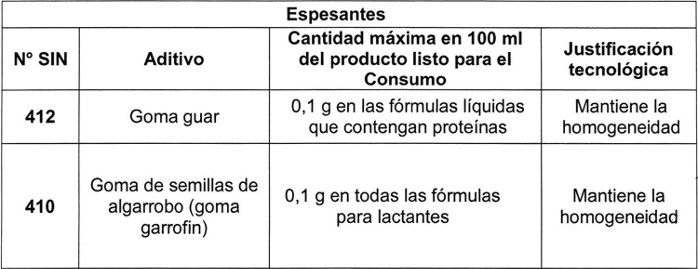 .
.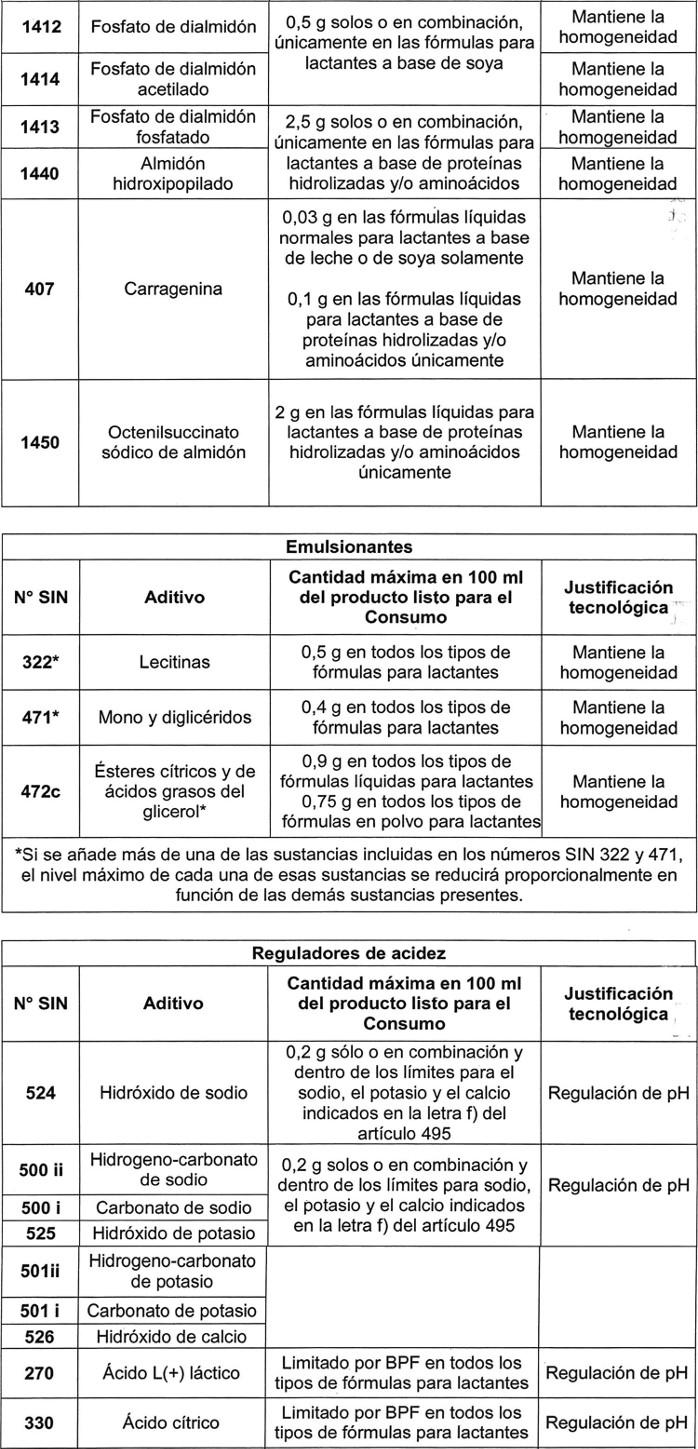 .
.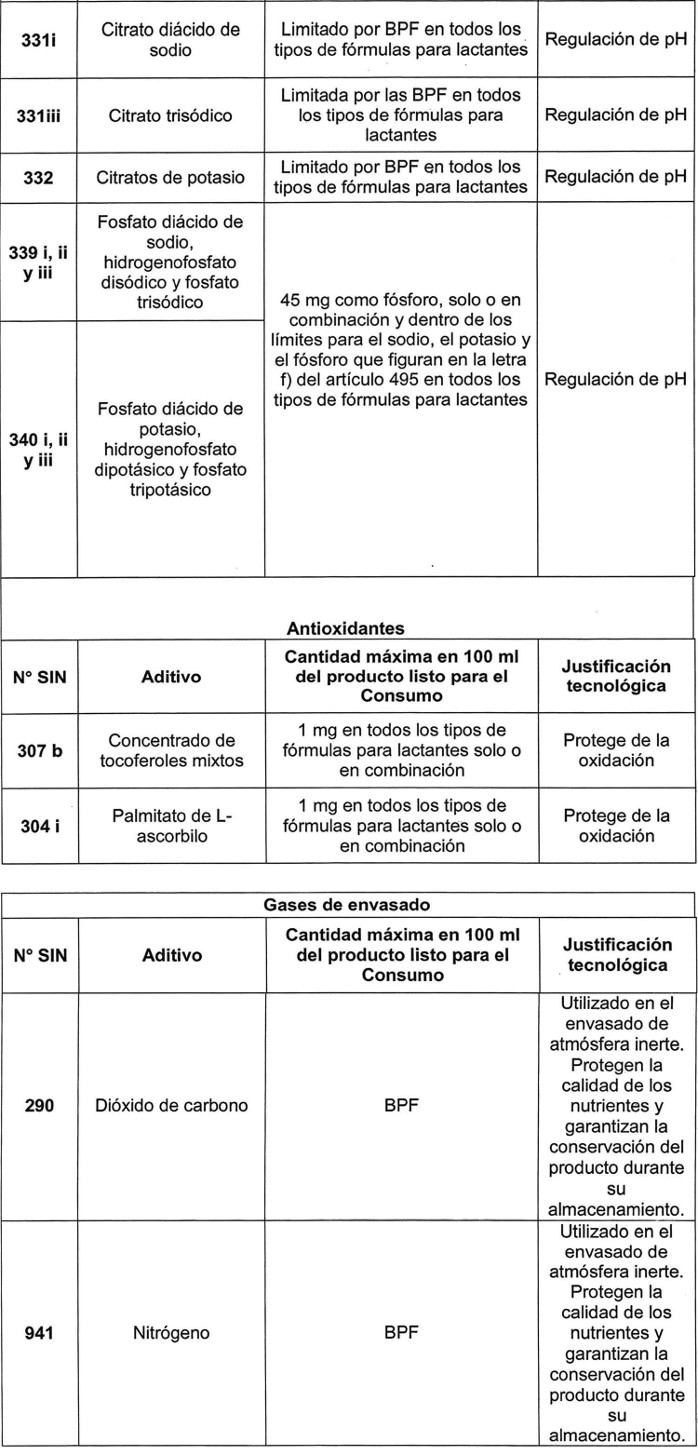 .
. 4.- Reemplázase el artículo 498 por el siguiente:
"Artículo 498.- Preparaciones comerciales de alimentos infantiles son aquellas utilizadas durante el período de destete y adaptación de los niños a la alimentación sólida. Se preparan para ser administrados directamente, o bien, deshidratados para ser reconstituidos".
5.- Reemplázase el artículo 501 por el siguiente:
"Artículo 501.- Estos alimentos infantiles deben contener sustancias inocuas y adecuadas para la alimentación de los lactantes y niños pequeños hasta los 36 meses de edad.
El producto y sus componentes no deberán haber sido tratados con radiaciones ionizantes".
6.- Reemplázase el artículo 502 por el siguiente:
"Artículo 502.- Estos alimentos deberán presentar la siguiente composición:
a) Proteínas
El contenido de proteínas de los colados o picados deberá ser el correspondiente a la declaración de ingredientes en su rotulación, según las siguientes condiciones:
a.1) Al menos 7g/100 kcal, cuando la carne, el pollo, el pescado u otra fuente de proteínas de origen animal, individualmente o en combinación, sean los únicos ingredientes mencionados en la denominación del producto. En estos productos, la carne, el pollo, el pescado u otra fuente de proteínas de origen animal deberán constituir en total, como mínimo tanto el 40% del peso total del producto, como el 25% del peso total de las fuentes de proteínas mencionadas.
a.2) Al menos 4g/100 kcal, cuando la carne, el pollo, el pescado u otra fuente de proteínas de origen animal, individualmente o en combinación, sean nombrados en primer lugar en la denominación del producto. En estos productos, la carne, el pollo, el pescado o la otra fuente de proteínas deberán constituir en total, como mínimo tanto el 10% del peso total del producto, como el 25% del peso total de las fuentes de proteínas mencionadas.
a.3) Al menos 3g/100 kcal, cuando la carne, el pollo, el pescado u otra fuente de proteínas de origen animal, individualmente o en combinación, aparecen declarados, aunque no en primer lugar, en la denominación del producto. En estos productos, la carne, el pollo, el pescado o la otra fuente de proteínas de origen animal deberán constituir en total, como mínimo tanto el 8% del peso total del producto, como el 25% del peso total de las fuentes de proteínas mencionadas.
a.4) Al menos 3g/100 kcal, cuando no menciona la carne, el pollo, el pescado u otra fuente de proteínas de origen animal en la denominación del producto.
En los casos en que los productos contengan menos proteínas que 3g/100 kcal, se considerarán bajos en proteínas, y deberá rotular de manera destacada, en la cara frontal del producto, una frase como se indica en la letra c) del artículo 505 de este reglamento.
b) Materia grasa:
No deben utilizarse grasas y aceites parcialmente hidrogenados.
c) Sodio: máximo 200 mg/100 g.
No se permitirá la adición de sal (NaCl) a los productos de postre a base de frutas.
d) Vitaminas y minerales: podrán agregarse vitaminas y minerales hasta los límites máximos establecidos en el artículo 495 del presente reglamento.
e) Fibra dietética total: deberá ser la propia de los alimentos naturales utilizados como ingredientes del producto, y no deberá adicionarse fibra dietética con ingredientes artificiales.
f) Carbohidratos disponibles: No deberán añadirse mono o disacáridos".
7.- Reemplázase el artículo 503 por el siguiente:
"Artículo 503.- Sólo se permitirá el uso de los siguientes aditivos, en la cantidad que se indica por 100 g o 100 ml del producto listo para el consumo:
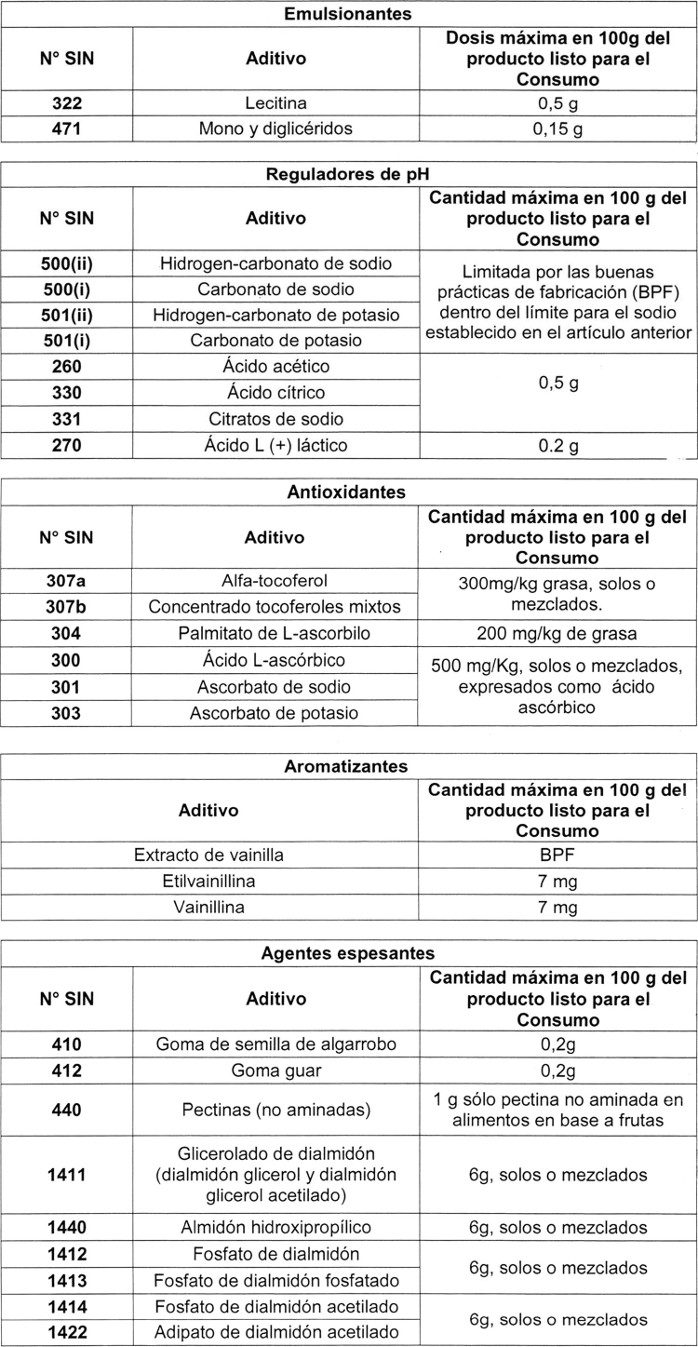 .
. 8.- Reemplázase el artículo 504 por el siguiente:
"Artículo 504.- El producto deberá prepararse con especial cuidado, mediante buenas prácticas de fabricación, a fin de eliminar totalmente los residuos de los plaguicidas que pueden necesitarse para la producción, el almacenamiento o la elaboración de las materias primas o del ingrediente alimentario acabado o, si ello es técnicamente inevitable, reducirlos en la mayor medida posible.
El producto no deberá contener residuos de hormonas ni de antibióticos determinados mediante métodos convenidos de análisis, y estará prácticamente exento de otros contaminantes y otras sustancias dañinas para la salud, especialmente, de sustancias farmacológicamente activas".
9.- Reemplázase el artículo 505 por el siguiente:
"Artículo 505.- Además de lo dispuesto para etiquetado general y para regímenes especiales, las preparaciones comerciales de alimentos infantiles deberán indicar en su etiqueta lo siguiente:
a) Su denominación de colado o picado, según las definiciones de este reglamento.
b) Se debe indicar la edad a partir de la cual podrá consumirse el producto, teniendo en cuenta su composición, textura y otras propiedades particulares. La edad indicada será, como mínimo, de seis meses para cualquier producto.
c) En los casos en que los productos contengan menos proteínas que 3g/100 kcal deberá indicar claramente y destacado en la cara frontal del envase la siguiente frase: "NO REEMPLAZA UNA COMIDA COMPLETA PARA UN NIÑO".
d) En este tipo de productos, no deberán incorporarse en los rótulos ni publicidad de los mismos, declaraciones de propiedades saludables".
10.- Agrégase el siguiente artículo 505 bis:
"Artículo 505 bis.- La información y rotulación nutricional de los alimentos comprendidos en este párrafo deberán expresarse por cada 100 g o 100 ml, según corresponda, y por cada porción del producto listo para el consumo. Además, opcionalmente, podrá expresarse por cada 100 kilocalorías (kcal) utilizables del producto".