APRUEBA DEFINICIONES Y LINEAMIENTOS PARA LA APLICACIÓN DE MEDIDAS QUE FACILITEN LA ADQUISICIÓN DE REMEDIOS EN EL CONTEXTO DE UNA ALERTA SANITARIA POR EPIDEMIA O PANDEMIA, CONFORME AL ARTÍCULO 1° DE LA LEY N° 21.267
Núm. 24 exenta.- Santiago, 12 de enero de 2021.
Vistos:
La ley N° 21.267, que establece medidas para facilitar la adquisición de remedios en el contexto de una alerta sanitaria por epidemia o pandemia; el decreto con fuerza de ley N° 1, de 2005, del Ministerio de Salud, que fija el texto refundido, coordinado y sistematizado del decreto ley N° 2.763, de 1979, y de las leyes N° 18.933 y N° 18.469; decreto con fuerza de ley N° 725, de 1967, del entonces Ministerio de Salud Pública, Código Sanitario; decreto N° 4, de 2020, del Ministerio de Salud, que decreta alerta sanitaria por el periodo que se señala y otorga facultades extraordinarias que indica por emergencia de salud pública de importancia internacional (ESPII) por brote del nuevo coronavirus (2019-NCOV); el decreto N° 466, de 1984, del Ministerio de Salud, que aprueba reglamento de farmacias, droguerías, almacenes farmacéuticos, botiquines y depósitos autorizados; decreto N° 404, de 1983, del Ministerio de Salud, reglamento de estupefacientes; decreto N° 405, de 1983, del Ministerio de Salud, reglamento de productos psicotrópicos; y en la resolución N° 7, de 2019, de Contraloría General de la República, que fija normas sobre exención del trámite de toma de razón, y
Considerando:
1° Que, al Ministerio de Salud le compete ejercer la función que le corresponde al Estado de garantizar el libre e igualitario acceso a las acciones de promoción, protección y recuperación de la salud y de rehabilitación de la persona enferma, así como coordinar, controlar y, cuando corresponda, ejecutar tales acciones.
2° Que, la ley N° 21.267, que establece medidas para facilitar la adquisición de remedios en el contexto de una alerta sanitaria por epidemia o pandemia, dispuso en su artículo 1° una serie de medidas relativas al expendio y dispensación de productos farmacéuticos, vigencia y validez de recetas médicas durante una alerta sanitaria dictada con ocasión de una epidemia o pandemia.
3° Que, el 5 de febrero de 2020, este Ministerio dictó el decreto N° 4, de 2020, que decreta Alerta Sanitaria por el período que se señala y otorga facultades extraordinarias que indica por Emergencia de Salud Pública de Importancia Internacional (ESPII) por brote del nuevo coronavirus (2019-NCOV).
4° Que, para la adecuada implementación del artículo 1° de la ley N° 21.267, y en el contexto ya señalado en el considerando anterior, con el objeto de resguardar el principio de certeza jurídica junto con la debida armonía y coherencia de las normas, corresponde determinar los lineamientos y definiciones que permitan que todas las personas puedan acceder de manera oportuna a los medicamentos que requieran, en el periodo de pandemia en el que nos encontramos, resguardando la seguridad de los pacientes y permitiendo una fiscalización uniforme por parte de la autoridad sanitaria a lo largo del país.
5° Que, teniendo presente lo anterior, dicto la siguiente:
Resolución:
1° Apruébase el documento denominado "Definiciones y lineamientos para la aplicación de medidas que faciliten la adquisición de productos farmacéuticos en el contexto de la alerta sanitaria dictada mediante decreto N° 4, de 2020, del Ministerio de Salud", cuyo texto es el siguiente:
DEFINICIONES Y LINEAMIENTOS PARA LA APLICACIÓN DE MEDIDAS QUE FACILITEN LA ADQUISICIÓN DE PRODUCTOS FARMACÉUTICOS EN EL CONTEXTO DE LA ALERTA SANITARIA DICTADA MEDIANTE DECRETO N° 4, DE 2020, DEL MINISTERIO DE SALUD
DIRECTRICES DE APLICACIÓN.
I. Vigencia y validez de las recetas durante el decreto N° 4, de 2020, del Ministerio de Salud, que decreta alerta sanitaria por el período que se señala y otorga facultades extraordinarias que indica por emergencia de salud pública de importancia internacional (ESPII) por brote del nuevo coronavirus (2019-NCOV).
Las recetas que hayan sido extendidas desde el 8 de agosto de 2019, tendrán vigencia para su dispensación en algún establecimiento, hasta el 8 de agosto de 2021 o hasta seis meses después del término de la alerta, en caso que esta fuera prorrogada.
Para efectos de su expendio, vigencia y validez para la dispensación de los productos farmacéuticos prescritos en una receta, se tendrán las siguientes consideraciones:
1. Tratándose de recetas no sujetas a retención en el establecimiento de entrega y que incorporen la prescripción de productos farmacéuticos de uso crónico, se podrá realizar como máximo la entrega de una cantidad suficiente de los medicamentos prescritos para el tratamiento de un periodo de tres meses.
Para efectos de estas instrucciones, se entenderá como medicamento de uso crónico aquel destinado al tratamiento de una enfermedad de aquellas reconocidas como tales, cuyo uso se requiere por un periodo prolongado de tiempo (mayor a dos meses) y que se indica como tal en la respectiva receta bajo la frase "para uso crónico" o similar. En caso que no se indique en la prescripción, el profesional del establecimiento de entrega del fármaco, será responsable de evaluar si el producto prescrito es de uso crónico, atendiendo lo que señale el paciente o adquirente y la naturaleza e indicaciones propias del medicamento que se trate, propendiendo en todo momento al uso racional de los medicamentos.
Al momento de la entrega periódica de los medicamentos prescritos, deberá dejarse constancia al reverso de la receta, indicando la cantidad de productos entregados y la fecha, con timbre del establecimiento que se trate.
2. Tratándose de recetas de productos psicotrópicos, estupefacientes u otras sujetas a retención en el establecimiento de entrega, éstas sólo tendrán validez para la dispensación en un solo acto de los productos farmacéuticos prescritos en ellas, por hasta seis meses después del término de la alerta sanitaria, es decir, hasta el 8 de agosto de 2021, en caso que no sea prorrogada.
II. Expendio de medicamentos durante la vigencia del decreto N° 4, de 2020, del Ministerio de Salud, que decreta alerta sanitaria por el periodo que se señala y otorga facultades extraordinarias que indica por emergencia de salud pública de importancia internacional (ESPII) por brote del nuevo coronavirus (2019-NCOV).
Al amparo de la ley N° 21.267, cuando se decrete alerta o emergencia sanitaria en razón de una epidemia o pandemia y durante toda su vigencia, los productos farmacéuticos podrán ser expendidos por cualquier establecimiento autorizado para ello, mostrando una copia de la receta que los prescriba, ya sea en formato físico o digital, en cualquiera de sus formas.
Para efectos de la aplicabilidad de las indicaciones antes referidas y considerando la necesidad universal de farmacoterapia de las personas, la situación y restricciones de movilidad y funcionamiento de los establecimientos durante la pandemia; así como también las diferentes modalidades de atención y tecnologías informáticas disponibles, se tendrán las siguientes consideraciones:
1. Definiciones:
1.1. Copia de receta en formato digital: Aquellos formatos electrónicos que contengan la imagen de una receta emitida en formato físico por un profesional habilitado o recetas emitidas en sistemas electrónicos de prescripción y presentadas para su expendio por medios digitales.
1.2. Copia de una receta en formato físico: Aquellas que se presentan en papel para su expendio y son obtenidas ya sea por la impresión de una receta cuya imagen se contiene en un formato electrónico según las indicaciones anteriores o por fotocopia de una receta emitida en formato físico por un profesional habilitado.
1.3. Expendio: Toda entrega de productos farmacéuticos, sea mediante la venta directa de los medicamentos o la entrega ejecutada en razón del pago de éstos por parte de un seguro de salud, público o privado, con cobertura total o parcial.
2. Precisiones importantes:
2.1. No será considerada copia de una receta, aquella elaborada por técnicos o profesionales de la salud en los establecimientos que expenden o en los establecimientos de salud, y que consiste en la transcripción de los datos desde la receta a otro soporte físico, con el fin de que el paciente conozca las indicaciones de uso del producto prescrito.
2.2. No serán consideradas como copias de recetas aquellas obtenidas a partir de la digitalización, impresión o fotocopia de autocopiativos de talonarios de recetas o el mismo autocopiativo.
2.3. El expendio de medicamentos que se realice exhibiendo una copia de la receta en formato gráfico o digital, aplicará a todo establecimiento farmacéutico o asistencial autorizado para la entrega de dichos productos, tales como farmacias, botiquines, almacenes farmacéuticos y establecimientos asistenciales de salud.
3. Modalidades para el expendio: Las copias de recetas en formato digital podrán exhibirse de las siguientes formas:
3.1 Presentarse por medio de soportes electrónicos de diversa índole, tales como smartphone, tablets u otro similar.
3.2. Ser comunicadas o transmitidas al establecimiento que se trate, mediante correo electrónico u otra forma de envío del archivo correspondiente.
3.3. Tratándose de recetas retenidas y considerando la obligación de registro y archivo establecido según reglamentos correspondientes, el establecimiento de expendio deberá imprimir la receta si es que no recibe una copia impresa del adquiriente.
III. Registros y archivos.
Sin perjuicio de las condiciones excepcionales de expendio establecidas en la ley N° 21.267, los establecimientos autorizados para la entrega de medicamentos deberán contar con los archivos y registros indicados en los decretos supremos N° 404, de 1983, N° 405, de 1983 y N° 466, de 1984, todos del Ministerio de Salud, referidos a los Reglamentos de Estupefacientes, de Productos Psicotrópicos y de Farmacias, Droguerías, Almacenes Farmacéuticos, Botiquines y Depósitos autorizados, respectivamente. Para los referidos fines podrán imprimir una copia de la receta digitalizada, si fuera el caso.
IV. Reserva de datos.
La receta y su contenido, así como su imagen digitalizada, serán reservados y considerados datos sensibles, sujetándose a lo establecido en la ley N° 19.628 o la que la reemplace, así como también a lo dispuesto en las leyes N° 20.584 y demás leyes y reglamentos que sean aplicables en la materia.
V. Sistema para Validación de Recetas Gráficas.
Tratándose de la entrega de medicamentos en el que se empleen copias de recetas en formato digital o físico, que incluyan productos sujetos a control legal por medio de receta retenida o cheque, previo a la entrega de los productos, las recetas deberán ser validadas en el sistema electrónico del Ministerio de Salud, denominado "Sistema para Validación de Recetas Gráficas", el cual fuera implementado al amparo de las disposiciones del artículo 38° del decreto N° 466, de 1984, ya referido.
El "Sistema para Validación de Recetas Gráficas" sólo será aplicable a los establecimientos no asistenciales que realicen venta directa de los medicamentos, tales como farmacias comunitarias y similares.
En el "Sistema para Validación de Recetas Gráficas" será responsabilidad del prescriptor incorporar al sistema electrónico aludido la receta digitalizada, así como también informar periódicamente a la autoridad sanitaria respectiva el documento emitido y remitir copia del mismo previa inutilización, inscribiendo sobre ésta la palabra "digitalizada".
En el caso de recetas cheques, deberá el prescriptor remitir la receta original a la autoridad sanitaria correspondiente al domicilio del prescriptor, para lo cual se tendrá un plazo máximo de dos meses, pudiendo ingresarlas en la respectiva oficina de partes o remitirlas vía correo, con entrega certificada, en sobre cerrado dirigido a la Unidad de Prestadores de Salud que corresponda.
Será responsabilidad del prescriptor eliminar aquellas recetas que emita y que no corresponden a recetas cheque, debiendo inutilizarlas y destruirlas.
En el caso de recetas emitidas por sistemas electrónicos de prescripción y que incorporen medicamentos similares a psicotrópicos y estupefacientes -con receta retenida-, se deberá verificar que ésta no haya sido dispensada previamente. Para ello, los sistemas que permitan la emisión de recetas electrónicas deberán proveer de herramientas de gestión documental, para que la dispensación de la receta sea registrada y posible de inhabilitar para su uso posterior. Estos sistemas quedarán bajo la fiscalización de las Secretarías Regionales Ministeriales de Salud.
Las características, condiciones de acceso y funcionamiento del referido Sistema se anexan en documento denominado "Sistema para la Validación de Recetas Gráficas".
VI. Uso racional de medicamentos.
Los químicos farmacéuticos y demás profesionales a cargo de los establecimientos de entrega de medicamentos serán responsables de propender el uso racional de éstos por parte de quienes los adquieran para sí mismos o para un tercero, así como también de verificar que no acontezcan condiciones que hagan recomendable la suspensión o revisión del tratamiento que se trate, tales como la aparición de reacciones adversas, ausencia de los resultados esperados u otra condición, instancia en la cual deberán informar adecuadamente tales recomendaciones.
VII. Fiscalización.
Las Secretarías Regionales Ministeriales de Salud del país y el Instituto de Salud Pública, en sus respectivos ámbitos de competencia, podrán fiscalizar la correcta aplicación de la ley N° 21.267 y de estos lineamientos.
El uso malicioso de recetas presentadas en forma digitalizada o copia física, comprendiéndose en éste la falsificación o adulteración por modificación de las indicaciones del documento o su empleo en la adquisición reiterada y en cantidades injustificadas respecto de la prescripción, será sancionado conforme al Libro X del Código Sanitario y al Código Penal.
Con el objeto de perseguir la responsabilidad penal que corresponda, la Secretaría Regional Ministerial de Salud o el Instituto de Salud Pública, en su caso, deberá realizar la respectiva denuncia ante los órganos competentes (tribunales con competencia en lo penal, Ministerio Público o a la policía).
 .
.  .
.  .
. 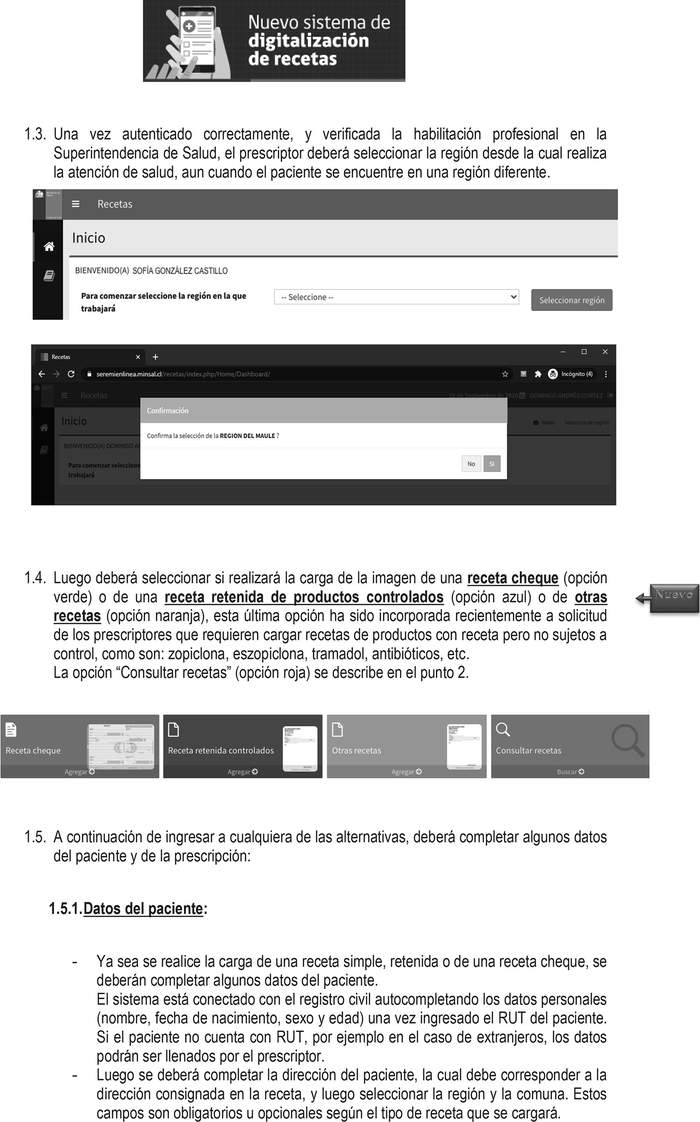 .
.  .
.  .
.  .
. .
. .
.  .
.  .
.  .
. .
. 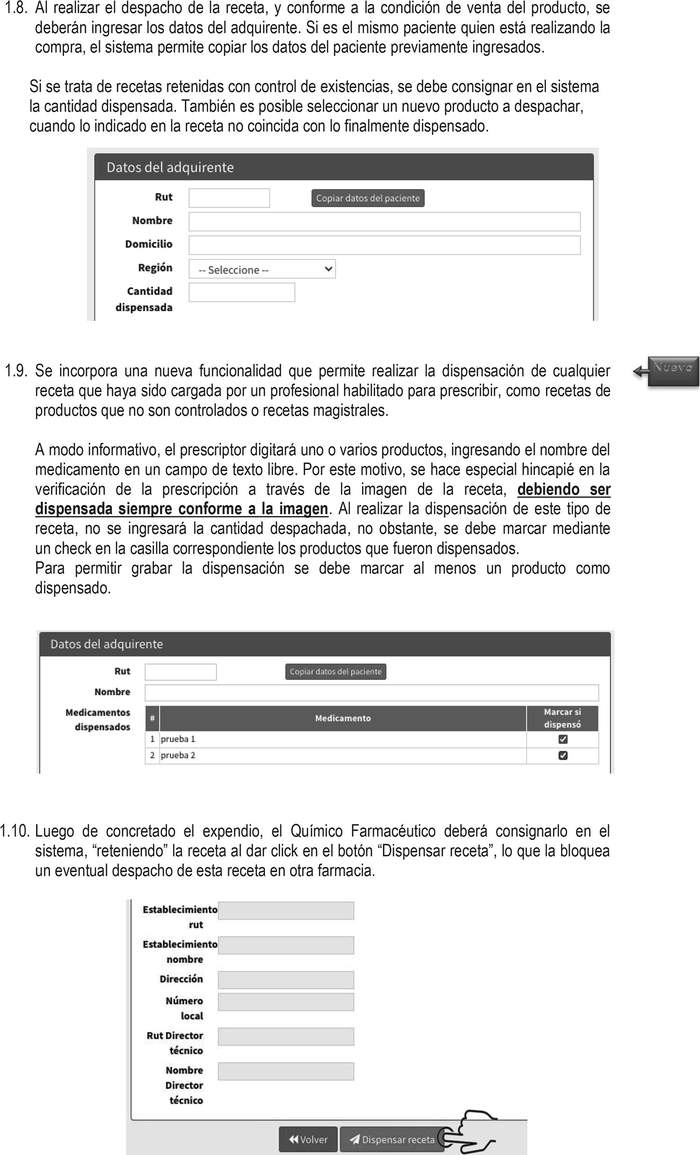 .
. .
. .
. 2° Publícase por la División de Políticas Públicas Saludables y Promoción, el texto íntegro de la presente resolución y del documento "Sistema para la Validación de Recetas Gráficas" en el sitio web del Ministerio de Salud.
Anótese, comuníquese y publíquese.- Paula Daza Narbona, Subsecretaria de Salud Pública.
Transcribo para su conocimiento resolución exenta N° 24, de 12 de enero de 2021.- Por orden de la Subsecretaria de Salud Pública.- Saluda atentamente a Ud., Jorge Hübner Garretón, Jefe de División Jurídica.