MODIFICA EL DECRETO Nº 500 EXENTO Y EL DECRETO Nº 27 EXENTO, AMBOS DE 2012, DEL MINISTERIO DE SALUD
Núm. 29 exento.- Santiago, 27 de abril de 2021.
Vistos:
Lo dispuesto en el artículo 4º del Libro I del decreto con fuerza de ley Nº 1 de 2005, del Ministerio de Salud, que fija el texto refundido, coordinado y sistematizado del decreto ley Nº 2.763, de 1979 y de las leyes 18.469 y 18.933; decreto con fuerza del ley Nº 725, de 1967, del entonces Ministerio de Salud Pública, Código Sanitario; las disposiciones del artículo 52º y aquellas del inciso 1º del artículo 221º, contenidas en el decreto supremo Nº 3, de 2010, del Ministerio de Salud, Reglamento del Sistema Nacional de Control de Productos Farmacéuticos de Uso Humano; lo solicitado por la Jefa de Gabinete de la Subsecretaría de Salud Pública, mediante su memorándum B 35 Nº 155, de 16 de abril de 2021; la resolución Nº 7, de 2019, de la Contraloría General de la República, que fija normas sobre exención del trámite de toma de razón, y teniendo presente las facultades concedidas en el decreto supremo Nº 28, de 2009, del Ministerio de Salud, dicto el siguiente,
Considerando:
1º Que, al Ministerio de Salud le compete ejercer la función que corresponde al Estado de garantizar el libre e igualitario acceso a las acciones de promoción, protección y recuperación de la salud y de rehabilitación de la persona enferma; así como coordinar, controlar y, cuando corresponda, ejecutar tales acciones.
2º Que, conforme con lo anterior, corresponde a esta Secretaría de Estado formular, fijar y controlar las políticas de salud.
3º Que, de acuerdo con el artículo 94º del Código Sanitario, compete al Ministerio de Salud velar por el acceso de la población a medicamentos o productos farmacéuticos de calidad, seguridad y eficacia.
4º Que, el artículo 221, inciso 1º, del Reglamento del Sistema Nacional de Control de Productos Farmacéuticos de Uso Humano, dispone que "el Ministerio de Salud, mediante decreto, aprobará la norma técnica que determine los productos que requieren demostrar su equivalencia terapéutica, estableciendo las listas de los principios activos y de los productos farmacéuticos que servirán de referencia de los mismos, cuando corresponda; lo que podrá hacerse a proposición del Instituto.".
5º Que, en virtud de lo anterior, el Ministerio de Salud dictó el decreto exento Nº 500, de 2012, que aprueba la Norma General Técnica Nº 136, que "Determina los principios activos contenidos en los productos farmacéuticos que deben demostrar su Equivalencia Terapéutica y lista de productos farmacéuticos que sirven de referencia de los mismos", modificada en varias oportunidades.
6º Que, asimismo, el artículo 221 inciso 3º del reglamento antes citado, prescribe que por decreto del Ministerio "se aprobará la norma técnica que establezca los criterios técnicos necesarios para determinar los productos farmacéuticos que requieran demostrar equivalencia terapéutica".
7º Que, a raíz de lo anterior, esta Secretaría de Estado dictó el decreto exento Nº 27, de 2012, que aprueba la Norma Técnica Nº 131 que "Define los criterios destinados a establecer la Equivalencia Terapéutica en productos farmacéuticos en Chile.".
8º Que, mediante memorándum Nº 155, de 16 de abril de 2021, la Jefa de Gabinete de la Subsecretaría de Salud Pública, ha estimado necesario realizar modificaciones a las normas técnicas asociadas a la exigencia de Equivalencia Terapéutica.
9º Que, dichas modificaciones se refieren, en primer término, a acoger la proposición del Instituto de Salud Pública enviada mediante Ord. Nº 63, de 2021, respecto a incorporar diversos principios activos al listado contenido en la Norma Técnica Nº 131. Además, se incorporarán también la Clorpromazina y Colchicina al referido listado, denominado "Demostración de Equivalencia Terapéutica para principios activos no nuevos (maduros) de larga experiencia de uso.".
10º Que, por otra parte, en virtud del análisis de una reclamación particular, se advirtió la necesidad de establecer plazos para la presentación de estudios de Equivalencia Terapéutica en el caso de productos farmacéuticos que contengan uno o más de los principios activos señalados en la Norma Técnica Nº 136 y que se presentan en formas farmacéuticas distintas al producto de referencia.
11º Que, además, el Instituto de Salud Pública en su Ord. Nº 358, del 8 de abril de 2021, referido al estado de avance de las exigencias de demostración de Equivalencia Terapéutica, informó alrededor de un 30% de certificaciones efectivas. Los motivos del retraso estarían asociados a las restricciones establecidas en virtud de la emergencia sanitaria por pandemia de la enfermedad COVID-19. En ese sentido, existirían problemas en la ejecución de estudios "in vivo" tras las cuarentenas establecidas en las zonas de emplazamiento de los Centros de Investigación, complejidades en la importación de productos de referencia y, en el caso de las formas farmacéuticas líquidas, problemas en las validaciones de procesos, ya que existe prioridad nacional para la manufactura de productos de sedo-analgesia, requerido para la atención clínica de las personas que sufren cuadros graves de COVID-19.
12º Que, por lo antes expuesto, dicto el siguiente:
Decreto:
Artículo primero: Reemplázase la tabla contenida en el numeral 7 del decreto exento Nº 27, de 2012, del Ministerio de Salud, que "Aprueba Norma Técnica Nº 131 denominada "Norma que define los criterios destinados a establecer la Equivalencia Terapéutica en productos farmacéuticos en Chile.", por la siguiente:
LISTA DE PRINCIPIOS ACTIVOS NO NUEVOS (MADUROS) DE LARGA EXPERIENCIA DE USO
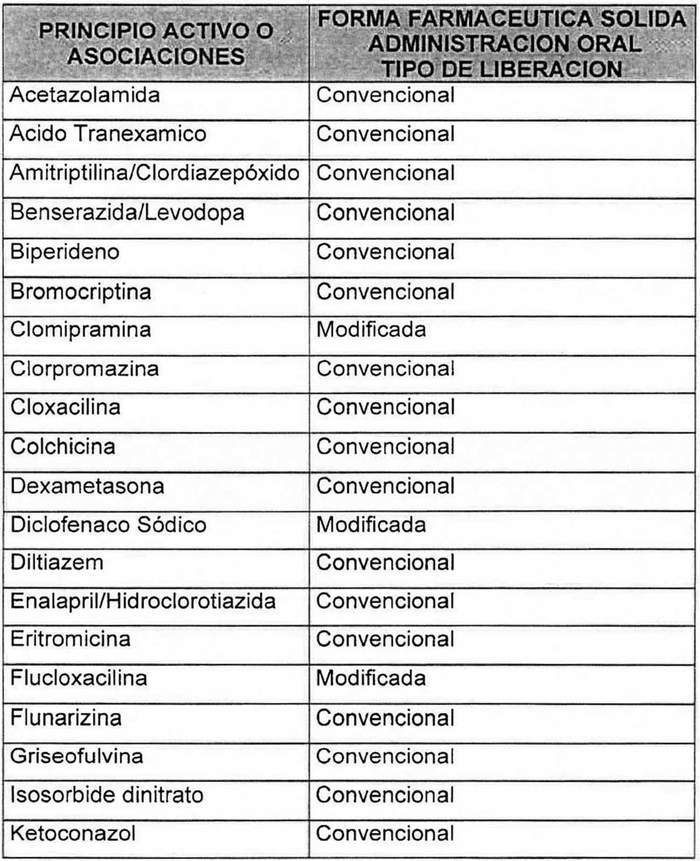
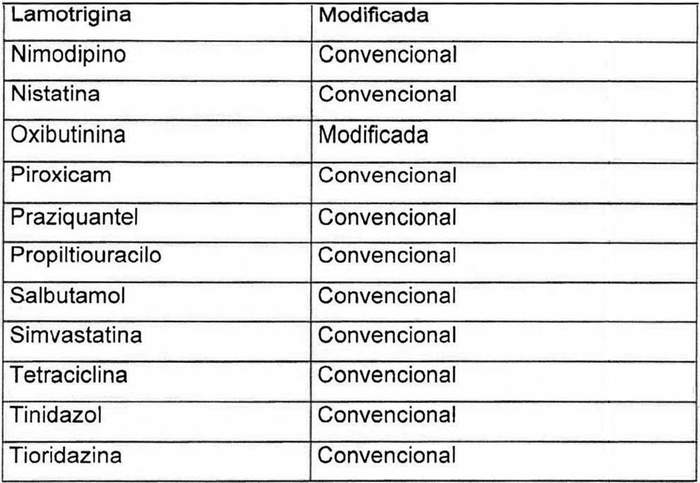
NOTA
El numeral 1° de la Resolución 716 Exenta, Salud, publicada el 17.08.2021, rectifica el principio activo flucloxacilina inserto en la tabla por el que la citada norma indica.
El numeral 1° de la Resolución 716 Exenta, Salud, publicada el 17.08.2021, rectifica el principio activo flucloxacilina inserto en la tabla por el que la citada norma indica.
Artículo segundo: Modificase el decreto exento Nº 500, de 1 de junio de 2012, del Ministerio de Salud, mediante el cual se aprobó la Norma Técnica Nº 136, denominada "Norma que determina los principios activos contenidos en productos farmacéuticos que deben demostrar su equivalencia terapéutica y lista de productos farmacéuticos que sirven de referencia de los mismos" en la forma que a continuación se indica:
a) Sustitúyase, el inciso segundo del artículo quinto, por el siguiente:
"Otórgase plazo hasta el 30 de septiembre de 2022 a aquellos titulares de productos farmacéuticos registrados en Chile, que deban cumplir con la demostración de equivalencia terapéutica. El mismo plazo aplicará para productos farmacéuticos que deban cumplir con la señalada demostración y se presenten como formulaciones masticables, bucodispersables, dispersables, láminas bucodispersables o cualquier otra forma farmacéutica de administración oral, que difiera de aquella en la que se presenta el respectivo producto de referencia establecido para la realización de los estudios de equivalencia terapéutica."
Artículo tercero: Un texto actualizado de las normas, conteniendo las modificaciones que se aprueban en este decreto y las anteriores realizadas, se mantendrá en el Departamento de Políticas Farmacéuticas y Profesiones Médicas de la División de Políticas Públicas Saludables y Promoción de la Subsecretaría de Salud Pública, entidad que a su vez deberá velar por su oportuna publicación en la página web del Ministerio de Salud, www.minsal.cl, para su adecuado conocimiento y difusión, debiendo además asegurar que las copias y reproducciones que se emitan guarden estricta concordancia con el texto aprobado.
Artículo cuarto: Las disposiciones del presente decreto regirán desde el día 30 de abril de 2021.
Anótese y publíquese.- Enrique Paris Mancilla, Ministro de Salud.
Transcribo para su conocimiento decreto exento Nº 29 - 27 de abril 2021.- Por orden de la Subsecretaria de Salud Pública.- Saluda atentamente a Ud., Jorge Hübner Garretón, Jefe de la División Jurídica, Ministerio de Salud.