ESTABLECE OBLIGATORIEDAD DE IMPLEMENTAR MÉTODO DE ENSAYO PARA LA DETERMINACIÓN DEL COMPLEJO BURKHOLDERIA CEPACIA, MICROORGANISMOS OBJETABLES, EN MATERIAS PRIMAS Y PRODUCTOS TERMINADOS QUE INDICA
Núm. 1.881 exenta.- Santiago, 29 de abril de 2022.
Visto:
Lo dispuesto en Art. 64º del DS 3/2010, del Ministerio de Salud, faculta al Instituto de Salud Pública de Chile a exigir las modificaciones al registro sanitario que sean necesarias para garantizar la calidad, seguridad y eficacia de los productos, cuando se forme la convicción que las condiciones del registro sanitario representen un riesgo en su seguridad y eficacia; el memorando Nº 345 de fecha 27/04/2022 del Jefe (S) del Departamento Agencia Nacional de Medicamentos, por el cual adjunta informe técnico y solicita evaluar la pertinencia de emitir una resolución exenta que exija la implementación de método de ensayo para determinación de la ausencia de complejo Burkholderia cepacia en agua calidad farmacéutica y en ciertas preparaciones farmacéuticas no estériles en base acuosa y además para que este parámetro microbiológico sea incorporado en las especificaciones de producto terminado.
Considerando:
Primero. Que, de conformidad con lo dispuesto en el artículo 57 del decreto con fuerza de Ley Nº 1, de 2005, del Ministerio de Salud, el Instituto de Salud Pública de Chile servirá de laboratorio nacional y de referencia en los campos de la microbiología, inmunología, bromatología, farmacología, imagenología, radioterapia, bancos de sangre, laboratorio clínico, contaminación ambiental y salud ocupacional y desempeñará las demás funciones que le asigna la presente Ley, comprendiéndose entre sus atribuciones, según lo dispuesto en el artículo 59 del mismo cuerpo legal, las de ejercer las actividades relativas al control de calidad de medicamentos, entendiéndose que en esa actividad se encuentra contemplada, entre otras, la de controlar las condiciones de internación, exportación, fabricación, distribución, expendio y uso a cualquier título de estos productos.
Segundo. Que, el Código Sanitario, por su parte, establece en el artículo 96 que el Instituto es la autoridad encargada en todo el territorio nacional del control sanitario de los productos farmacéuticos, de los establecimientos del área y de fiscalizar el cumplimiento de las disposiciones que sobre esta materia se contienen en este Código y sus reglamentos.
Tercero. Que, el complejo de Burkholderia cepacia (CBC) es un grupo de especies bacterianas gramnegativas, estrechamente relacionadas, formado por 22 especies conocidas a la fecha (Ver tabla 1); este complejo se identificó como un importante patógeno oportunista que causa morbilidad y mortalidad en personas inmunocomprometidas, especialmente en aquellas con fibrosis quística, enfermedad granulomatosa crónica, pacientes con ventilación mecánica, personas inmunodeprimidas y personas con una enfermedad subyacente grave. Además, se han documentado numerosos brotes de infecciones nosocomiales debidas a transmisión de persona a persona o por contaminación de equipos pudiendo causar bacteremia, artritis séptica, osteomielitis, meningitis, peritonitis, infecciones del tracto urinario, respiratorio y endocarditis, entre otras. Cabe hacer notar que algunas especies del complejo Burkholderia cepacia son significativamente importantes como patógenos en humanos debido a que tienen un alto grado de resistencia a los antibióticos, una excepcional transmisibilidad en ambientes nosocomiales y gran capacidad para sobrevivir intracelularmente.
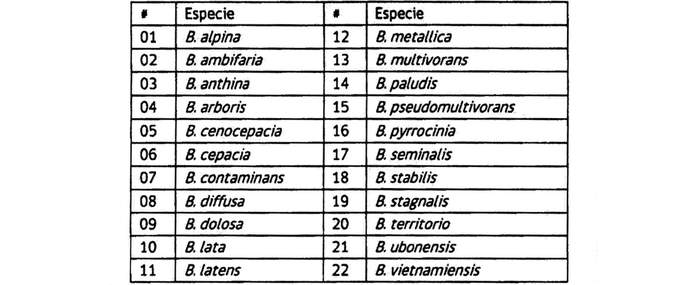
Tabla 1 Lista de especies del complejo Burkholderia cepacia descritas hasta 2017
Cuarto. Que, las 22 especies, descritas a la fecha, del complejo Burkholderia cepacia son un grupo muy estable dentro del género Burkholderia cuando se analiza filogenéticamente el gen ADNr 16S y presentan hasta el 78% de sus genes en común. A pesar de sus similitudes, un número importante de especies del complejo Burkholderia cepacia está siendo caracterizado para nombrarlas formalmente como nuevas especies. En general, estas especies presentan genomas de gran tamaño (hasta 9 Mpb) divididos en 2-5 replicones, típicamente dispuestos en tres cromosomas y un gran plásmido. Esta característica aporta una gran versatilidad metabólica sumado la capacidad de resistencia a desinfectantes y a agentes antimicrobianos logrando sobrevivir durante un largo período de tiempo con escasos nutrientes y multiplicarse fácilmente en ambientes acuosos, como agentes desinfectantes y fluidos intravenosos utilizados en hospitales. Este complejo CBC es capaz de sobrevivir o multiplicarse en una variedad de productos no estériles formulados con agua, por su potencialidad de ser resistente a los preservantes utilizados en productos farmacéuticos.
Quinto. Que, los organismos del complejo Burkholderia cepacia son comunes en el medio ambiente, incluida el agua, y por lo tanto son omnipresentes en la mayoría de los entornos. A nivel internacional durante los últimos años, se ha visto una frecuencia al alza de microorganismos contaminantes pertenecientes al complejo de Burkholderia cepacia (Burkholderia cepacia complex) presentes en las contaminaciones de fármacos no estériles que llevan agua en su composición, siendo en este último año el responsable de la mayoría de los retiros del mercado por contaminación microbiológica.
Sexto. Que, en relación a la fabricación de productos farmacéuticos, se ha podido establecer que el punto de origen más común de las contaminaciones microbiológicas por organismos de este complejo, corresponde a los sistemas de producción de agua farmacéutica, situación que podría tener relación con deficiencias en el diseño, operación y monitoreo de estos sistemas de producción.
Séptimo. Que, a partir de diciembre de 2019, la Farmacopea de los Estados Unidos (USP) publicó oficialmente el capítulo <60> Examen Microbiológico de productos No Estériles: Pruebas para el Complejo Burkholderia Cepacia, mediante el cual a través de la utilización de un agar selectivo -indicador y promotor del crecimiento para Burkholderia cepacia, Burkholderia cenocepacia y Burkholderia multivorans e inhibitorio para Pseudomonas aeruginosa-, es posible determinar la ausencia del complejo Burkholderia cepacia en agua, materias primas y productos farmacéuticos terminados, cuando se aplican todas las medidas de control interno descritas en el mismo capítulo.
Octavo. Que, la autoridad regulatoria de los Estados Unidos, Food and Drug Administration (FDA) ha advertido a su industria farmacéutica aplicar el método/ examen <60> de la USP especialmente en productos farmacéuticos no estériles a base de agua, basado en que se han producido retiros repetidos de antisépticos contaminados, como povidona yodada, cloruro de benzalconio y gluconato de clorhexidina, en los EE.UU., así como en el extranjero. Estos productos farmacéuticos se encuentran presentes en prácticamente todos los establecimientos de salud, siendo afectados particularmente los pacientes vulnerables debido a su condición médica.
Noveno. Que, la autoridad regulatoria de Argentina, Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT), ha redactado el documento ANMAT-MED-MPF-001-000, actualmente en periodo de consulta pública, el que incorporará su determinación en productos farmacéuticos, y la autoridad regulatoria de Colombia, Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA), ha emitido alertas de dispositivos médicos contaminados con Burkholderia cepacia y de retiros del mercado asociados a este complejo.
Décimo. Que, en las inspecciones rutinarias de Buenas Prácticas de Manufactura desde el 2020, este Instituto ha venido constatando la presencia de este complejo en los sistemas de producción, almacenamiento y distribución de agua purificada de los laboratorios farmacéuticos de producción, por lo que existiría un riesgo potencial de su presencia de manera inadvertida en algunos productos farmacéuticos con el respectivo impacto en pacientes susceptibles.
Undécimo. Que, desde el año 2021 a la fecha, el Instituto de Salud Pública ha recibido e investigado al menos 15 denuncias por sospecha de contaminación por el complejo Burkholderia cepacia en productos farmacéuticos y preparados magistrales debido a la investigación de un brote multicéntrico en establecimientos de salud a nivel nacional. A la fecha se ha confirmado la presencia de este complejo en 2 lotes de productos farmacéuticos.
Duodécimo. Que, de acuerdo a lo dispuesto en el artículo 178 del decreto supremo Nº 3, de 2010, del Ministerio de Salud, "Los requerimientos de calidad de las especialidades farmacéuticas serán los establecidos en las especificaciones del producto y los métodos de control que se utilizarán serán los aprobados al otorgarse el respectivo registro sanitario o en sus modificaciones posteriores".
Decimotercero. Que, por otro lado, el artículo 64 del mismo reglamento establece que el Instituto podrá exigir, mediante resolución fundada, exigir que dentro de un plazo definido se realicen las modificaciones del registro que sean necesarias para garantizar la calidad, seguridad y eficacia en el uso de una o varias especialidades farmacéuticas, cuando mediante antecedentes científicos se forme la convicción que alguna de las condiciones de uso autorizadas presenta un riesgo en su seguridad y eficacia.
Decimocuarto. Que, dado todo lo expuesto el Instituto de Salud Pública de Chile se ha formado la convicción de la necesidad de establecer un reforzamiento en la vigilancia en las actividades de producción y garantía de calidad de los fabricantes de productos farmacéuticos para prevenir riesgos de contaminación microbiológica, especialmente en relación a microorganismos objetables como el complejo Burkholderia cepacia, así como la detección de problemas emergentes y actuar de manera oportuna para evitar la exposición de pacientes y consumidores a medicamentos inseguros.
Teniendo presente lo dispuesto en los Título I del Libro Cuarto y en los Títulos II y III del Libro Décimo, todos del Código Sanitario; lo dispuesto en el decreto supremo 3, de 2010, del Ministerio de Salud; en los artículos 59 letra b), 60 y 61 letra b) del decreto con fuerza de ley Nº 1, de 2005, del Ministerio de Salud, que fija el texto refundido, coordinado y sistematizado del decreto ley Nº 2.763, de 1979, y de las leyes Nº 18.933 y Nº 18.469; en la resolución Nº 7, de 2019, de la Contraloría General de la República; y las facultades que me confiere el decreto Nº 51, de 2020, del Ministerio de Salud, dicto la siguiente:
Resolución:
1. Establécese la obligatoriedad para los laboratorios de control de calidad pertenecientes a los laboratorios de producción farmacéutica o laboratorios externos de control de calidad de implementar un método microbiológico de ensayo apropiado para la determinación del complejo Burkholderia cepacia, microorganismo objetable, cuyo alcance corresponderá a materias primas como agua calidad farmacéutica (producción propia o suministro externo) y/o materias primas cuyo contenido de agua (actividad de agua -aw-) esté por sobre 0,6 (a w > 0,6), así como para productos farmacéuticos terminados no estériles a base de agua, tales como preparaciones acuosas de uso oral, oromucosal, dérmicas, nasales y/o preparaciones para inhalación; con el fin de garantizar que los componentes de un producto farmacéutico y el lote del producto terminado antes de su distribución se encuentren libres de este contaminante.
Los establecimientos de producción farmacéutica que posean sistemas propios de generación, almacenamiento y distribución de agua purificada (laboratorios farmacéuticos de producción y/o recetarios magistrales) deberán incorporar este método como parte de los programas de monitoreo rutinario de dichos sistemas.
2. Establécese Resolución 3975 EXENTA,
SALUD
N° 5
D.O. 13.09.2022la obligatoriedad de incorporar como parámetro microbiológico la ausencia del complejo de Burkholderia cepacia en las especificaciones de producto terminado de medicamentos no estériles a base de agua, tales como preparaciones acuosas de uso oral, oromucosal, dérmicas, nasales y/o preparaciones para inhalación.
SALUD
N° 5
D.O. 13.09.2022la obligatoriedad de incorporar como parámetro microbiológico la ausencia del complejo de Burkholderia cepacia en las especificaciones de producto terminado de medicamentos no estériles a base de agua, tales como preparaciones acuosas de uso oral, oromucosal, dérmicas, nasales y/o preparaciones para inhalación.
Para tales efectos deberá presentar ante este Instituto los antecedentes correspondientes a la siguiente prestación Modificación de Especificaciones de Producto Farmacéutico o Pesticida (por producto), código de la prestación 4111020, cuya solicitud estará exenta de arancel.
3. Instrúyase implementar el método analítico para la detección del complejo Burkholderia cepacia el capítulo <60> Examen Microbiológico de Productos no Estériles: Pruebas para el Complejo Burkholderia Cepacia de la Farmacopea de Estados Unidos de América (USP), u otro método de detección validado.
A causa de la existencia de métodos de control alternativos al recomendado; producto del advenimiento de nuevas tecnologías en el ámbito de la microbiología, se requerirá de la validación completa de ellos para su implementación.
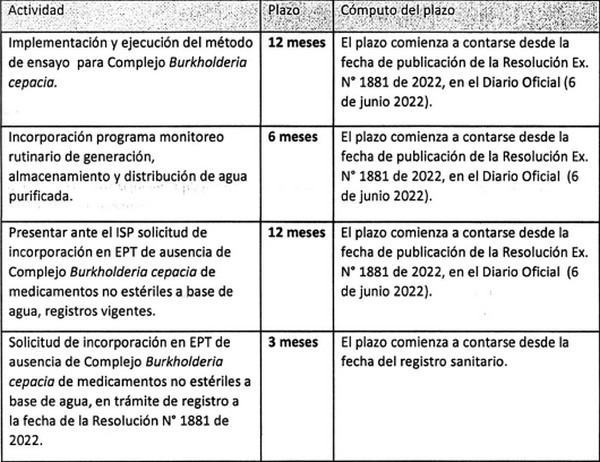
4. Establécese los siguientes plazos para la implementación y fiscalización del punto 1, con las pertinentes distinciones:
Anótese, comuníquese y publíquese su texto íntegro en el Diario Oficial.- Heriberto García Escorza, Director (S), Instituto de Salud Pública de Chile.