MODIFICA EL DECRETO Nº 500 EXENTO, DE 2012, QUE APRUEBA LA NORMA TÉCNICA Nº 136, NOMINADA "NORMA QUE DETERMINA LOS PRINCIPIOS ACTIVOS CONTENIDOS EN LOS PRODUCTOS FARMACÉUTICOS QUE DEBEN DEMOSTRAR SU EQUIVALENCIA TERAPÉUTICA Y LISTA DE PRODUCTOS FARMACÉUTICOS QUE SIRVEN DE REFERENCIA DE LOS MISMOS" Y EL DECRETO Nº 27 EXENTO, DE 2012, QUE APRUEBA LA NORMA TÉCNICA Nº 131, NOMINADA "NORMA QUE DEFINE LOS CRITERIOS DESTINADOS A ESTABLECER EQUIVALENCIA TERAPÉUTICA EN PRODUCTOS FARMACÉUTICOS EN CHILE", AMBOS DEL MINISTERIO DE SALUD
Núm. 48 exento.- Santiago, 26 de septiembre de 2025.
Vistos:
Lo dispuesto en los artículos 1 y 19 Nº 9, del decreto supremo Nº 100, de 2005, del Ministerio Secretaría General de la Presidencia, que fija el texto refundido, coordinado y sistematizado de la Constitución Política de la República; en el decreto con fuerza de ley Nº 1, de 2005, del Ministerio de Salud, que fija texto refundido, coordinado y sistematizado del decreto ley Nº 2.763, de 1979 y de las leyes Nº 18.933 y Nº 18.469; en el decreto supremo Nº 136, de 2004, del Ministerio de Salud, Reglamento Orgánico del Ministerio de Salud; el Código Sanitario, aprobado por el decreto con fuerza de ley Nº 725, de 1967, del Ministerio de Salud; en la ley Nº 18.575, Ley Orgánica Constitucional de Bases Generales de la Administración del Estado; en el decreto Nº28, de 2009, del Ministerio de Salud, que faculta al Ministerio de Salud para firmar "Por orden del Presidente de la República" y delega facultades que indica en la Subsecretaria de Salud Pública y Subsecretario de Redes Asistenciales; en el decreto supremo Nº 3, de 2010, del Ministerio de Salud, que aprueba el Reglamento del sistema nacional de control de los productos farmacéuticos de uso humano; en el decreto exento Nº 500, de 1 de junio de 2012, del Ministerio de Salud, que aprueba la Norma Técnica Nº 136, nominada "Norma que determina los principios activos contenidos en los productos farmacéuticos que deben demostrar su Equivalencia Terapéutica y lista de productos farmacéuticos que sirven de referencia de los mismos"; en el decreto exento Nº 27, de 18 de enero de 2012, del Ministerio de Salud, que aprueba la Norma Técnica Nº 131 nominada "Norma que define los criterios destinados a establecer la equivalencia terapéutica en productos farmacéuticos en Chile"; en el memorándum B35/Nº 428, de 2025, de la División de Políticas Públicas Saludables y Promoción, de la Subsecretaría de Salud Pública; y lo dispuesto en la resolución Nº 36, de 2024, de la Contraloría General de la República, y
Considerando:
1º. Que, al Ministerio de Salud le compete ejercer la función que corresponde al Estado de garantizar el libre e igualitario acceso a las acciones de promoción, protección y recuperación de la salud y de rehabilitación de la persona enferma, así como coordinar, controlar y, cuando corresponda, ejecutar tales acciones.
2º. Que, conforme al artículo 94 del Código Sanitario, al Ministerio de Salud le corresponde velar por el acceso de la población a medicamentos o productos farmacéuticos de calidad, seguridad y eficacia, lo que llevará a cabo por sí mismo, a través de sus Secretarías Regionales Ministeriales y de los organismos que se relacionan con el Presidente de la República por su intermedio.
3º. Que, el Código Sanitario en su artículo 95, dispone que "Producto farmacéutico o medicamento es cualquier substancia natural, biológica, sintética o las mezclas de ellas, originada mediante síntesis o procesos químicos, biológicos o biotecnológicos, que se destine a las personas con fines de prevención, diagnóstico, atenuación, tratamiento o curación de las enfermedades o sus síntomas o de regulación de sus sistemas o estados fisiológicos particulares, incluyéndose en este concepto los elementos que acompañan su presentación y que se destinan a su administración".
4º. Que, el decreto supremo Nº 3, de 2010, del Ministerio de Salud, que aprueba el Reglamento del Sistema Nacional de Control de Productos Farmacéuticos de Uso Humano, establece en su artículo 221 que "El Ministerio de Salud, mediante decreto, aprobará la norma técnica que determine los productos que requieren demostrar su equivalencia terapéutica, estableciendo las listas de los principios activos y de los productos farmacéuticos que servirán de referencia de los mismos, cuando corresponda; lo que podrá hacer a proposición del Instituto".
Luego, el inciso 3º del mismo artículo, señala que "por decreto del Ministerio se aprobará la norma técnica que establezca los criterios técnicos necesarios para determinar los productos farmacéuticos que requieran demostrar equivalencia terapéutica".
5º. Que, en cumplimiento de lo anterior, el Ministerio de Salud dictó el decreto exento Nº 500, de fecha 1 de junio de 2012, que aprueba la Norma Técnica Nº 136, nominada "Norma que determina los principios activos contenidos en los productos farmacéuticos que deben demostrar su equivalencia terapéutica y lista de productos farmacéuticos que sirven de referencia de los mismos"; y el decreto exento Nº 27, de 18 de enero de 2012, que aprueba la Norma Técnica Nº 131 nominada "Norma que define los criterios destinados a establecer la equivalencia terapéutica en productos farmacéuticos en Chile"; ambos decretos con sus respectivas modificaciones posteriores.
6º. Que, mediante decreto exento Nº 35, de 2024, esta Secretaría de Estado modificó el decreto exento Nº 500, de 2012, otorgándose un plazo hasta el 30 de septiembre de 2025, para que todo titular de registro sanitario de un producto farmacéutico que reúna alguna de las características descritas en el Punto 4.2. de la Norma Técnica Nº 131, así como aquellos presentados en formulaciones masticables, bucodispersables, dispersables, láminas bucodispersables u otras formas de administración oral distintas de las del producto de referencia, presenten al Instituto de Salud Pública de Chile los antecedentes destinados a demostrar su equivalencia terapéutica.
7º. Que, el referido decreto afecta a un número significativo de registros sanitarios, los cuales presentan grados disímiles de avance en su proceso de certificación, según los antecedentes proporcionados por el Instituto de Salud Pública de Chile (ISP).
8º. Que, para el adecuado análisis de dicha situación, se requirieron antecedentes a la Agencia Nacional de Medicamentos (ANAMED) del Instituto de Salud Pública, los que fueron objeto de evaluación por un grupo técnico ad hoc integrado por profesionales de dicha Agencia, de la Central de Abastecimiento del Sistema Nacional de Servicios de Salud (CENABAST), de la División de Planificación Sanitaria, de la División de Gestión de la Red Asistencial, de la División de Atención Primaria, y del Departamento de Políticas y Regulaciones Farmacéuticas, Prestadores de Salud y Medicinas Complementarias de la División de Políticas Públicas Saludables y Promoción.
9º. Que, el análisis consideró múltiples parámetros, tales como el número de registros vigentes, la proporción de productos certificados y no certificados, la pertenencia de los fármacos a estrategias de salud pública, la información de adquisición y oferta a CENABAST, los antecedentes proporcionados por titulares de registros en encuestas ejecutadas por el Instituto de Salud Pública, así como datos de importación y expendio farmacéutico.
10º. Que, respecto de las formas farmacéuticas sólidas, se verificó un cumplimiento heterogéneo en los procesos de certificación, identificándose la necesidad de ampliar los plazos de demostración de Equivalencia Terapéutica en casos específicos y respecto de determinados medicamentos, por un periodo adicional de 24 meses, con el objeto de resguardar la Política de Equivalencia Terapéutica/Intercambiabilidad en Chile, prevenir quiebres de stock y asegurar la disponibilidad y acceso de la población a los medicamentos.
11º. Que, en relación con las formas farmacéuticas líquidas de composición acuosa, se verificó igualmente la necesidad de otorgar una prórroga de 24 meses, atendido que, pese a los avances en el número de productos certificados, aún subsisten formulaciones pendientes de demostrar su equivalencia terapéutica, cuya relevancia para la terapéutica nacional hace indispensable asegurar su continuidad en el mercado.
12º. Que, de igual forma, se revisaron los avances en certificación de formas farmacéuticas alternativas, verificándose una situación análoga y la necesidad de establecer una prórroga de 24 meses, aunque circunscrita únicamente a determinadas formulaciones.
13º. Que, adicionalmente, se estimó procedente actualizar el listado de principios activos clasificados como "no nuevos/maduros", así como el listado de productos de referencia para la realización de estudios de Equivalencia Terapéutica, conforme a la propuesta técnica de la Agencia Nacional de Medicamentos del Instituto de Salud Pública de Chile.
14º. Que, en mérito de lo expuesto, resulta necesario modificar los decretos exentos Nº 500 y Nº 27, ambos del año 2012, del Ministerio de Salud, a fin de establecer prórrogas y nuevos plazos de demostración de Equivalencia Terapéutica para determinados principios activos y formas de liberación; así como de formas farmacéuticas sólidas, líquidas acuosas y alternativas, junto con la actualización de listados técnicos respectivos.
15º. Que, por lo antes expuesto, dicto el siguiente:
Decreto:
Artículo primero.- Modifícase el decreto exento Nº 500, de 1 de junio de 2012, del Ministerio de Salud, que aprueba la Norma Técnica Nº 136, nominada "Norma que determina los principios activos contenidos en los productos farmacéuticos que deben demostrar su equivalencia terapéutica y lista de productos farmacéuticos que sirven de referencia de los mismos", en la forma que se indica a continuación:
a) Otórguese plazo hasta el 30 de septiembre de 2027, para cumplir con la exigencia de presentación de estudios de Equivalencia Terapéutica ante el Instituto de Salud Pública de Chile, para los productos farmacéuticos registrados que contengan los "Principios Activos" o "Asociaciones" y bajo la "Forma de Liberación", que a continuación se indican:
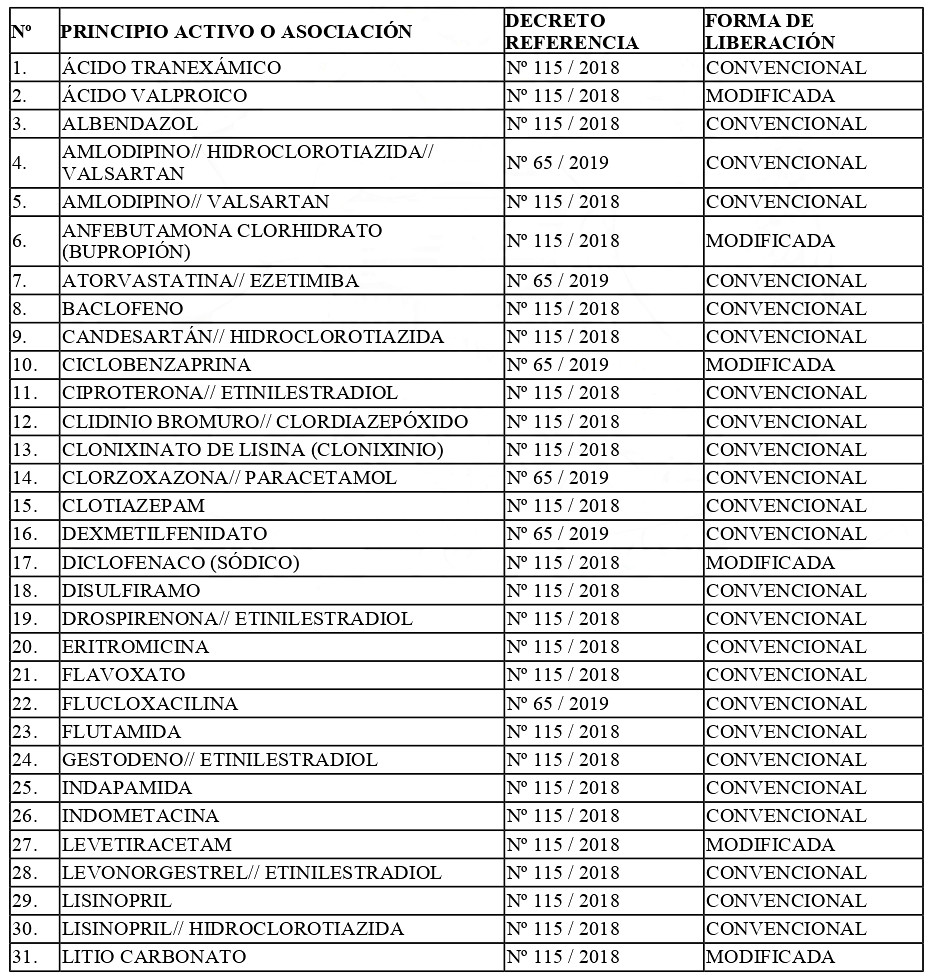
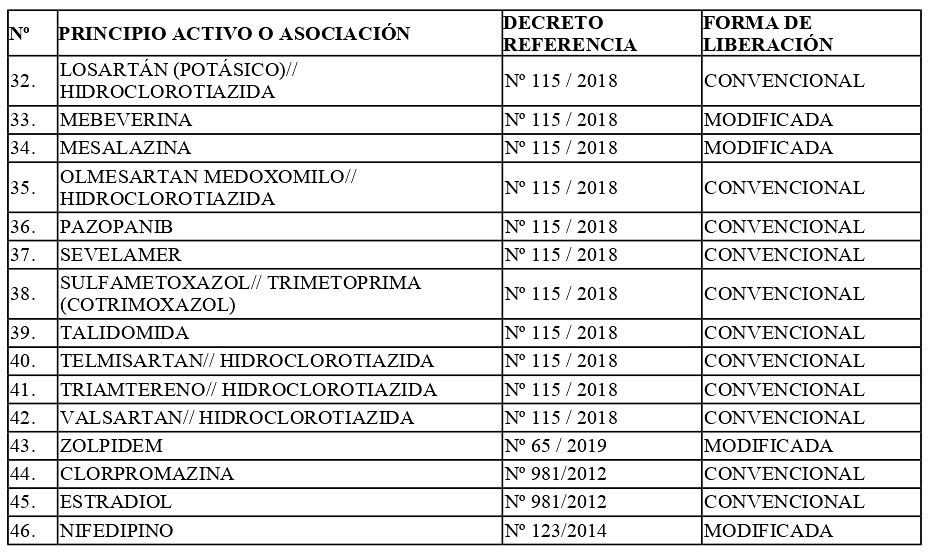
b) Sustitúyase, el inciso segundo del artículo quinto, por el siguiente:
"Otórgase plazo hasta el 30 de septiembre de 2027, para que a todo titular de registro sanitario de un producto farmacéutico que reúna alguna de las características descritas en el Punto 4.2. de la Norma Técnica Nº 131, "Norma que define los criterios destinados a establecer la equivalencia terapéutica en productos farmacéuticos en Chile", aprobada mediante el decreto exento Nº 27, de fecha 18 de enero de 2012, del Ministerio de Salud, presente ante el Instituto de Salud Pública de Chile los antecedentes para demostrar su equivalencia terapéutica. El mismo plazo señalado precedentemente aplicará para productos farmacéuticos registrados por los principios activos o sus asociaciones que se indican en el listado incorporado más abajo, que deban cumplir con la señalada demostración y se presenten como formulaciones masticables, bucodispersables, dispersables, láminas bucodispersables o cualquier otra forma farmacéutica de administración oral, que difiera de aquella en la que se presenta el respectivo producto de referencia establecido para la realización de los estudios de equivalencia terapéutica.

Artículo segundo.- Modifícase el decreto exento Nº 27, de 18 de enero de 2012, del Ministerio de Salud, que aprueba la Norma Técnica Nº 131 nominada "Norma que define los criterios destinados a establecer la equivalencia terapéutica en productos farmacéuticos en Chile", en la forma que se indica continuación:
a) Agrégase al numeral 7º: "LISTA DE PRINCIPIOS ACTIVOS NO NUEVOS (MADUROS) DE LARGA EXPERIENCIA DE USO", los siguientes "principios activos o asociaciones" y "forma farmacéutica sólida, administración oral tipo de liberación", cuyo detalle se indica a continuación:

b) Incorpórase a la "Lista de Productos de Referencia para los Estudios de Equivalencia Terapéutica", los siguientes productos de referencia:
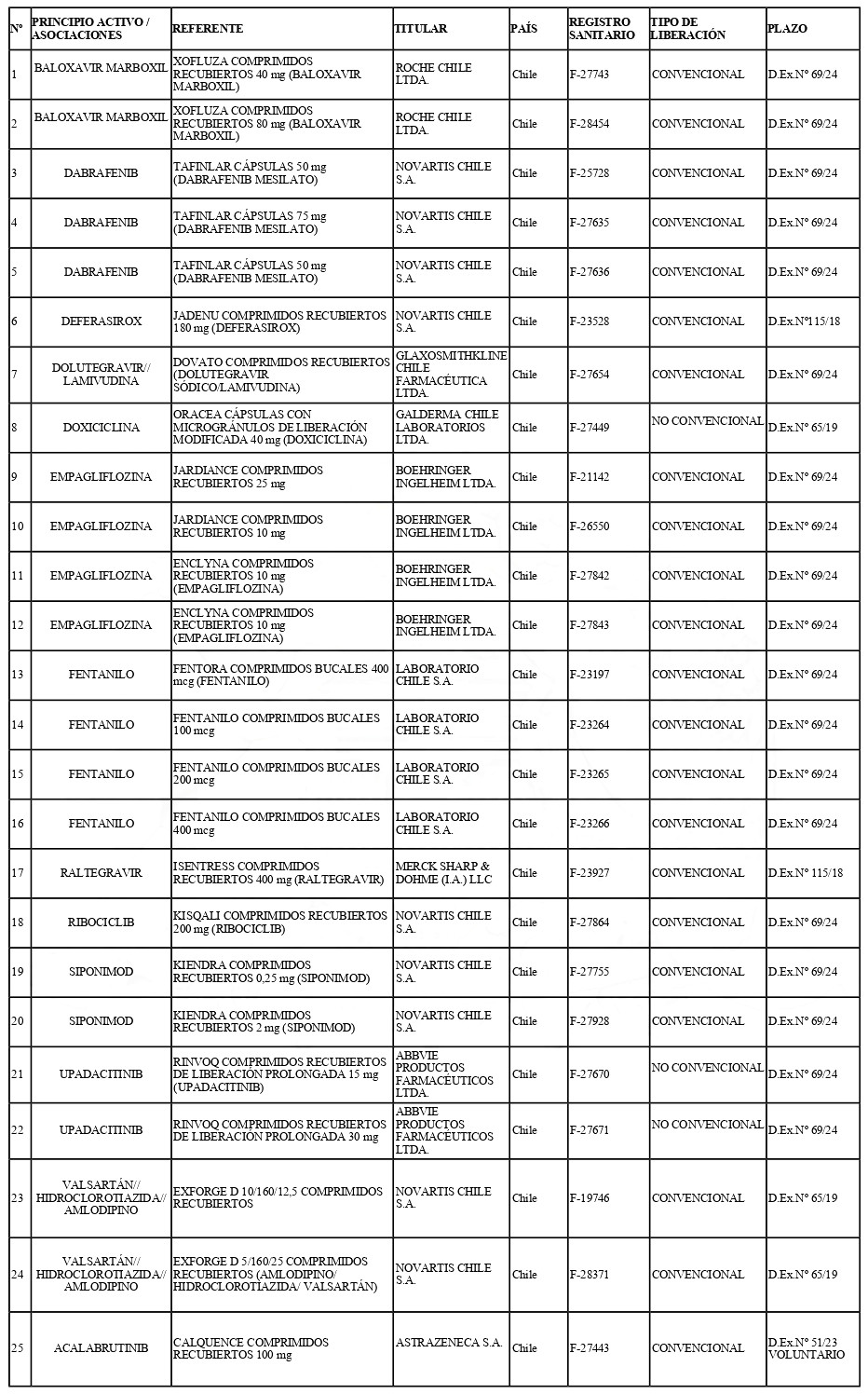
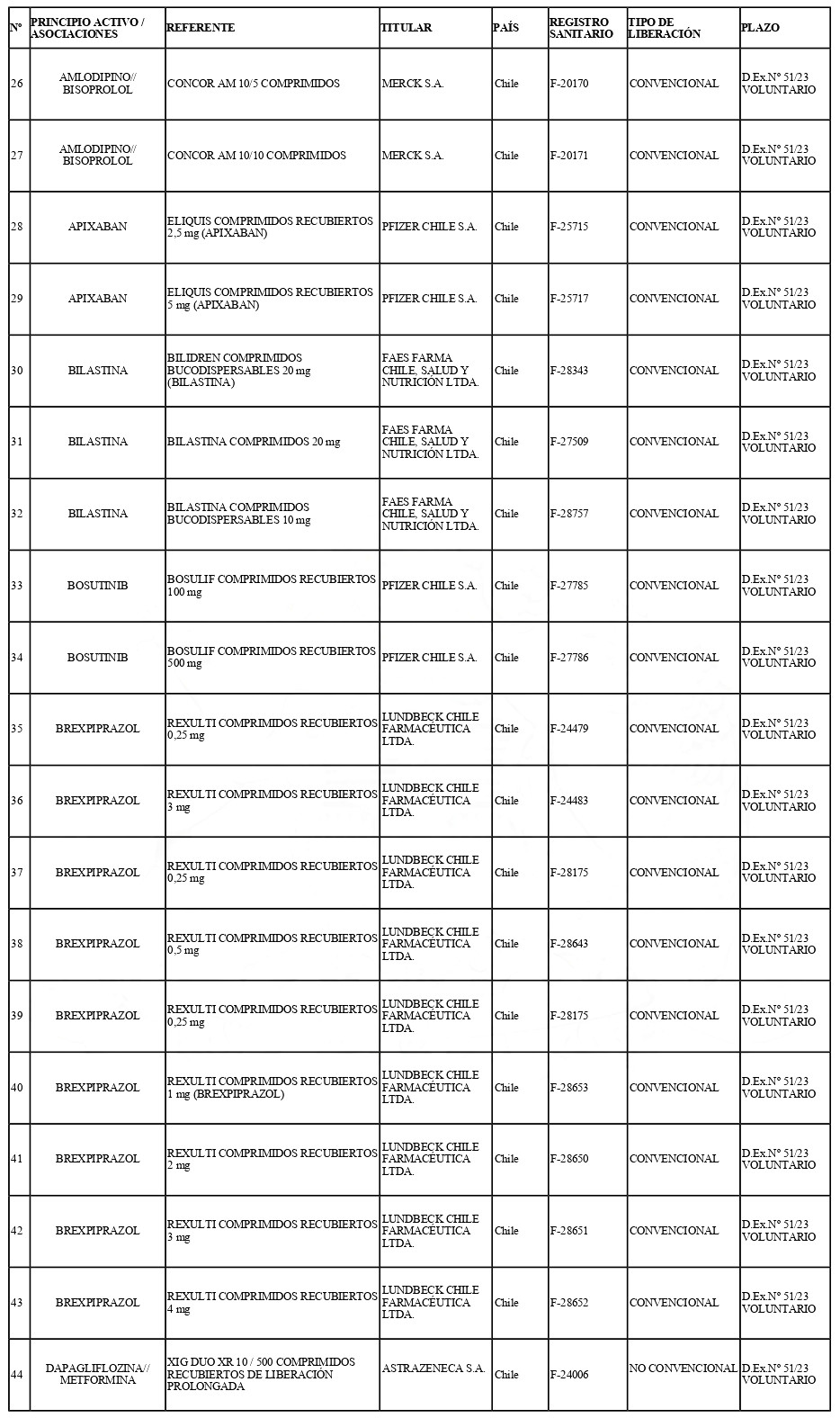
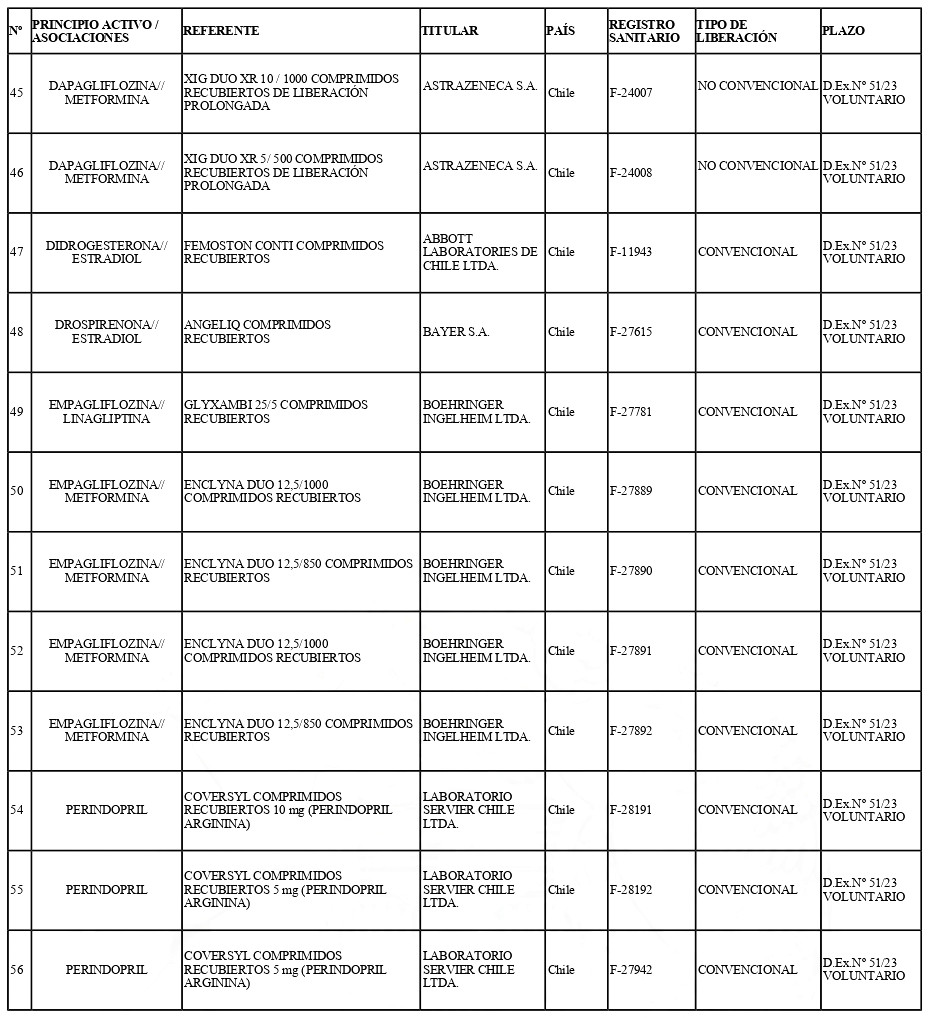
Artículo tercero.- El texto actualizado de las Normas Técnicas Nº 131 y Nº 136, conteniendo las modificaciones que se aprueban en este decreto y las anteriores realizadas, se mantendrá en el Departamento de Políticas y Regulaciones Farmacéuticas. De Prestadores de Salud y de Medicinas Complementarias de la División de Políticas Públicas Saludables y Promoción de la Subsecretaría de Salud Pública, entidad que a su vez deberá velar por su oportuna publicación en la página web del Ministerio de Salud, www.minsal.cl, para su adecuado conocimiento y difusión, debiendo además asegurar que las copias y reproducciones que se emitan guarden estricta concordancia con el texto aprobado.
Artículo cuarto.- Déjase constancia que las disposiciones contenidas en el presente acto administrativo regirán desde la fecha de su publicación en el Diario Oficial.
Anótese, comuníquese y publíquese.- Por orden del Presidente de la República, Ximena Aguilera Sanhueza, Ministra de Salud.
Transcribo para su conocimiento decreto exento Nº 48, 26 de septiembre 2025.- Por orden de la Subsecretaría de Salud Pública.- Saluda atentamente a Ud., Yasmina Viera Bernal, Jefa de la División Jurídica, Ministerio de Salud.