APRUEBA PLAN DE RECUPERACIÓN, CONSERVACIÓN Y GESTIÓN DEL HUILLÍN (LONTRA PROVOCAX)
Núm. 36.- Santiago, 21 de octubre de 2024.
Vistos:
Lo dispuesto en los artículos 19 N° 8 y 32 N° 6, de la Constitución Política de la República; en los artículos 37, 70 letra i), 71 letra f) y 73 de la ley N° 19.300, sobre Bases Generales del Medio Ambiente; en la ley N° 21.600, que crea el Servicio de Biodiversidad y Áreas Protegidas y el Sistema Nacional de Áreas Protegidas; en el Convenio sobre Diversidad Biológica, promulgado como ley de la República mediante el decreto supremo N° 1.963, de 1994, del Ministerio de Relaciones Exteriores; en el decreto con fuerza de ley N° 1/19.653, de 2000, del Ministerio Secretaría General de la Presidencia, que fijó el texto refundido, coordinado y sistematizado de la ley N° 18.575, Orgánica Constitucional de Bases Generales de la Administración del Estado; en la ley N° 19.880, que Establece Bases de los Procedimientos Administrativos que Rigen los Actos de los Órganos de la Administración del Estado; en el decreto supremo Nº 1, de 2014, del Ministerio del Medio Ambiente, que aprueba el Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies; en el decreto supremo Nº 42, de 2011, del Ministerio del Medio Ambiente, que aprueba y oficializa el séptimo proceso de Clasificación de especies según estado de conservación; en carta de 29 de agosto de 2022, de Huella Natureza SpA; en la resolución exenta Nº 24, de 12 de enero del 2023, del Ministerio del Medio Ambiente, que inicia el procedimiento abreviado para la elaboración del Plan de Recuperación, Conservación y Gestión del Huillín (Lontra provocax); en el acuerdo N° 13/2024, del Consejo de Ministros para la Sustentabilidad y el Cambio Climático, adoptado el 5 de julio de 2024; en la resolución Nº 7, de 2019, de la Contraloría General de la República; y,
Considerando:
1. Que, conforme al artículo 19 N° 8 de la Constitución Política de la República, es deber del Estado tutelar la preservación de la naturaleza, así como velar por la protección y conservación de la diversidad biológica del país.
2. Que, conforme lo dispone el literal i) del artículo 70 de la ley N° 19.300, sobre Bases Generales del Medio Ambiente ("ley N° 19.300"), es atribución del Ministerio del Medio Ambiente proponer políticas y formular planes, programas y acciones que establezcan los criterios básicos y las medidas preventivas para favorecer la recuperación y la conservación de los recursos hídricos, genéticos, la flora, la fauna, los hábitats, los paisajes, ecosistemas y espacios naturales, en especial los frágiles y degradados, contribuyendo al cumplimiento de los convenios internacionales de conservación de la biodiversidad. Uno de dichos instrumentos son los planes de recuperación, conservación y gestión de especies, referidos en el artículo 37 de la ley N° 19.300.
3. Que, el artículo 144 de la ley N° 21.600, que crea el Servicio de Biodiversidad y Áreas Protegidas ("SBAP") y crea el Sistema Nacional de Áreas Protegidas ("ley N° 21.600"), modificó el artículo 37 de la ley N° 19.300, en orden a señalar que el mencionado Servicio deberá aprobar planes de recuperación, conservación y gestión de especies ("Planes RECOGE"), de acuerdo con lo dispuesto en la referida ley.
4. Que, previo a la modificación indicada en el considerando precedente, el artículo 37 de la ley N° 19.300 atribuía la competencia para aprobar los Planes RECOGE al Ministerio del Medio Ambiente.
5. Que el artículo primero transitorio de la ley N° 21.600, dispuso que será un decreto con fuerza de ley, que deberá ser dictado dentro del plazo de un año de publicada la Ley, el que establecerá la fecha en que el SBAP entrará en funcionamiento.
6. Que, el decreto con fuerza de ley N° 1, de 2024, del Ministerio del Medio Ambiente estableció en su artículo 3° que la entrada en funcionamiento del SBAP contemplará un período para su implementación, y otro de entrada en operaciones, añadiendo que el período de implementación se extenderá desde la publicación del referido decreto con fuerza de ley N° 1 en el Diario Oficial; hecho que sucedió el 09 de marzo de 2024, y hasta el día anterior a la fecha de su entrada en operaciones propiamente tal.
7. Que, atendido a que el SBAP se encuentra en un período de implementación, en la elaboración y aprobación de los Planes RECOGE se debe seguir el principio de continuidad de la función pública, establecido en los artículos 3° y 28 de la ley N° 18.575, en virtud del cual los órganos de la Administración tienen por finalidad promover el bien común atendiendo las necesidades públicas en forma continua y permanente, por lo que la potestad para aprobar los Planes RECOGE, se mantiene en el Ministerio del Medio Ambiente, hasta la entrada en operaciones del SBAP (aplica criterio adoptado por la Contraloría General de la República, entre otros en su Dictamen N° 26190, de 2012).
8. Que, el decreto supremo N° 1, de 2014, del Ministerio del Medio Ambiente, que aprueba el Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies, define los Planes RECOGE como un instrumento administrativo que contiene el conjunto de acciones, medidas y procedimientos que deberán ejecutarse para recuperar, conservar y manejar especies que hubiesen sido clasificadas de acuerdo con el artículo 37 de la ley N° 19.300.
9. Que, en el mismo sentido, la ley N° 21.600, define plan de manejo como "instrumento de gestión ambiental basado en la mejor evidencia posible, que establece metas, principios, objetivos, criterios, medidas, plazos y responsabilidades para la gestión adaptativa de la biodiversidad", y Planes de recuperación, conservación y gestión de especies como aquel plan de manejo "destinado a mejorar el estado de conservación de una o más especies clasificadas de conformidad a lo establecido en el artículo 37 de la ley N° 19.300".
10. Que, a través del decreto supremo N° 42, de 2011, del Ministerio del Medio Ambiente, que oficializó el séptimo proceso de Clasificación de Especies según su Estado de Conservación, se clasificó al Huillín como En Peligro (EN).
11. Que, el Huillín se encuentra en el referido estado de conservación por la pérdida y fragmentación de su hábitat derivada de remoción de la vegetación ribereña y canalización de cursos de agua, entre otros; la presencia de visón y de perros de vida libre, especies exóticas invasoras; interacción con acuicultura; y la caza ilegal histórica a que fue sometido.
12. Que, siguiendo lo establecido en el artículo 21 del decreto supremo Nº 1, de 2014, del Ministerio de Medio Ambiente, que aprueba el Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies, a través de resolución exenta Nº 24, de 12 de enero de 2023, del Ministerio del Medio Ambiente, se dio inicio al procedimiento abreviado para la elaboración del Plan de Recuperación, Conservación y Gestión del Huillín (Lontra provocax).
13. Que, en conformidad con lo establecido en el literal f) del artículo 71, de la ley N° 19.300, y en artículo 19 del decreto supremo Nº 1, de 2014, del Ministerio de Medio Ambiente, el Consejo de Ministros para la Sustentabilidad y el Cambio Climático, en sesión ordinaria de 5 de julio de 2024, adoptó por unanimidad el acuerdo N° 13/2024, de proponer a S.E. el Presidente de la República, el Plan de Recuperación, Conservación y Gestión del Huillín (Lontra provocax).
Decreto:
Artículo único.- Apruébase el siguiente Plan de Recuperación, Conservación y Gestión del Huillín (Lontra provocax):
PLAN DE RECUPERACIÓN, CONSERVACIÓN Y GESTIÓN DEL HUILLÍN (Lontra provocax)
1. Introducción
Los Planes de Recuperación, Conservación y Gestión de Especies (RECOGE) son un instrumento, cuyo procedimiento de elaboración es administrado por el Ministerio del Medio Ambiente, hasta la entrada en pleno funcionamiento del Servicio de Biodiversidad y Áreas Protegidas, (ley Nº 19.300), que contienen el conjunto de metas, objetivos y acciones que deberán ejecutarse para recuperar, conservar y manejar una o más especies que hayan sido clasificadas en el marco del Reglamento para la Clasificación de Especies Silvestres según Estado de Conservación.
Asimismo, la propuesta da cumplimiento a lo señalado en el artículo 43 de la ley N° 21.600, que crea el Servicio de Biodiversidad y Áreas Protegidas, norma que establece los contenidos mínimos que debe poseer un plan RECOGE.
Los Planes RECOGE forman parte de una batería de instrumentos de gestión de la política pública para la conservación de la biodiversidad del país, mencionados tanto en la ley N° 19.300, de Bases Generales sobre el Medio Ambiente, como en ley N° 21.600.
El objetivo principal de estos planes RECOGE es mejorar el estado de conservación de las especies nativas de Chile, así como también mejorar la coordinación de los distintos Órganos de la Administración del Estado para lograr una gestión eficaz en la conservación de especies nativas, e involucrar al sector privado y a la sociedad civil en la conservación de la biodiversidad, todo lo cual contribuye al desarrollo sustentable de nuestro país (decreto supremo Nº1, de 2014, del Ministerio del Medio Ambiente), dar cumplimiento de la Estrategia Nacional de Biodiversidad 2017-2030 (MMA 2017) en su ámbito temático de Conservación de Especies Nativas, y, en este caso particular, la Estrategia Global de Conservación de Nutrias (UICN 2018).
El presente documento corresponde a la propuesta de Plan RECOGE del huillín (Lontra provocax), especie que se encuentra catalogada En Peligro (EN) por el DS N°42/2011 del Ministerio del Medio Ambiente (MMA) en el marco del Reglamento de Clasificación de Especies y por la Unión Internacional para la Conservación de la Naturaleza -UICN- (Sepúlveda et al. 2015). Esta propuesta se presenta para ser formalizada de acuerdo con el artículo 21 del Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies (DS N°1/2014 del Ministerio del Medio Ambiente).
2. Presentación del Plan de Recuperación, Conservación y Gestión del Huillín (Lontra provocax)
El huillín (Lontra provocax) también conocido como nutria de río, lobito de río patagónico, gato del agua, aúilaf (en yámana) ó yem'chen (aonikenk) (Iriarte & Jaksic 2012), es una de las dos nutrias que habitan en Chile en conjunto con el chungungo (Lontra felina). Es una especie que ha sufrido una reducción drástica en sus poblaciones originales, debido principalmente a la caza ilegal (histórica) y a la destrucción de su hábitat (Sielfeld & Castilla 1999). Su distribución actual es disjunta y se presenta en ambientes de agua dulce y marinos. Las poblaciones de ambientes dulceacuícolas se distribuyen, actualmente, de forma aislada y restringida desde el río Imperial (38°S) hacia el sur de Chile (Rodríguez-Jorquera & Sepúlveda 2011). Las subpoblaciones en ambientes costero-marinos se encuentran en la costa del Pacífico, desde los 46°S hasta Tierra del Fuego (Sepúlveda et al. 2015).
Es así como en un contexto general, las poblaciones de esta especie, desde la Región de la Araucanía hacia el sur de Chile, se han visto influenciada por una rápida y drástica transformación del paisaje, debido al reemplazo de bosques y otras áreas naturales a plantaciones exóticas, agricultura y ganadería (Armesto et al. 1998, Echeverría et al. 2006). Además, la construcción de represas, modificación de los cauces, contaminación, acuicultura e introducción de especies invasoras, han hecho cambiar las comunidades ecológicas de agua dulce en Chile y el mundo (Hauenstein et al., 2005). Según distintos autores (Medina 1996, Medina-Vogel et al. 2003, Sepúlveda et al. 2009) el factor que lidera la disminución de la distribución de la especie es la degradación de su hábitat, dado por las transformaciones del paisaje antes señaladas. Y al ser la especie huillín una especie sensible a impactos antrópicos (Sepúlveda et al. 2009), esto se ha traducido en una reducción de sus poblaciones en el pasado y una proyección de reducción de sus poblaciones en el futuro, llevándola a que sea susceptible a extinciones locales.
En ambientes dulceacuícolas la conservación del huillín es un gran desafío por dos razones principales (Sepúlveda et al. 2009): (1) tienen un gran ámbito de hogar y bajas densidades de población, siendo muy susceptibles a la perturbación humana (Woodroffe & Ginsberg 1998-2000; Cardillo et al. 2004), y (2) es una especie que depende de ecosistemas de agua dulce, los que están muy amenazados por acciones humanas a nivel local y regional (Barbosa et al. 2003, Suski & Cooke 2007). En el caso del sistema marino, hasta el año 2015 la salmonicultura era considerada una amenaza potencial (Sepúlveda et al. 2015), actividad que es intensiva y de éxito económico en el país (Bruschman & Fortt 2005).
Es así como la definición de especies indicadoras de salud ecológica, conocida como aquellas especies que se encuentran altamente relacionadas con condiciones ambientales particulares, por sus características de sensibilidad a perturbaciones o contaminantes, alterando su distribución, abundancia, dispersión, éxito reproductivo, entre otras, pueden ser utilizadas como estimadoras de los atributos o estatus de otras especies o condiciones ambientales (Caro & O'Doherty 1999, Fleishman et al. 2001), pudiendo considerarse la especie huillín una de estas. Además, el huillín ha sido considerado como una especie "paraguas" (Medina & Chehébar 2000, Cassini & Sepúlveda, 2006). Realizar acciones de conservación para el huillín implicaría la conservación de los ambientes donde habita y áreas adyacentes, ya que requiere de una oferta adecuada de peces, crustáceos y otras presas, riberas con vegetación en donde encontrar refugio y un ambiente libre de contaminación (Medina & Chehébar 2000).
La historia de protección de ecosistemas en Chile ha concentrado los esfuerzos en ecosistemas terrestres, siendo la conservación de ecosistemas acuáticos incipiente (Faúndez 2020), existiendo así un sesgo relacionado a la representatividad de los ecosistemas, ya que aún existen algunos sin o muy baja representación (Pliscoff & Fuentes-Castillo 2011).
Conforme a los antecedentes anteriores, que describen una especie con problemas de conservación, escenarios globales de amenaza a la biodiversidad y vacíos en protección de ecosistemas es que resulta prioritario generar una propuesta del Plan de Recuperación, Conservación y Gestión (RECOGE) de la especie huillín con la finalidad de generar una estructura de plan con lineamientos y acciones clave, que permitan en un periodo de tiempo determinado alcanzar una mejora en el estado de conservación de la especie huillín.
La elaboración del Plan de RECOGE del Huillín fue conducido por la Consultora Huella Natureza, con el apoyo de The Pew Charitable Trust, considerando la participación de una serie de actores clave, tanto público como privados, a través de 14 talleres del Grupo de Elaboración, 12 talleres territoriales, dos talleres binacionales y tres reuniones bilaterales con organismos públicos y privados. La metodología utilizada para obtener la información del plan fue Estándares Abiertos para la Práctica de la Conservación (CMP 2013).
3. Antecedentes generales del Huillín
3.1 Descripción de la especie
El huillín (Lontra provocax) comúnmente llamado "nutria de río", es endémica de la región patagónica de Chile y una pequeña porción de Argentina (Larivière 1999a). El huillín pertenece al orden Carnivora, siendo el representante más grande de la familia Mustelidae en Chile. El adulto se caracteriza por poseer cuerpo alargado y patas cortas con cinco dedos con garras, su cabeza es aplanada y posee un pelaje aterciopelado café oscuro en la parte superior y más blanquecina en la zona ventral, el cual puede ser corto o largo. Una característica distintiva de esta nutria es su rinario o nariz, el cual es de forma estrellada y no presenta pelaje (Larivière 1999). La nutria de río mide entre 1,1 y 1,3 metros de longitud incluyendo su cola (38 a 45 cm), su peso varía entre los 6 a 15 Kilogramos (Medina et al. 2004). Las manos y pies poseen membranas interdigitales que le ayudan durante el nado (Quintana et al. 2009).
La dieta del huillín varía según su disponibilidad y zona geográfica, siendo así que las poblaciones que habitan agua dulce consumen principalmente crustáceos de los géneros Aegla y Samastacus (Chehébar et al. 1986, Medina 1998, Sepúlveda et al. 2009) y de forma secundaria peces (peces nativos, salmonideos y pejerrey), la lamprea austral (Geotria australis), anfibios como la rana chilena (Calyptocephalella gayi) y aves (Chehébar 1985, Medina 1997, Medina 1998, Medina-Vogel 2001, Medina-Vogel & González-Lagos 2008). Mientras tanto en los canales australes su alimentación consiste en 70% de peces y un 30% de crustáceos. Peces costeros de los géneros Harpagifer, Patagonotothen, Eleginops, Cottopoerca y crustáceos de los géneros Munida, Taliepus, Cancridae, Gañatheidae, Lithodidae, Lithoides, Paralois y Campylonotus (Sielfeld & Castilla 1999). En cuanto a Magallanes, basándose en el análisis fecal, los ítems más importantes en la dieta del huillín son los peces, crustáceos y aves. A estos deben agregarse algunos invertebrados que no aparecen en las fecas y que son detectados en el análisis de restos alimentarios de madrigueras, como moluscos y equinodermos (PCN Huillín, 2009).
Las heces de huillín son cilíndricas con subdivisiones o amorfas, donde generalmente se evidencia la presencia de restos de crustáceos, espinas de peces y en escasas ocasiones huesos de algún pequeño mamífero, a veces están rodeadas de un líquido viscoso oscuro. Miden hasta 3 cm de diámetro y 11 cm de largo, generalmente disgregadas y fáciles de reconocer, de color rojo, café o blanco con un olor almizclado, dulzón y peculiar (Muñoz-Pedreros 2008).
L. provocax es una especie solitaria, excepto madres con sus crías o en el periodo reproductivo en el que se puede observar en parejas. La ubicación de las áreas de mayor actividad dentro del ámbito de hogar parece estar asociada al menos con presencia de madriguera o sitios de descanso (Sepúlveda et al. 2007). En el caso de ambiente dulceacuícola, su área mínima para una unidad reproductora es más de 25 km lineales de riberas de arroyos (SERNAPESCA 2005), siendo la ubicación adecuada, para esta unidad, un factor limitante (Beja 1996, Kruuk 1995). Por lo tanto, la protección de las guaridas existentes parece ser un componente crucial para la conservación efectiva del hábitat (Sepúlveda et al. 2007).
El apareamiento del huillín se produce en invierno y las pariciones en primavera, en madrigueras con entradas camufladas. Se han registrado madres con hasta tres crías desde octubre a enero, incluso hasta febrero según algunos autores. Las crías comienzan a nadar a los 3 meses de edad, donde por lo general son capaces de capturar sus propios alimentos a los 4 meses. Los individuos juveniles solitarios se presentan desde febrero a mayo. Los jóvenes siguen siendo parte del grupo familiar durante el primer año antes de dispersarse. La madurez reproductiva se alcanza en el segundo o tercer año de vida. Una elevada proporción de los individuos muere antes de alcanzar dicha madurez. Sólo alrededor del 1% logra sobrevivir hasta los 6-10 años de edad (PCN Huillín 2009).
3.2 Descripción del hábitat y distribución territorial del huillín
Esta especie habita ríos, esteros, lagos, estuarios, canales y litoral marino rocoso. En medios dulceacuícolas se ubica en sectores lacustres o ríos con vegetación ribereña densa, con abundantes árboles y grandes raíces, así como denso sotobosque con presencia de quila (Chusquea quila) (Sepúlveda et al. 2007, Medina-Vogel et al. 2004) lo que le permite el acceso imperceptible al agua y adecuado refugio (Choupay 2006).
En cuanto a su hábitat costero marino, se asocia a vegetación terrestre compuesta de canelo (Drymis winteri), dura (Maytenus magellanicus) y coihue (Nothofagus betuloides) (Sielfeld 1990). Al sur del Golfo de Corcovado y en los archipiélagos magallánicos, la especie utiliza ambiente marino, prefiriendo en zonas litorales rocosas del tipo paredón o bloques protegidos y no expuestos al Océano Pacífico, en sectores con abundante vegetación ribereña (canelo, dura y coihue), lo que, junto con una menor perturbación antrópica, serían características que favorecerían el establecimiento de madrigueras (Chehébar et al. 1986, Medina 1996a, 1996b, Sielfeld 1983).
Las madrigueras del huillín pueden estar al interior de grietas profundas en grandes rocas, entre raíces y rocas (ríos preandinos y andinos), o excavadas en las riberas con entradas sumergidas durante la época de las crecidas (ríos de la Cordillera de la Costa y Depresión Intermedia). Las madrigueras también se encuentran bajo arbustos y raíces entre los brazos de ríos al interior de bosques inundados o hualves; y se han encontrado distantes hasta 50 m del cuerpo de agua (Medina 1991, Medina 1996), entre 3 a 8 m sobre el nivel del agua (Chehébar 1986). Su ámbito de hogar de la especie puede ser muy amplio, con individuos que pueden recorrer desde 0,9 hasta 11,3 km en un solo día (Sepúlveda et al. 2007).
En ambientes marinos tienen sus madrigueras entre el roquerío costero. Al igual que en ambiente dulceacuícola, desarrollan actividad crepuscular y nocturna, utilizando el día para descanso y traslado. El comportamiento nocturno sugiere una relación con los hábitos de los crustáceos del género Aegla (PCN Huillín 2009).
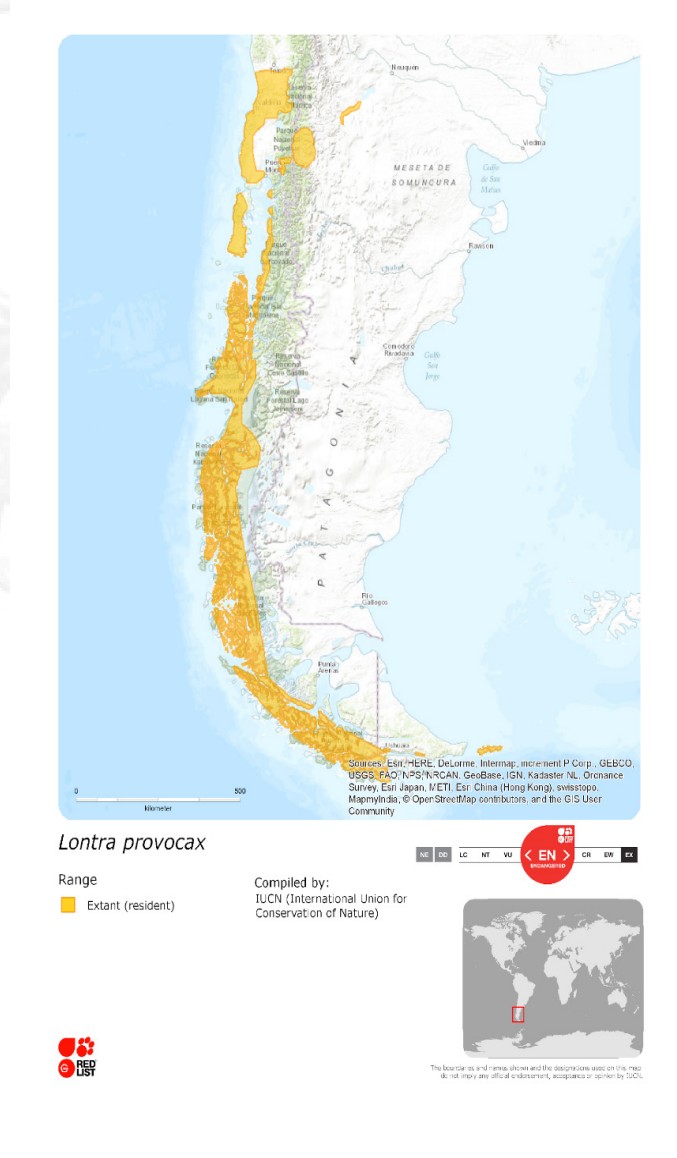
Su distribución actual en Chile va desde el río Imperial en la Región de la Araucanía, hasta el extremo sur de Tierra del Fuego en Chile y Argentina, 54ºS en la Región de Magallanes (Sepúlveda et al. 2007) (Figura 1). En el pasado, su distribución norte comprendía desde el río Cachapoal 34ºS en la Región de O'Higgins, por lo que la especie en ambientes de agua dulce ha sufrido una reducción drástica de sus poblaciones a menos del 10% de su distribución original, considerándose hoy la nutria con probablemente menor distribución en el mundo (Medina 1996). Se distribuye en forma heterogénea, en asociación con las presas y con ambientes con refugios, ya sean densos en raíces o rocas (Sielfeld & Castilla 1999). En Argentina está presente a lo largo de Los Andes desde la parte sur de la provincia de Neuquén hasta Tierra del Fuego (Cabrera 1961, Redford & Eisenberg 1992); se encuentra en el Parque Nacional Lanín (Neuquén), donde sólo subsistirían dos poblaciones en la zona sur y en los Parques Nacionales Nahuel Huapi (Neuquén y Río Negro), Los Arrayanes (Neuquén) y Parque Nacional Lanín hasta Tierra del Fuego (PN Huillín 2009), (posiblemente formando un continuo con la población aledaña que se encuentra en Chile) y, por último, en la Isla de los Estados (Massoia & Chébez 1993). En Argentina, actualmente, la distribución de agua dulce, esta principalmente restringido a la cuenca hidrográfica del río Limay, en el Parque Nacional Nahuel Huapi (Chehébar 1985, Cassini et al. 2010, Valenzuela et al. 2012). Los mapas en Figura 1 y 2 (Anexo 8), muestran sitios donde se ha registrado la presencia de huillín y fueron construidos durante el proceso de elaboración del Plan, de acuerdo a la información obtenida y recabada de las diferentes instancias participativas de los actores clave en los talleres desarrollados.
En Chile se cuenta con registros de la especie en al menos las siguientes áreas protegidas: Santuario de la Naturaleza (SN) Río Cruces, SN Río Maullín, Parque Nacional (PN) Vicente Pérez Rosales, SN Humedales de la Cuenca de Chepu, PN Chiloé, PN Pumalín Douglas Tompkins, PN Corcovado, PN Isla Magdalena, PN Laguna San Rafael, Área Marina Costera Protegida (AMCP) Tortel, PN Bernardo O'Higgins, PN Kawésqar, Parque Marino Francisco Coloane, AMCP Francisco Coloane, PN Alberto de Agostini y AMCP Seno Almirantazgo.
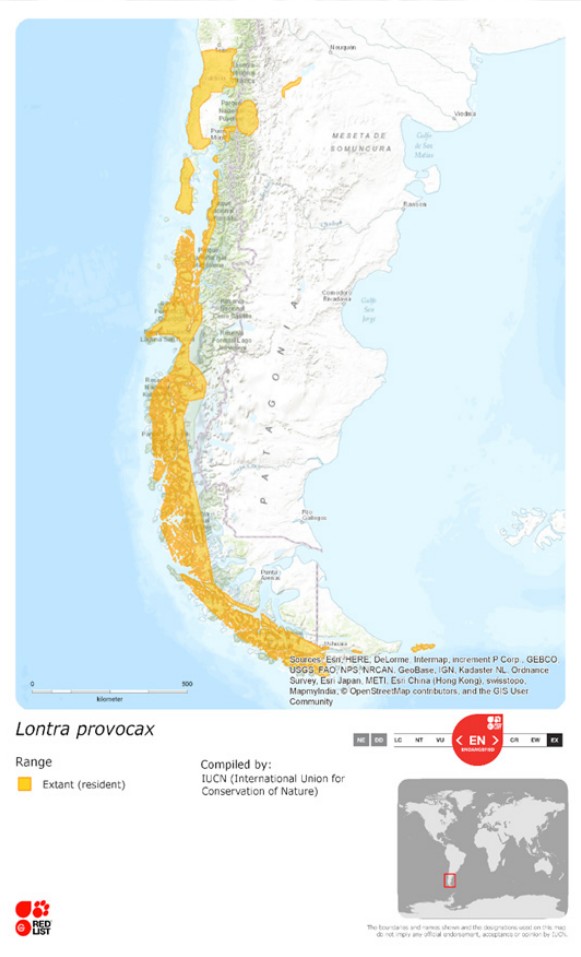
Figura 1. Mapa de distribución de la especie huillín según la The IUCN Red List of Threatened Species. Fuente: Sepúlveda et al. 2015.
3.3 Estado de conservación de la especie según clasificación internacional y nacional
La clasificación histórica del Estado de Conservación del huillín se describe en una primera instancia en el Libro Rojo de la Fauna Terrestre de Chile (Glade, 1993), asignándosele la categoría de En Peligro de Extinción.
Actualmente, en Chile se encuentra clasificada en estado de conservación "En Peligro" (decreto supremo N° 42, de 2011, del Ministerio del Medio Ambiente). Asimismo, esta especie mantiene su clasificación en esta misma categoría por la UICN desde el año 2000, sumándose como parte de las especies clasificadas en el apéndice I de la Convención sobre el Comercio Internacional de Especies Amenazadas de Fauna y Flora Silvestres (Sepúlveda et al. 2015).
Este grado de amenaza se debe a que la población podría alcanzar una reducción mayor o igual al 50% en los próximos 30 años, correspondientes a tres generaciones de la especie; por destrucción y degradación de hábitat en las subpoblaciones de agua fresca, y por actividades pesqueras en las subpoblaciones de ambientes marinos. Esto debido a la reducción de la calidad del hábitat por remoción de vegetación, canalización de cursos de agua, el dragado extensivo, depredación por perros domésticos y uso intensivo para actividades de pesca, sumado a la perturbación por ganado y prácticas de caza ilegal (Medina 1996a, Medina-Vogel et al. 2004, Chehébar et al. 1986, Housse 1953, Medina 1996a, 1996b, Porro & Chehébar 1995). Chehébar (1985). A lo anterior se suma el hecho que actualmente más del 90% de las poblaciones de huillín en ambientes de agua dulce en Chile están fuera de las áreas protegidas del Estado (Medina-Vogel 2004, Medina-Vogel et al. 2007).
La probable extinción del huillín estaría claramente asociada a la pérdida de la vegetación ripariana, y el drenaje, canalización y rectificación de los cursos de agua por obras de ingeniería (Medina et al. 2003, Sepúlveda et al. 2009), y especialmente la pérdida de los bosques inundados o pantanoso (hualve) y humedales costeros, ya sea por su eliminación, o sustitución por vegetación exótica (Medina & González 2007, Sepúlveda et al. 2009).
3.4 Estado de las poblaciones de huillín
La evaluación del estado de las poblaciones de huillín para el presente plan se realizó a través de un Análisis de Viabilidad que consiste en determinar, de acuerdo a la mejor información disponible, el estado actual de la especie.
En esta etapa del plan, identificó solo "Sitios de ocupación (presencia/ausencia)" como atributo ecológico clave, que fue evaluado de manera diferenciada por cada ambiente (Tabla 2). Dado que la información es insuficiente para determinar rangos cuantitativos para establecer el estado en que se encuentran las poblaciones, se realizó una evaluación simple determinando 4 rangos cualitativos de la condición de cada población, pobre, regular, buena o muy buena, en base a los antecedentes recopilados y la opinión de expertos.
Tabla 2. Estado de las poblaciones de huillín según Atributo Ecológico Clave
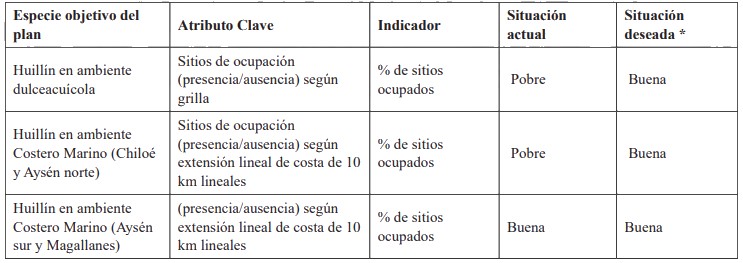
* Se considera alcanzar la situación deseada en el largo plazo, es decir más allá del tiempo definido para Plan RECOGE (15 años).
Los datos de ocupación serán levantados una vez se implemente la acción de monitoreo considerada en el plan.
4. Diagnóstico e identificación de amenazas y sus efectos sobre el Huillín
En este plan se utiliza la definición de amenaza según la metodología de estándares abiertos para la práctica de la conservación que establece que son: "... actividades humanas que degradan de forma inmediata los objetos de conservación (por ejemplo: pesca y cacería no sostenible, perforaciones petroleras, construcción de carreteras, aguas residuales industriales o la introducción de especies exóticas invasoras), pero también pueden ser fenómenos naturales alterados por la actividad humana (por ejemplo: aumento en el número de tormentas extremas o evaporación aumentada debido a los efectos del cambio climático) o en casos inusuales, fenómenos naturales cuyo impacto aumenta por causa de otras actividades humanas (por ejemplo: un potencial tsunami que amenaza las últimas poblaciones del rinoceronte asiático)" (CMP 2013).
La identificación de amenazas se realizó en talleres diferenciados por ambiente. Esta diferenciación fue fundamental para establecer las actividades que producen impactos negativos sobre el huillín, especialmente la individualización de los factores que contribuyen a la presentación de cada amenaza. De esta forma, independientemente de que en ambos ambientes se identifican actividades similares que amenazan al huillín, las causas que contribuyen a que estas amenazas se presenten pueden ser diferentes. También se identificaron actividades que solo se presentaron en uno de los ambientes. De esta manera, durante los talleres se realizó un trabajo participativo a través de mapas para visualizar los alcances de cada una de las amenazas diferenciado además por ambiente.
4.1 Calificación y priorización de amenaza (Ranking de amenazas)
Junto con identificar las amenazas, estas se priorizaron de acuerdo a los niveles de alcance, severidad e irreversibilidad según la metodología de Estándares Abiertos para la Conservación. Este análisis se realizó por separado por ambiente lo que permitió establecer las actividades con mayor impacto negativo en cada caso.
La definición de los criterios para la priorización de amenazas se describe a continuación (FOS 2009):
. Alcance: Proporción del objeto de conservación (huillín) que se puede esperar razonablemente que se vea afectada por la amenaza en los próximos diez años dada la continuación de las circunstancias y tendencias actuales. Se mide como la proporción de la población del objeto de conservación.
. Severidad: Dentro del alcance, la severidad es el nivel de daño al objeto de conservación a partir de la amenaza que cabe razonablemente esperar, dada la continuación de las circunstancias y tendencias actuales. Medido como el grado de reducción de la población del objeto de conservación dentro del alcance.
. Irreversibilidad: El grado en que los efectos de una amenaza pueden ser revertidos y el objeto de conservación afectado por la amenaza restaurado, si la amenaza deja de existir.
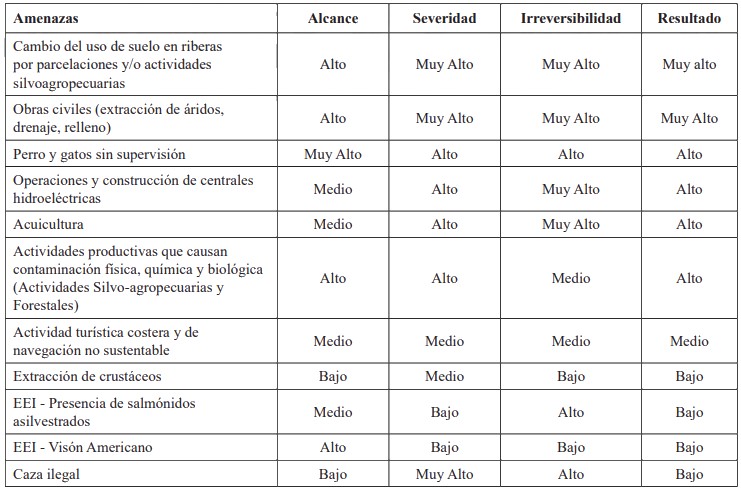
4.1.1. Amenazas en ambientes dulceacuícolas
El ambiente dulceacuícola corresponde al hábitat del huillín en cuerpo de agua de dulce y administrativamente se encuentran desde la Región de la Araucanía hasta la Región de Aysén.
4.1.2. Amenazas en ambientes costero marino
El ambiente costero marino corresponde al hábitat del huillín marino como costas, fiordos y canales, administrativamente se encuentran desde la Región de Los Lagos hasta la Región de Magallanes.
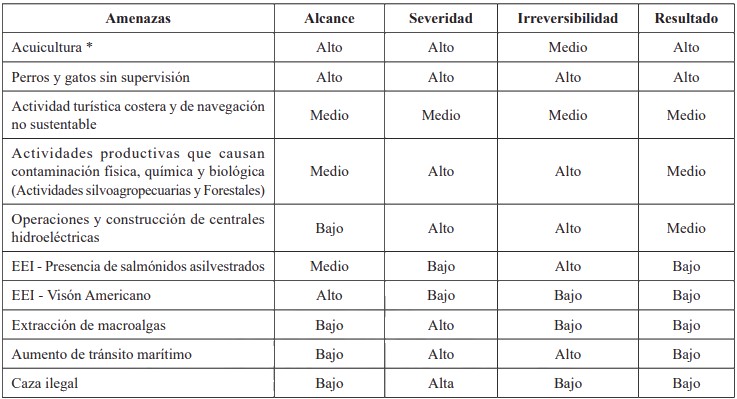
*Hay acuerdo en la falta de conocimiento y datos sobre los impactos de la acuicultura sobre el huillín y por tanto sobre la necesidad de desarrollar investigación al respecto.
La revisión y análisis de las amenazas permitieron identificar aquellas actividades que afectan a la especie en ambos tipos de ambientes y aquellas propias de cada uno, a las primeras se les denominó transversales.
4.2 Descripción de las amenazas
En este capítulo se describen las actividades que producen impactos negativos sobre el huillín. En una primera instancia se describen las amenazas que fueron identificadas en ambos ambientes, a lo que se llamó amenazas transversales. En cada una de ellas se mencionan antecedentes y se describe su presentación en el hábitat del huillín y cuando es necesario se señalan diferencias que existen entre ambientes. Posteriormente, se señalan las amenazas que solo se identificaron en uno de los ambientes de la especie.
4.2.2 Amenazas transversales en ambientes dulceacuícolas y costero marino
A. Acuicultura
La acuicultura en pisciculturas en tierra fue identificada como una amenaza potencial para el huillín, siendo mencionada por servicios de pesca durante los talleres debido a la existencia de evidencia observada o informada de interacción negativa para el huillín, realizadas durante las actividades de fiscalización. No obstante lo anterior, se sustenta en al menos el registro de un ejemplar muerto en el año 2018 producto de la interacción con en un centro, específicamente en bocatoma en una piscicultura (Melipeuco, Región de la Araucanía).
Cabe señalar que la evidencia formal de interacción se encuentra referida solo al proceso productivo en tierra por "atrapamiento e ingreso en la bocatoma". Respecto de los centros de salmonicultura en mar, la información sobre los registros de avistamientos durante el 2022, dan cuenta que en el área circundante a los centros de cultivo (balsas jaulas), reportados por la industria para el 2022, (información preliminar en proceso de análisis), solo 20 centros reportaron "avistamiento en el área circundante en mar" y ninguno registró interacción directa con el centro, no existiendo registro de mortalidades asociadas.
Aunque le evidencia es anecdótica, existe un solo registro formal, específicamente desde el año 2009, el cual se encuentra además publicado en el sitio web del Servicio Nacional de Pesca y Acuicultura y ha sido mencionado varias veces en distintas reuniones de trabajo. Paralelamente desde el trabajo de sistematización y validación de una base de datos de avistamiento de mamíferos marinos en centros de cultivo de salmones en mar, la cual se encuentra en construcción, se pueden citar algunas tendencias preliminares que dan cuenta que el 0,11% de los casi 17.000 registros de avistamiento de mamíferos marinos, corresponden a huillines. Paralelamente, se reconoce la ausencia de estudios específicos que evalúen el posible impacto de estas actividades productivas sobre huillines.
Por otra parte, las interacciones entre la acuicultura y otros mamíferos marinos están documentadas y suelen ser negativas, ya que éstos resultan afectados por pérdida de hábitat, disparos con armas de fuego en intentos por disuadir el acercamiento, principalmente de lobos marinos y el enmalle accidental en redes loberas o cabos de fondeo y redes (Ribeiro et al. 2007, Hucke-Gaete et al. 2013, Quiñones et al. 2019 en Hucke-Gaete et al. 2021).
El efecto negativo de la industria sobre los mamíferos probablemente sea mucho más relevante a nivel ecosistémico (Hucke-Gaete et al. 2021), ya que la actividad conlleva múltiples impactos ecológicos y sociales, incluyendo contaminación marina por antibióticos, eutroficación de las aguas marinas y lacustres, introducción de un depredador voraz, infecciones virales y desplazamiento de comunidades tradicionales de pescadores desde sus territorios ancestrales (Buschmann et al. 2021, Molinet & Niklitschek 2021). Sin embargo, cabe señalar que los registros oficiales demuestran que, los grados de interacción de los distintos mamíferos no son iguales, por ejemplo, para todo el año 2022 se reportan 125.000 interacciones con lobos marinos versus solo 20 con huillines (información preliminar en análisis).
Olavarría et al (2006) describen que uno de los impactos potenciales que genera esta industria es la construcción y modificación de terrenos adyacentes al borde costero, generándose asentamientos humanos que pueden ser directamente industriales o asociados a caminos, todos los cuales generan algún tipo de presión sobre este espacio en ambas especies de nutrias.
En este sentido, las amenazas que ejercería la acuicultura sobre el huillín son básicamente a través de los siguientes mecanismos:
. Modificación del hábitat por los procesos de construcción, instalación y operación de las pisciculturas en tierra y todos sus procesos asociados (Olavarría et al. 2006).
. Los riesgos en la interacción de estos especímenes con las instalaciones de las pisciculturas en tierra.
. El escape de especies salmonídeas que pueden invadir el hábitat del huillín y modificar la cadena alimenticia en su perjuicio, al depredar sobre presas que también pueda consumir el huillín (Buschmann et al. 2006, Correa & Gross 2008, Niklitschek et al. 2013, Habit et al. 2019).
. Aumento en el tránsito de embarcaciones.
. Aumento en la presencia de perros y gatos que llegan con los operarios.
B. Perros y gatos sin supervisión
Los perros, domesticados hace miles de años (Larson et al. 2012), han tenido un rol clave en actividades humanas como la cacería, control de plagas, seguridad y cuidado de ganado, entre otros.
Sin embargo, a pesar de los múltiples beneficios recíprocos entre humano y perro, la tenencia irresponsable ha tenido como consecuencia diversos impactos negativos tanto para seres humanos, como para otros animales (domésticos y silvestres) y el medio ambiente (ICAM 2007, Gompper 2014, Loss et al. 2013). Los perros pueden afectar a la fauna silvestre urbana y rural de manera directa (e.j., ataque, persecución, transmisión de enfermedades, competencia) o indirecta, alterando conductas normales de las especies, generando estrés, desplazamiento, entre otros (Young et al. 2011, Bonnington et al. 2013, Moseby et al. 2015). Es así como los impactos de perros pueden afectar tanto la estabilidad de las poblaciones como el bienestar individual de especies silvestres (Young et al. 2011, Loss et al. 2013).
Además, los perros pueden tener diversos impactos sobre la economía de las comunidades locales, ya que suelen depredar animales de granja como gallinas, vacas, ovejas, cabras (Lunney et al. 2013, Acosta-Jammet 2015, Montecino-Latorre & San Martin 2018), contaminar paisajes, dispersar basuras, y generar desechos, lo cual, sumado a los riesgos para la salud de las personas, pueden afectar otras actividades productivas como el turismo (Lunney et al. 2013, OIE/WSPA 2017). Encuestas a nivel nacional de percepción de salud y medio ambiente (MINSAL 2017, CIS UNAB 2019) posicionan a los perros (vagos, de libre desplazamiento o sin supervisión) como un elemento importante de contaminación ambiental.
A nivel internacional, los perros y gatos han sido identificados como de las principales amenazas para la biodiversidad (Gompper 2014, Mori et al. 2019), mientras que a nivel nacional múltiples estudios han explorado estos impactos (Svensson & Farías 2010, Acosta-Jamett et al. 2011). En particular, los perros han sido considerados una causa de mortalidad y desplazamiento para especies como el pudú (Pudu puda), huemul (Hippocamelus bisulcus), zorros (Lycalopex spp.), entre otros (e.j. Silva-Rodríguez et al. 2009, 2010).
En el caso del riesgo de transmisión de enfermedades, la interacción de ambas especies expone al huillín a patógenos como distemper canino (Sepúlveda et al. 2014), el Parvovirus Canino, y Leptospirosis (Barros et al. 2022).
C. Caza ilegal
Una de las principales causantes de la declinación poblacional del huillín en el pasado, identificada tanto en ambientes dulceacuícolas como costeros marinos, fue la caza para la exportación de pieles (Medina 1996). Entre 1910 y 1954 un total de 38.263 pieles de nutria, tanto de L. felina como L. provocax fueron exportadas desde Chile. La exportación se detuvo después de 1954 gracias a la implementación de leyes y acuerdos internacionales (Iriarte & Jaksic 1986) (Global Otter Conservation Strategy, IUCN Otter Specialist Group.)
A lo anterior se suma en menor cantidad, la caza comercial para subsistencia y de gran importancia para la alimentación, uso medicinal (de aceite de lobo y de aceite de huillín) y abrigo, para los primeros habitantes del Litoral de Aysén (Martinic 2005, Marticorena 2009, Torrejón et al. 2013). Aunque sin poder estimar su magnitud, utilizando el conocimiento local y los registros bibliográficos fue posible reconstruir las áreas de acción de las cuadrillas de cazadores en el pasado reciente, las que estuvieron concentradas principalmente en el archipiélago de Los Chonos, al oeste de los canales Pérez Norte y Pérez Sur para el caso del chungungo (L. felina), mientras que en el caso del huillín la cacería comercial se desarrolló en las costas este y oeste de los canales Moraleda y Costa (Simpson 1870, Torrejón et al. 2013, conocimiento local Melinka y Repollal).
En la actualidad esta amenaza está aún presente, y aunque el número puede ser bajo, su efecto en las poblaciones remanentes puede ser muy importante. Por ejemplo, en el río Queule se encontró un huillín muerto por arma de fuego el 2003, la población de huillines de ese río no debe superar los 20 individuos, por tanto, un individuo cazado representa el 5% de la población (Medina-Vogel com. pers.). Durante las prospecciones entre 1987 y 1992, se identificaron varias pieles de huillín en La Araucanía y en la Región de los Lagos y Ríos, igualmente se obtuvieron evidencias de caza en Magallanes (Medina 1996).
D. Actividades productivas que causan contaminación biológica, química y física
Una de las amenazas que afectan al huillín en ambientes dulceacuícolas es la contaminación de cuerpos de agua en los cuales vive esta especie afectando la calidad de su hábitat y el de sus presas, donde entre algunas de las causas se encuentran en el uso de sustancias químicas como fertilizantes, pesticidas y/o herbicidas para la actividad silvoagropecuaria y forestal, las cuales escurren o son vertidas hacia los cuerpos de agua (Álvarez 2013), además de la generación de compuestos nitrogenados de la ganadería, llegando a los cuerpos de agua mediante procesos de arrastre superficial o lixiviación (Correa-Araneda 2011).
En el caso del ambiente costero-marino, unido al aumento del tráfico de embarcaciones se asocian actividades humanas que generan impactos como contaminación por acumulación y fragmentación de plásticos. En todo el mundo, casi el 80% de la basura flotante proviene de asentamientos humanos costeros, mientras que el restante 20% proviene de todo tipo de embarcaciones y plataformas oceánicas (Coe & Rogers 2012). En Patagonia es común observar grandes cantidades de residuos marinos entre las que se incluyen bolsas plásticas, sogas y restos de redes (Hucke-Gaete et al. 2021). Existen registros que en 100 km de costa se podían encontrar más de 50 t de basura marina (Acuña-Ruz et al. 2018), la cual puede causar enmalles u obstrucción de vías respiratorias y/o gástricas en especies como aves y mamíferos marinos. Esta amenaza es especialmente compleja de manejar ya que el plástico, al degradarse queda reducido a micropartículas y fibras, las cuales son consumidas por mamíferos marinos (Hucke-Gaete et al. 2021).
Si bien esta amenaza quedó identificada como transversal, tanto para ambiente dulceacuícola como para marino, no queda integrada en plan de trabajo de los primeros años, y se reevaluará la integración de las actividades propuestas cuando se haga la primera evaluación y manejo adaptativo de este plan, ello básicamente por la ausencia de evidencia de un efecto directo sobre huillín.
E. Construcción y operación de centrales hidroeléctricas
Una de las consecuencias de la construcción de embalses y represas que ha sido identificada es la fragmentación de las poblaciones del huillín (Álvarez 2013). La intervención y desvío de los ríos dificulta la libre circulación de especies, causando la fragmentación del hábitat, e, incluso, la interrupción de la conectividad reduce los sitios de desove y por ende la oferta de alimentación para huillín (1).
La construcción y operación de represas y centrales hidroeléctricas es una amenaza potencial y latente a lo largo de todo el territorio donde habita el huillín, tanto en el ambiente dulceacuícola como costero-marino, ya que estas instalaciones modifican el régimen hídrico de ríos, canales y fiordos, así como las condiciones ecológicas del hábitat de la especie.
______________
(1) https://laderasur.com/estapasando/los-maquis-el-proyecto-hidroelectrico-ejecutado-sin-evaluacion-ambiental-en-aysen/
En el sector dulceacuícola, existen algunos proyectos que actualmente amenazan los hábitats del huillín. Uno de ellos es la Central Hidroeléctrica San Pedro (Colbún S.A.) en la Región de Los Ríos, la cual crearía un lago artificial sobre uno de los ríos con aguas más limpias de Chile y con una importante comunidad biodiversa de peces nativos del sur (Habit & Victoriano 2012, Centro de Energía 2016) y de huillín, impactando negativamente en la cuenca del río Valdivia. En otras cuencas de alto valor de conservación como la del río Biobío, se ha descrito desde la ciencia una evidente disminución en la biodiversidad y abundancia de especies nativas en los últimos diez años, producto de impactos ambientales originados por actividades industriales que incluye la construcción de grandes centrales hidroeléctricas (Habit et al. 2006).
En el caso del ambiente costero-marino, existe una amenaza permanente potencial frente a la elaboración de proyectos hidroeléctricos en la zona de canales y fiordos patagónicos. Ejemplo de ellos es Edelaysén, que desde enero de 2020 ejecutan, sin evaluación ambiental, el proyecto "Rehabilitación Mini Central Hidroeléctrica Los Maquis 2 x 500 kW" (1MW), presentado como el mejoramiento de una instalación ya existente. Esta propuesta ha sido aceptada por el Servicio de Evaluación Ambiental (SEA) y que tiene con gran preocupación a los habitantes del territorio ya que se construye dentro de la Zona de Interés Turístico (ZOIT) Chelenko (2).
F. Actividad turística costera y de navegación no sustentable
El turismo puede estar afectando directa e indirectamente al Huillín, al utilizar su hábitat para los recorridos, actividades y para el desarrollo de infraestructura (Olavarría et al. 2006).
En el ambiente dulceacuícola, tanto la región de Los Ríos y como la Región de Los Lagos son reconocidas por su gran cantidad de lagos y ríos que otorgan la posibilidad de realizar diversas actividades y deportes acuáticos, atrayendo en los meses estivales a gran cantidad de turistas. En ambas regiones se promueve el turismo de navegación a través de rafting, kayak y paseos en barcos por ríos, lagos, humedales y ensenadas, en pequeñas y grandes embarcaciones. En la Región de Los Ríos, se realizan estas actividades en ríos como Angachilla, Valdivia, Calle Calle, Cruces y Cau Cau, pasando y ocupando lugares que son hábitat y potencial hogar del huillín. Estas actividades tienen su más alta frecuencia durante los meses de enero y febrero, meses que coinciden con la época de reproductiva y de crianza de los huillines.
En el caso del ambiente costero marino, la mayor apertura de los canales y fiordos a la navegación comercial y otros proyectos de desarrollo privado, sumado a la disminuida presencia de la Armada de Chile, facilitan el incremento de presiones ambientales y sociales (Barros & Harcha 2004). Un ejemplo de ello es el crecimiento exponencial de la industria del turismo de cruceros en áreas que antes fueron resguardadas por la Armada, lo que implica el desembarque en islas deshabitadas y áreas protegidas que carecen de información básica, infraestructura y guardaparques (Rozzi et al. 2021). En este sentido, el turismo no regulado es una amenaza para lugares aislados tales como la zona patagónica (Kirk et al. 2018).
Aunque no existen registros de interacciones de nutrias con actividades turísticas, debido a que es de muy baja intensidad, hay aspectos indirectos de actividades como el turismo y recreación que podrían representar una amenaza potencial a las nutrias al utilizar el hábitat de éstas, principalmente para el desarrollo de infraestructura (Olavarría et al. 2006). Sin embargo, considerando el rol que tienen las nutrias como depredadores topes en los ecosistemas costeros es necesario evaluar potenciales impactos indirectos que estén afectando, debido a la contaminación costera por estos asentamientos humanos.
G. Especies Exóticas Invasoras
G.1. Visón americano como puente transmisor de enfermedades desde el perro y gatos al huillín
En los territorios rurales del sur de Chile se presenta una interacción entre animales domésticos (perros y gatos), el visón americano (mustélido exótico invasivo) y el huillín.
Varios estudios describen comportamientos del visón como animales exploradores siendo capaces de alejarse varios cientos de metros del curso de agua y llegar a las casas principalmente en busca de gallinas teniendo aquí altas probabilidades de tener contacto con perros y gatos domésticos, los cuales generalmente cumplen roles de cuidado y protección de los hogares.
(2) https://radio.uchile.cl/2021/04/26/corte-suprema-resolvera-disputa-por-construccion-de-central-los-maquis-en-aysen/
Generalmente los perros y gatos en zonas rurales no cuentan con una Tenencia Responsable de Mascotas adecuada, deambulando libremente sin supervisión y careciendo muchas veces de su vacunación y desparasitación periódica, convirtiéndose en una fuente de patógenos para especies nativas y exóticas, y si bien perros y huillines tienen menores posibilidades de contacto, ya que estos últimos rara vez llegan a casas en busca de alimento y no exploran mucho más allá que unos metros fuera del curso de agua, el contacto entre perros y visones sí podría traer consecuencias a huillines a través de la función de puente para la transmisión de enfermedades. El visón, en sus exploraciones por las casas, puede tener contacto directo con perros-gatos y sus heces, pudiendo contagiarse de patógenos, los cuales posteriormente podría transmitir al huillín al volver a los cuerpos de agua, al tener contacto con huillines o al usar las mismas letrinas.
En el caso de la triada "gato – visón – huillín", se ha encontrado relación por medio del parásito Toxoplasma gondii, el cual es un protozoo agente etiológico de la toxoplasmosis (enfermedad zoonótica).
Toxoplasma gondii, distribuido en todo el mundo presenta un ciclo indirecto con felinos domésticos y salvajes como hospederos definitivos. Los ooquistes se eliminan al medio ambiente a través de heces donde pueden permanecer infecciosos durante meses o años. Las especies de sangre caliente pueden infectarse al ingerir los ooquistes y la infección puede persistir en los hospederos infectados durante toda la vida (Dubey 2010). El efecto de la mayor presencia de T. gondii en el océano ha afectado negativamente el estado de salud de las poblaciones amenazadas de nutrias marinas del Pacífico norte, aumentando su mortalidad (Tenter et al. 2000, Kreuder et al. 2001) y apoyando la hipótesis de la transmisión de tierra a mar de este parásito a través de la escorrentía de agua dulce contaminada (Miller et al. 2002).
La infección generalizada por T. gondii en mamíferos acuáticos sugiere que la contaminación de las cuencas hidrográficas terrestres con T. gondii es prevalente, y que se distribuye un número suficiente de ooquistes en los ecosistemas de agua dulce y marinos para infectar y causar enfermedades tanto en mamíferos cercanos a la costa como pelágicos (VanWormer et al. 2013).
En Chile el primer estudio en este ámbito detectó en hábitats de huillín que los visones en mayor cercanía a centros urbanos presentaban una mayor seroprevalencia y detección por PCR de T. gondii (35 vs 100%) (Sepúlveda et al. 2011). Posteriores estudios han identificado ADN de T. gondii en tejidos de un visón americano y huillín (Barros et al. 2018).
El visón americano, puede servir como reservorios de enfermedades para las nutrias. Por ejemplo, la exposición de la nutria a T. gondii estará influenciada por la presencia de felinos en el campo. En este sentido, los gatos domésticos y salvajes representan el factor epidemiológico más importante en la dispersión del parásito (Millán et al. 2009) y su distribución y densidad están directamente influenciadas por la presencia humana.
En el caso de la triada perro – visón – huillín, el visón cumpliría también un rol de puente en la transmisión de enfermedades (Barros et al. 2022). En este sentido, estudios describen que, dada la diferencia de tamaños entre el huillín y visón, es poco probable que la especie introducida sea la dominante en la posible interacción que existe entre ambas especies (Valenzuela 2011, Medina-Vogel et al. 2013). Sin embargo, existe alta probabilidad de que ocurra transmisión de enfermedades infecciosas entre ellas, considerando tanto la alta sobreposición de actividad como co-ocurrencia en las letrinas de huillín, así como la conducta del visón al utilizar ambientes más terrestres donde habría encuentros con perros, actuando de esta manera como un hospedero puente de agentes transmisibles (Parvovirus y Virus Distemper Canino) entre perros y huillines (Sepúlveda et al. 2011).
G.2. Presencia de salmónidos asilvestrados
Chile presenta una larga historia de introducciones de salmónidos producto de la pesca deportiva y actualmente por el cultivo de salmones, convirtiéndose en el segundo país con mayor producción a nivel mundial (Habit et al. 2012, Arismendi et al. 2014).
Entre las décadas del setenta y noventa, los esfuerzos se concentraron en proyectos de cultivo para establecer poblaciones silvestres de salmón chinook (O. tshawytscha) en la Isla de Chiloé y río Prat; salmón coho (O. kisutch) en la isla de Chiloé; salmón chum (Oncorhynchus keta), salmón masou (Oncorhynchus masou) y salmón rosa (Oncorhynchus gorbuscha) en Aysén (Niklitschek et al. 2013). A pesar de los intentos de producción de estas especies, ninguno de estos esfuerzos de cría tuvo éxito comercial, pero sí tuvieron una gran influencia en la naturalización del salmón chinook, el cual invadió toda la zona patagónica (Ciancio et al. 2005, Soto et al. 2007, Correa & Gross 2008).
A escala de interacciones tróficas, según el estudio realizado por Soto et al. (2001), el grupo de los salmónidos asilvestrados posee una similitud en la dieta con las especies nativas. Al ser depredadores topes en sus sistemas natales, pueden competir con ellas dado que pueden alimentarse de una gran variedad de recursos disponibles en el ambiente, como peces, insectos, moluscos y crustáceos. Según lo anterior, existe un nivel importante de evidencia, de cómo la presencia de salmónidos puede influir en las especies nativas. Ortiz-Sandoval et al. (2015) establecen una sobreposición en la dieta de especies nativas de Chile y Argentina con la dieta que poseen los salmónidos invasores, alimentación basada principalmente de bentos y de peces en etapas adultas. Parte de este solapamiento en la dieta, afecta la disponibilidad de recursos para la especie nativa, ya que los salmónidos son más eficientes en el consumo de presas en ambientes pelágicos y en ambientes profundos con baja vegetación. Correa et al. (2012), demuestran que los depredadores topes pueden llegar a tener un efecto indirecto a nivel de alteración de nicho trófico de las especies nativas, por lo tanto, la presencia de estas especies podría disminuir la oferta alimenticia de peces nativos por competencia y afectar su nicho trófico, debido a que las etapas juveniles se alimentan de ítems como zooplancton, macroinvertebrados bentónicos e insectos (Pérez 2017).
En ecosistemas dulceacuícolas, tanto la pesca deportiva, como el cultivo de salmónidos han generado un fuerte impacto, contribuyendo a que especies como la trucha marrón (Salmo trutta) y trucha arcoíris (Oncorhynchus mykiis) dominen múltiples ecosistemas acuáticos. Estas especies han extendido su distribución y abundancia en las aguas continentales de Chile y Argentina y el salmón chinook en casi todos los ríos del sur de Chile (Correa & Gross 2008, Rossi et al. 2012, Soto et al. 2007). Sobre el éxito de las otras especies, no ha sido suficientemente documentado (Pérez 2017).
Según Arismendi et al. (2009), se ha observado un incremento en depredación de parte de salmónidos (incluido chinook) sobre las especies nativas (i.e. Galaxias platei, G. maculatus y Aplochiton zebra). El salmón chinook causa depredación sobre los peces endémicos de Chile (Ibarra et al. 2011), consumiendo insectos, larvas y huevos de peces y crustáceos de las cuales se alimentan peces, anfibios y aves nativas, así como generando cambios en la composición específica de la ictiofauna, en la dinámica de los nutrientes, en la fisiología de las aguas dulces continentales y en la cantidad de materia orgánica por descomposición de salmones que mueren al migrar desde el mar hacia cabecera de ríos (Subpesca 2018).
Por otra parte, en ambiente costero-marino, la explotación pesquera de salmónidos de vida libre en el Sistema de Fiordos y Canales de la Patagonia (SFCP) es la consecuencia de más de un siglo de introducciones reiteradas de estas especies en Chile y Argentina (Basulto 2003) y más de tres décadas de escapes masivos desde centros de cultivo (Arismendi et al. 2014). El impacto ecológico de las especies de los géneros Oncorhynchus y Salmo ha sido ampliamente estudiado en otros ecosistemas, sin embargo, existe ausencia de información en sistemas ecológicamente relevantes como los fiordos patagónicos. Por otra parte, un estudio más reciente señaló la presencia de juveniles de salmón coho (Oncorhynchus kisutch) y chinook (Oncorhynchus tshawytscha) en lagos y estuarios de estos ambientes (Górski et al. 2017). En la actualidad, se desconoce la abundancia de estas poblaciones, las que se presume altamente variables y se desconoce, además, la magnitud de la pesquería, dado que la normativa actual impide la declaración de las capturas, que se consideran ilegales. No obstante, se conoce, aunque todavía someramente, la dieta y rol trófico ejercido por estos salmónidos en el SFCP (Niklitschek et al. 2013).
La presencia de salmónidos asilvestrados causa una alteración tanto en ambiente dulceacuícola como costero-marino, afectando el nicho trófico mediante la depredación directa de alimento, cambio en la composición de la ictiofauna, dinámica de los nutrientes y cantidad de materia orgánica, entre otras. En este sentido, es relevante evaluar el impacto que generan sobre las poblaciones de huillín, tomando en consideración que las actividades de pesca deportiva están restringidas por la ley N°20.256, que si bien, se orienta a fomentar la actividad de pesca recreativa, también apunta a conservar las especies hidrobiológicas (salmones asilvestrados) y proteger sus ecosistemas, además de fomentar las actividades económicas y turísticas asociadas a la pesca recreativa y fortalecer la participación regional. Asimismo, la ley N° 21.600 regula la pesca de especies exóticas como las mencionadas dentro de áreas protegidas, para los fines de conservación de la diversidad biológica y la protección del patrimonio natural del país que fija el referido cuerpo legal.
4.2.3 Amenazas en ambientes dulceacuícolas
A. Cambio del uso de suelo en riberas por parcelaciones y/o actividades silvoagropecuarias
Las zonas ribereñas son ecosistemas dependientes de cursos o cuerpos de agua que cumplen funciones esenciales para la preservación de ecosistemas y sus relaciones territoriales, influyendo en el paisaje en términos de riqueza y belleza natural, a la vez que suministran bienes y servicios para la biota y el bienestar humano (Romero et al. 2014). En general, estas zonas permiten al paisaje que los alberga procesar mayor cantidad de materia orgánica, capturar más nitrógeno, mejorar la cantidad y calidad del agua, facilitar el procesamiento de contaminantes y regular la temperatura y luz que ingresa a los sistemas acuáticos (Scarsbrook et al. 2001, Sirombra & Mesa 2010, en Romero et al. 2014). Por otra parte, las zonas ribereñas o en galería son utilizadas como corredores biológicos, ya que estos paisajes son capaces de soportar una alta variedad de fauna convirtiéndose en sistemas claves para el mantenimiento de la diversidad tanto faunística como florística (Granados et al. 2006, Guevara et al. 2008).
Una de las amenazas identificadas es la alteración y la destrucción de humedales y por consiguiente de la vegetación ribereña, hábitat del huillín. A pesar de la importancia que tienen debido a su gran biodiversidad, actualmente se encuentran sometidos a numerosas presiones debido a la modificación de suelos aptos para la agricultura, así como para el establecimiento de proyectos inmobiliarios (Correa-Araneda et al. 2011). En ambos casos, los ecosistemas de humedales son drenados y/o rellenados debido al proceso de expansión poblacional (Figueroa et al. 2009).
En el caso de actividades agrícolas y ganaderas, la habilitación de zonas provoca la eliminación total de la vegetación ribereña, así como el drenado o secado de humedales o vegas (Álvarez 2013). El impacto del ganado en las zonas ribereñas incrementa la compactación del suelo, reduciendo la infiltración, degradando los márgenes de los cursos de agua y disminuyendo los niveles freáticos. Respecto a la vegetación, existe daño y reducción de la regeneración existente, y en algunos casos puede afectar especies endémicas asociadas a los cursos de agua. Por su parte, Ochoa (2007), señala que la extracción excesiva de agua con fines agrícolas, generan cambios en el funcionamiento de los sistemas ribereños.
Por otra parte, la actual regulación permite la aparición y proliferación de otros usos que fragmentan el borde de las áreas bajo protección, siendo el loteo y promoción de parcelas de agrado una de las formas más frecuentes de infiltrar usos urbanos en el suelo natural o rural (Romero et al. 2014). En el caso de los ecosistemas acuáticos se ha reducido la heterogeneidad ambiental y las complejas comunidades de plantas nativas de humedal, provocando la pérdida del hábitat y teniendo efectos sobre la fauna nativa. La homogenización ambiental permite la aparición de especies invasoras, además de la eutrofización, causada principalmente por la descarga de nutrientes y la contaminación bacteriológica contenida en los sistemas de escorrentía de agua y alcantarillado de drenaje de los alrededores de las zonas urbanas (Parra 1989, Urrutia et al. 2000, en Pauchard et al. 2006). Por su parte, Randolph (2004) y Owen (1998) afirman que el desarrollo urbano afecta a estos ecosistemas directamente a través de la impermeabilización de las superficies, lo que aumenta la erosión, sedimentación y contaminación por escorrentía de los ríos, además de contribuir con drenajes sépticos y vertederos a la contaminación de las aguas subterráneas.
B. Obras civiles que modifican cursos de aguas y vegetación ribereña
El crecimiento de la población humana ha provocado una mayor demanda de espacios y recursos naturales tanto acuáticos como terrestres, transformándolos y destruyéndolos a causa de la agricultura, la industria, la ganadería y la urbanización (Vitousek et al. 1997, Smith et al. 1999).
En base a las necesidades de la población, se desarrollan proyectos que apuntan al aprovechamiento de los ecosistemas acuáticos mediante la extracción de áridos, la desviación de cauces, drenaje de aguas o rellenos para la construcción de viviendas o industrias. Este problema es particularmente importante en los ecosistemas ribereños, donde las represas, desviadores de agua, alcantarillas, tuberías y otras estructuras civiles crean barreras para el movimiento natural de los organismos acuáticos (Washington Department of Fish and Wildlife 2009, Kemp 2012, en Morales & Sobenes, 2018). Este tipo de obras pueden provocar diferentes efectos como: reducción de hábitat, pérdida de vegetación acuática o despeje de vegetación ribereña (Martínez 2001, Swales 1989, en Morales & Sobenes 2018).
La fragmentación de los ríos provoca la pérdida de biodiversidad, y por lo tanto altera el funcionamiento natural de los ecosistemas (Morita & Yamamoto 2002, Morita & Yokota 2002, Williams et al. 2005, Goodwin et al. 2006, Mims & Olden 2012). Si es que existen obstáculos en un sistema ribereño y la fauna íctica no puede desplazarse aguas arriba o aguas abajo del obstáculo, es probable que se produzca una declinación en las poblaciones de peces, microorganismos, crustáceos, entre otros (Brooker 1985), alterando el estado ambiental del ecosistema ribereño (Jackson et al. 2001).
Una de las actividades que ejerce una importante presión es la extracción de áridos, debido a la demanda actual que existe principalmente para construcción. Se realiza desde canteras ubicadas en cerros rocosos y mayoritariamente es extraído de los lechos de ríos, para lo cual intervienen una fracción del lecho y modifican el cauce de las aguas. En este contexto, los efectos negativos sobre la biodiversidad son evidentes, repercutiendo gravemente sobre especies, microorganismos y flora que puedan existir en el lugar y algunos casos, puede modificar el hábitat de forma muy severa, así como la calidad de las aguas, particularmente por aumento de la turbidez.
Si bien no existe una cuantificación del impacto que provocan las obras civiles sobre los ecosistemas dulceacuícolas orientado a la pérdida de biodiversidad, la escasa información permite identificar que la alteración sobre estos hábitats podría estar generando importantes modificaciones en los ecosistemas donde habita el huillín, alterando su nicho ecológico.
C. Extracción de crustáceos
Los crustáceos cumplen un importante rol en el nivel trófico en el ambiente dulceacuícola debido a su actividad detritívora y omnívora, particularmente a través de funciones tales como limpieza y reciclado de materiales de desecho, limitación del grado de eutroficación y control de los niveles microbiológicos (Pérez et al. 1997).
En ambientes dulceacuícolas, la dieta del huillín varía según su disponibilidad, sin embargo, estas poblaciones consumen principalmente crustáceos de los géneros Samastacus y Aegla (Chehébar et al. 1986, Medina 1998, Sepúlveda et al. 2009).
En las aguas continentales chis entre el río Aconcagua (32°55'S, 71°18'W) y la península de Taitao (46°30'S, 74°30'W), habitan seis especies de camarones de la Familia Parastacidae (Crustácea, Decapoda, Astacidea) (Rudolph & Crandall 2007). Una de las especies de esta familia es Samastacus spinifrons (Philippi 1882), la cual habita aguas abiertas, i.e., riachuelos, ríos y lagos situados entre el borde costero y la precordillera andina (Bahamonde & López 1963). Samastacus spinifrons ha sido considerada atractiva para la acuicultura debido a ciertas características biológicas que les confieren ventajas comparativas respecto a las otras cinco especies. Sus poblaciones están siendo sometidas a una intensa presión extractiva para consumo humano, sin restricción de vedas, tallas mínimas de extracción o protección de las hembras ovígeras. En cuanto a su hábitat, esta especie está experimentando un deterioro progresivo por acción antrópica (Rudolph 2002).
Por otra parte, los crustáceos decápodos del género Aegla Leach son elementos conspicuos de la limnofauna del cono sur de Sudamérica (Schmitt, 1942). En Chile la diversidad del género alcanza a siete especies (Bahamonde & López 1963, Jara 1977) que representan poco más del 20% de las treinta y tres especies conocidas del género (Manning & Hobbs 1977). De las siete especies chilenas, cuatro se hallan representadas en la provincia de Valdivia y tres de ellas han sido registradas en la cuenca hidrográfica del río Valdivia (Schmitt 1942, Bahamonde & López 1963, Jara 1977) constituyendo el mayor conjunto de especies de Aegla detectado en una cuenca unitaria chilena.
Dado estos antecedentes, la extracción de ambos géneros es una amenaza latente para el huillín, debido a que afecta directamente la disponibilidad de alimento en ambientes dulceacuícolas, afectando las funciones ecológicas del ecosistema que habitan.
4.2.4 Amenazas en ambientes costero marino
A. Aumento de tránsito marítimo
Existen actividades que representan una serie de impactos o efectos ecológicos sobre las especies de mamíferos y aves marinas, entre las que destacan la acuicultura, la pesca industrial y artesanal, así como proyectos de desarrollo costero, turismo y transporte (Guala et al. 2021, Buschmann et al. 2021). A medida que estas actividades humanas se intensifican (particularmente la salmonicultura), también lo ha hecho el tráfico marítimo, que ha sido ampliamente reconocido como un factor importante que afecta a las poblaciones de aves y mamíferos marinos (Hucke-Gaete et al. 2021). No solo el riesgo de colisiones representa un peligro para estas especies (Laist et al. 2001), sino que el ruido submarino generado por la cavitación puede generar cambios en los comportamientos, distribución, abundancia y en las dinámicas poblacionales (Hildebrand 2009). Solo entre Puerto Montt y el fiordo Aysén, se concentran importantes rutas de navegación como resultado del aumento del transporte de carga, combustible, público, actividades turísticas, acuicultura y pesca (Hucke-Gaete et al. 2021).
Una de las áreas que ha tenido un mayor incremento de esta amenaza producto de las operaciones de la industria salmonera ha sido la zona de archipiélagos y fiordos al sur de la isla Grande de Chiloé. Por otra parte, la posible concreción del proyecto de construcción de un puente que conectaría la isla de Chiloé (por su lado norte) con el continente, aumentaría en forma considerable el tráfico de embarcaciones en el golfo de Corcovado, debido a que indudablemente Quellón se transformaría en el puerto más importante del sur de Chile.
En el caso del tránsito marítimo por turismo, se identifican tres tipos de rutas con poca información y datos disponibles: i) aquellas operadas por cruceros turísticos de amplia trayectoria (e.g., Laguna San Rafael); ii) las de carácter mixto que cumplen la función de conectar al territorio y son utilizadas por turistas que se desplazan de manera independiente (e.g., Ferry Tortel-Puerto Natales); iii) aquellas operadas por agentes locales que realizan navegaciones en las áreas silvestres protegidas del Estado (Guala et al. 2021). Las principales amenazas descritas se asocian con colisiones con animales, contaminación acústica y accidentes (derrames de petróleo). En el caso del huillín no se han registrado interacciones con actividades turísticas, sin embargo, existen registros de que esta actividad, principalmente asociada a la navegación, afecta a cetáceos y lobos marinos (CPPS/PNUMA 2007).
B. Extracción de macroalgas
Aunque no existen antecedentes del impacto que causa la extracción de macroalgas en la zona austral del país, se reconoce por expertos como una actividad que ejerce presión en los hábitats de huillín.
Actualmente, en el norte del país, existe una preocupación por esta creciente práctica que reviste un grave peligro para la protección de los océanos y la capacidad de adaptación de los ecosistemas al cambio climático. Las algas pardas, especies extraídas, tienen importancia ecológica porque constituyen hábitat y refugio para la reproducción, el asentamiento larval y reclutamiento de varias especies de invertebrados y peces. En ambientes marinos costeros del norte de Chile los huiros actúan como especies fundacionales e ingenieras de ecosistemas, constituyendo focos de alta diversidad biológica, que alberga además otras especies de importancia económica y social (e.g., lapas, loco, erizos, peces) (Vásquez et al. 2010).
Los efectos ecosistémicos de la exploración de algas pardas han sido demostrados, pero no cuantificados. Entre los efectos ecológicos está la remoción de especies asociadas y la alteración del hábitat. Esto, frecuentemente se traduce en cambios en los patrones de distribución y abundancia de las especies asociadas a estos ecosistemas, sumado a las modificaciones de sus estructuras poblacionales (Druehl & Breen 1986, Foster & Barrilotti 1990, Vásquez 1995).
Esta es una variable comunitaria recomendada como indicador que responde a cambios ambientales naturales o causados por impactos antrópicos como la explotación directa (Caddy & Mahon 1995). En algunas pesquerías se ha detectado, como producto de las cosechas y/o capturas, un cambio en la riqueza y abundancia relativa de las especies constituyentes de la comunidad (Bustamante & Castilla 1990, Castilla & Duran 1985). En este contexto, las algas pardas han sido descritas como importantes organismos estructuradores de comunidades, y sus estructuras de fijación conforman un microhábitat para un gran número de especies de invertebrados (Vásquez & Santelices 1984).
En base a lo anteriormente expuesto y a los niveles de extracción de algas no cuantificados en la zona austral del país, esta actividad se convierte en una amenaza potencial, sobre todo en zonas de borde costero donde habita el huillín poniendo en peligro a la especie y todo su ecosistema.
5. Actores Relevantes para la implementación del Plan
Dentro de los Actores clave, se consideran relevantes para la implementación del Plan a servicios públicos y municipalidades por sus competencias legales sobre el territorio, como también son importantes de relevar ONG y comunidades locales, estas últimas por el gran vínculo que fortalecen en apoyo de municipios, servicios públicos e investigadores. De igual modo se relevan a propietarios de áreas dedicadas a protección y conservación de la biodiversidad. Estos son:
Ministerios y Servicios Públicos
- MMA (Ministerio del Medio Ambiente)
- MINAGRI (Ministerio de Agricultura)
- MOP (Ministerio de Obras Públicas)
- Ministerio de Defensa Nacional
- MINEDUC (Ministerio de Educación)
- Secretarías Regionales Ministeriales de Economía
- SMA (Superintendencia del Medio Ambiente)
- SEA (Servicio de Evaluación Ambiental)
- DGA (Dirección General de Aguas)
- DOH (Dirección de Obras Hidráulicas)
- CONAF (Corporación Nacional Forestal)
- SUBPESCA (Subsecretaría de Pesca y Acuicultura)
- SUBTURISMO (Subsecretaría de Turismo)
- SERNAPESCA (Servicio Nacional de Pesca y Acuicultura)
- SAG (Servicio Agrícola y Ganadero)
- DIRECTEMAR – Armada
- SERNATUR (Servicio Nacional de Turismo)
- SUBDERE (Subsecretaría de Desarrollo Regional y Administrativo)
- FOSIS (Fondo de Solidaridad e Inversión Social)
- IFOP (Instituto de Fomento Pesquero)
- INDAP (Instituto Nacional de Desarrollo Agropecuario)
- INIA (Instituto Nacional de Investigaciones Agropecuarias)
- Gobiernos Regionales
- Comisiones Regionales de Uso de Borde Costero
- Servicios Locales de Educación Pública
- Carabineros de Chile
- Servicio de Biodiversidad y Áreas Protegidas (SBAP), una vez entre en pleno funcionamiento
Municipalidades
- Municipalidades Región de La Araucanía: Municipalidad de Cunco, Municipalidad de Melipeuco, Municipalidad de Toltén
- Municipalidades Región de Los Ríos: Municipalidad de Valdivia, Municipalidad de Corral, Municipalidad de La Unión, Municipalidad de Mariquina, Municipalidad de Paillaco, Municipalidad de Los Lagos, Municipalidad de Lanco, Municipalidad de Panguipulli, Municipalidad de Futrono, Municipalidad de Lago Ranco, Municipalidad de Máfil, Municipalidad de Río Bueno.
- Municipalidades Región de Los Lagos: Municipalidad de Puerto Varas, Municipalidad de Maullín, Municipalidad de Llanquihue, Municipalidad de Puerto Montt, Municipalidad de Ancud, Municipalidad de Castro, Municipalidad de Castro, Municipalidad de Quellón, Municipalidad de Chonchi, Municipalidad de Dalcahue, Municipalidad de Quinchao, Municipalidad de Quemchi, Municipalidad de Queilén, Municipalidad de Puqueldón, Municipalidad de Curaco de Vélez.
- Municipalidades Región de Aysén: Municipalidad de Aysén, Municipalidad de Tortel, Municipalidad de Puerto Cisnes, Municipalidad de Guaitecas.
- Municipalidades Región de Magallanes: Municipalidad de Timaukel, Municipalidad de Cabo de Hornos, Municipalidad de Natales, Municipalidad de Punta Arenas.
- Toda otra municipalidad para la cual existen hoy y a futuro registros de la especie.
Investigadores
- Universidad Andrés Bello
- Universidad Arturo Prat
- Universidad Católica de Chile / Centro de Ecología Aplicada y Sustentabilidad
- Universidad de Magallanes / Instituto de la Patagonia
- Universidad Católica de Temuco
- Comité Nacional Pro Defensa de la Flora y Fauna (CODEFF)
- Universidad Nacional de Tierra del Fuego
- Parque Nacional Tierra del Fuego – APN Argentina
- Parques Nacionales Ushuaia y Tierra del Fuego – APN Argentina
- Parque Nacional Nahuelhuapi – APN Argentina
- Fundación Biodiversidad Argentina – APN Argentina (Bariloche)
ONG
- Pew Charitable Trusts
- Aumén
- Centro de Humedales Río Cruces (CEHUM)
- Centro de Estudio y Conservación del Patrimonio Natural (CECPAN)
- Chiloé Silvestre
- Fundación Meri
- Fundación Omora
- Fundación Romahue
- Fundación Auiläff
- CODEFF
- Puelo Patagonia
- Fundación Legado Chile
- ONG Kauyeken
- WCS Chile
- Fundación para el AMP Pitipalena-Añihue
- Fundación Kreen
- Whalesound (operador turístico)
- Chiloé Protegido
- Fundación Conservación Marina
- Otras por identificar
Comunidades locales
- Escuela de Kayak (Aysén)
- Comité Técnico Local Gef Humedales Costeros
- Comité Ambiental Comunal de Tortel (Aysén)
- Asociación de Turismo Náutico (Aysén)
- Comunidad Peulla, Puerto Varas (Los Lagos)
- Lof Mapu Werrere de Cunco (La Araucanía)
- Santuario Río Maullín (Los Lagos)
- Museo Historia Natural Río Seco
- Comunidad Kawesqar Puerto Edén (Aysén)
- Asociación Comunidad Humedal (ACH)
- Otras por identificar
Sector privado
- Iniciativas de conservación privadas, incluye áreas protegidas privadas
- Empresas que operan en áreas de relevancia para huillín
6. Visión del Plan
"En los ríos, lagos del sur de Chile y en los fiordos y canales costeros de la Patagonia, las poblaciones de huillín han sido recuperadas mediante una gestión integral multisectorial y cuenta con una protección efectiva, permitiendo un desarrollo local compatible con la conservación de esta especie paragua y carismática".
7. Alcance del Plan
El alcance del Plan comprende de norte a sur desde la Región de La Araucanía hasta la Región de Magallanes. De este a oeste, desde la Cordillera de los Andes hasta el Océano Pacífico (Figura 2). La justificación de esta extensión dice relación con la distribución actual del huillín, la que se describe desde el río Imperial en la Región de la Araucanía (Sepúlveda et al., 2007), hasta el extremo sur de Tierra del Fuego en Chile y Argentina, 54ºS en la Región de Magallanes (IUCN, 2009).
En términos ecosistémicos, el alcance del Plan busca representar los diferentes ambientes en los que habita la especie, considerando tanto los ambientes dulceacuícolas (ríos, esteros y lagos), como los ambientes costero marinos (estuarios, fiordos y canales). Y, como último, en términos de la división político-administrativa, el área de estudio se divide en cinco regiones, desde la más norte a la más austral, siendo éstas: La Araucanía, Los Ríos, Los Lagos, Aysén del General Carlos Ibáñez del Campo, y Magallanes y la Antártica Chilena.
Figura 2. Mapa de distribución de la especie huillín según la The IUCN Red List of Threatened Species. Fuente: Sepúlveda et al. 2015
8. Meta del Plan
En un plazo de 15 años aumentan al menos en un 10% los sitios de ocupación de la especie en el ambiente dulceacuícola y costero marino, y la especie mantiene su rango actual de distribución, evitando la pérdida de poblaciones dentro de su distribución.
Nota: Para la evaluación de la meta se identificarán los sitios de monitoreo en el marco de la acción 2.1.1 y el programa de monitoreo que sea diseñado.
9. Objetivos del Plan de Acción
. Objetivo 1. Disminuir el impacto de las amenazas que afectan al huillín y su hábitat en el ambiente dulceacuícola y costero marino mediante la modificación de políticas públicas.
. Objetivo 2. Aumentar la protección de las poblaciones del huillín y su hábitat dentro y fuera de áreas protegidas tanto en el ambiente dulceacuícola como costero marino.
. Objetivo 3. Contar con una gobernanza e institucionalidad que permite la coordinación entre servicios y organizaciones, y con financiamiento para el desarrollo de acciones.
10. Estructura del Plan de Acción
A continuación, se detallan las líneas de acción con sus indicadores de seguimiento.
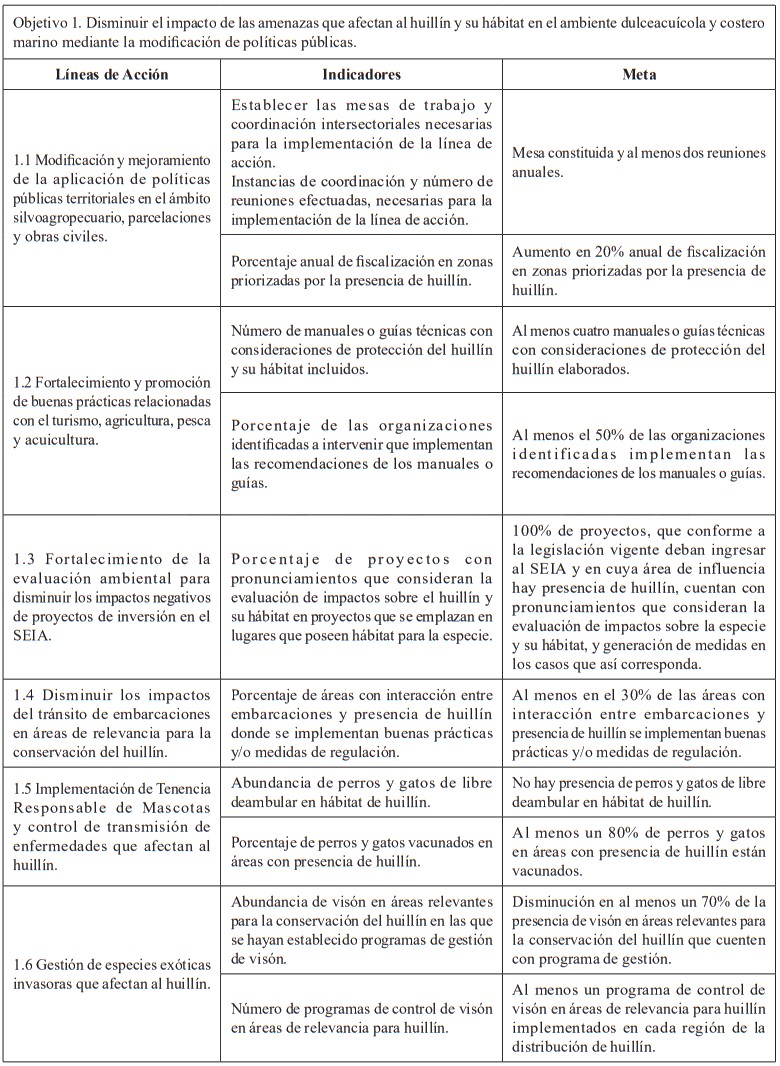
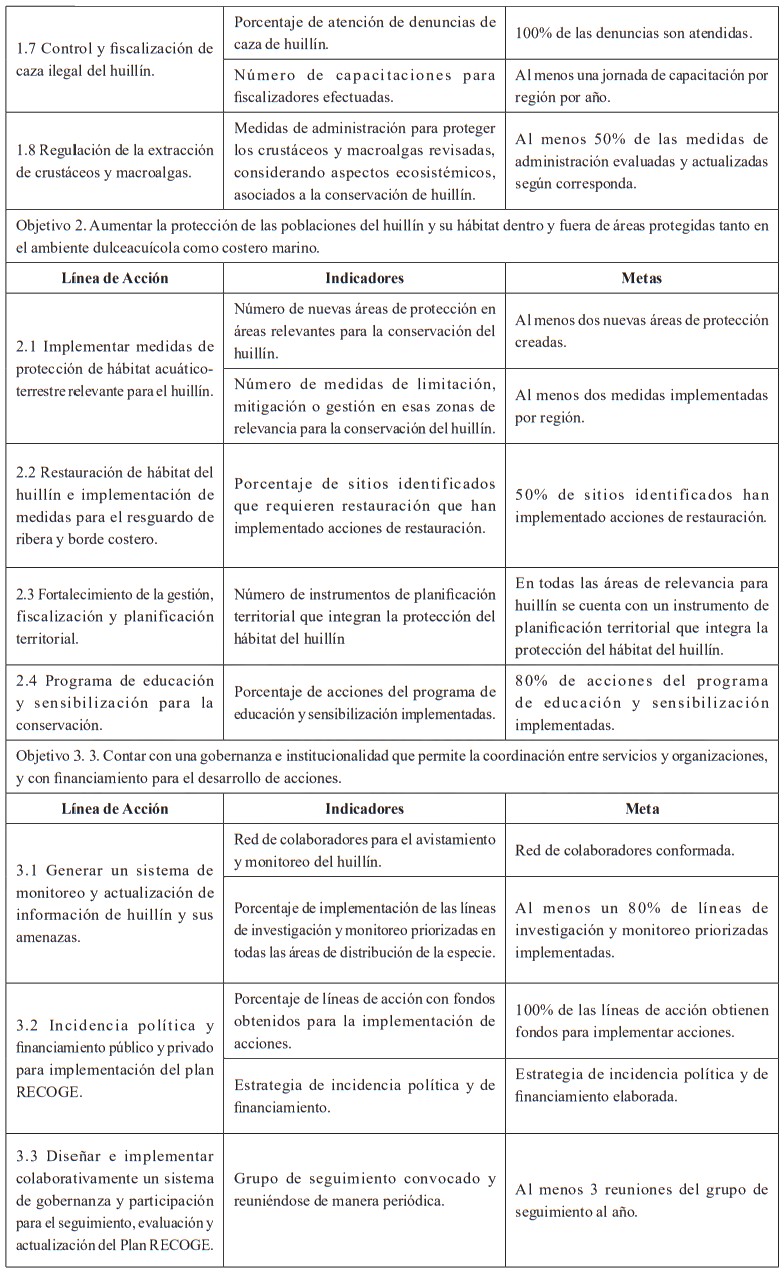
A continuación, se detalla las acciones según Línea de Acción y objetivo del Plan, actividades por la línea de acción, plazos asociados, productos / resultados y responsables sugeridos e indicadores de seguimiento para cada una de ellas.
Para la ejecución de estas acciones, y la implementación del Plan, se deberá promover la coordinación y sinergia con otras políticas públicas, así como estrategias y planes de acción a nivel nacional o regional que consideran actividades relacionadas directa o indirectamente a la implementación de acciones del presente plan RECOGE.
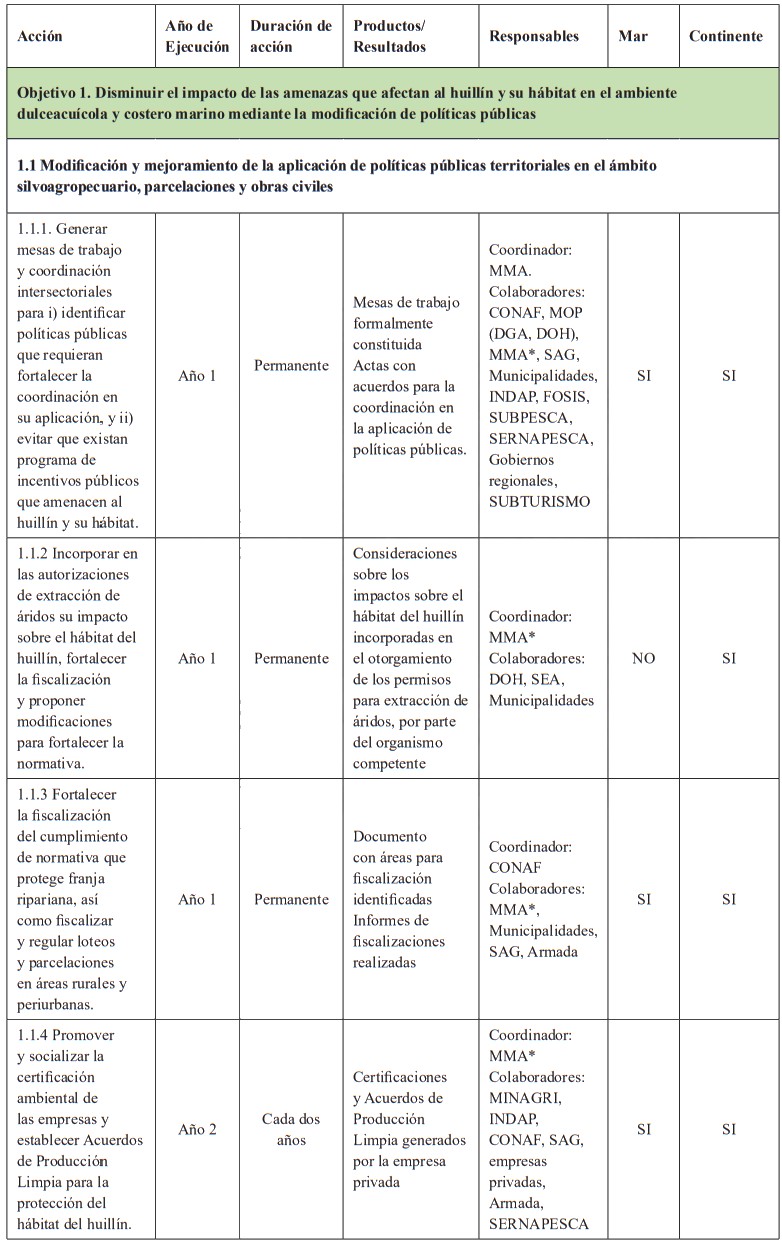
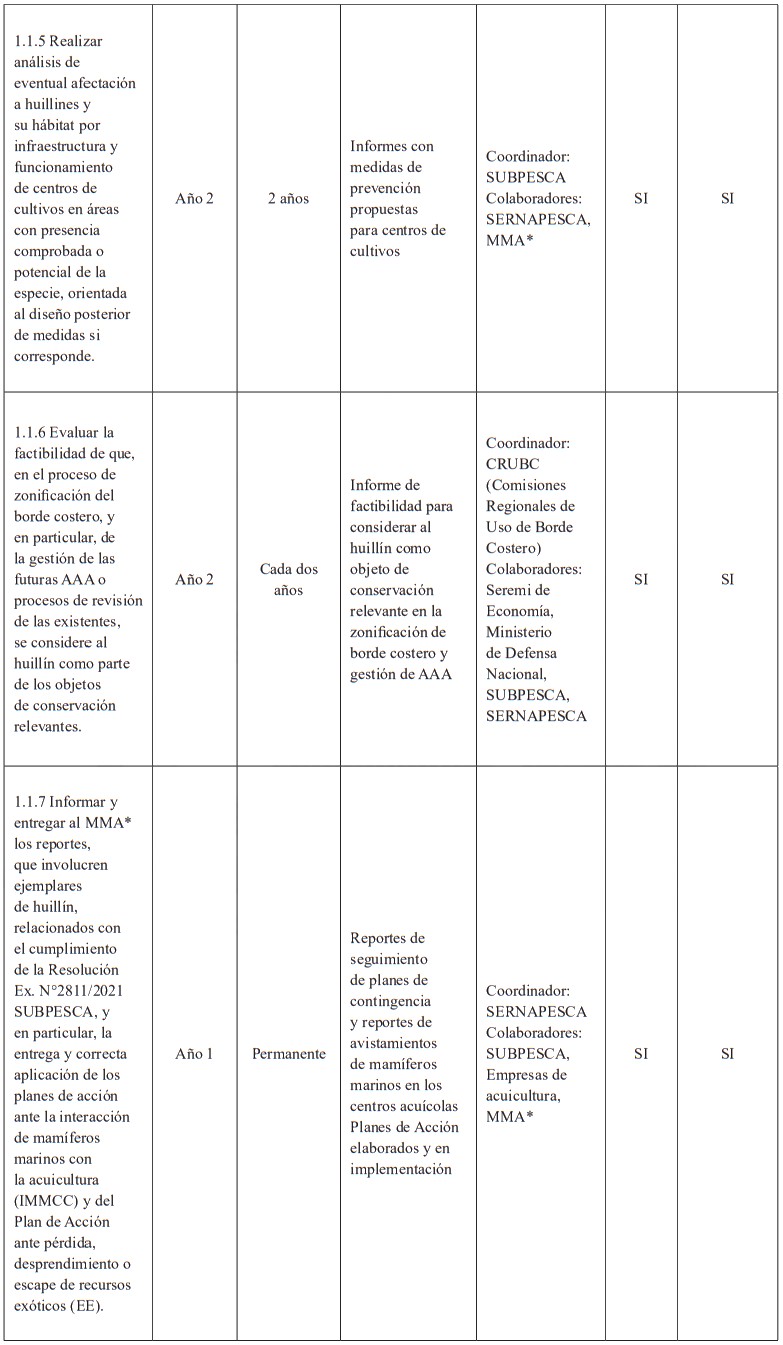
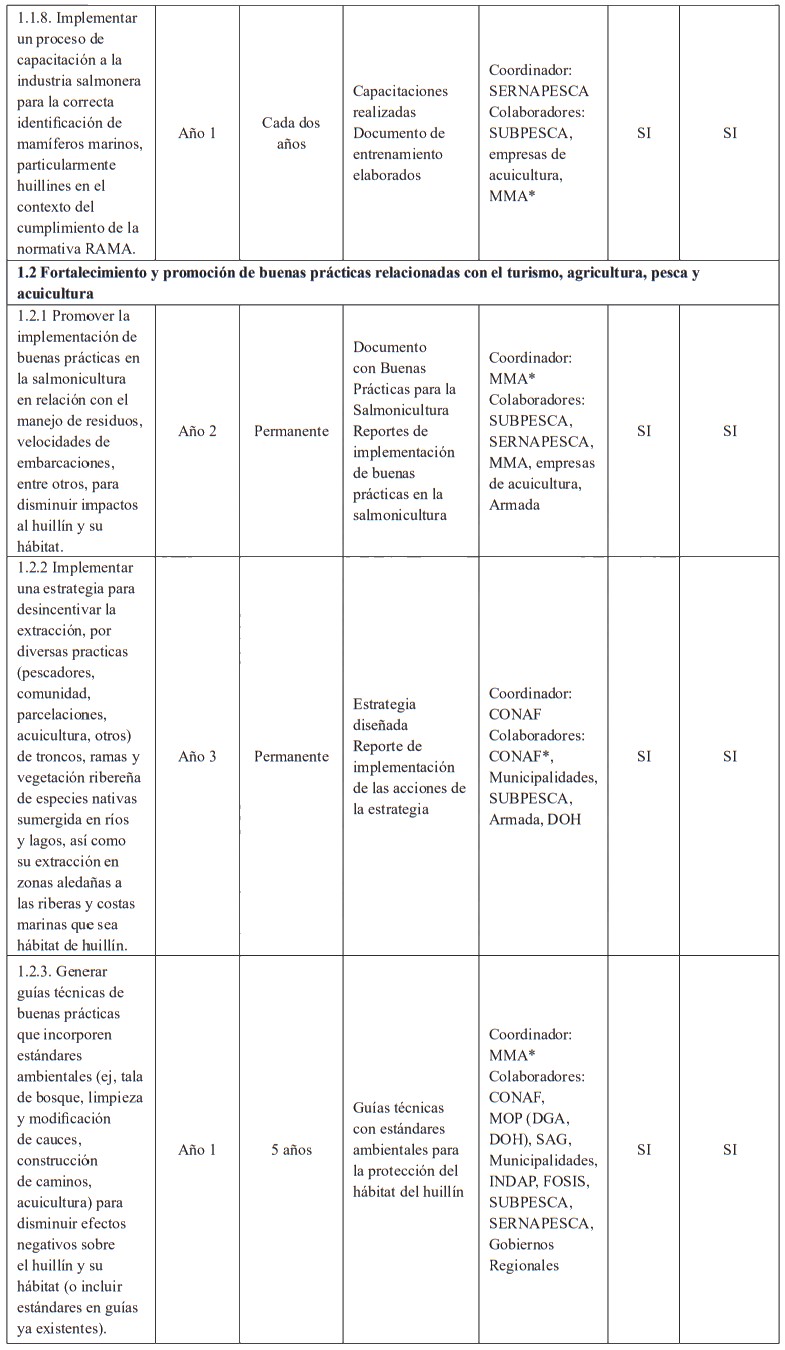
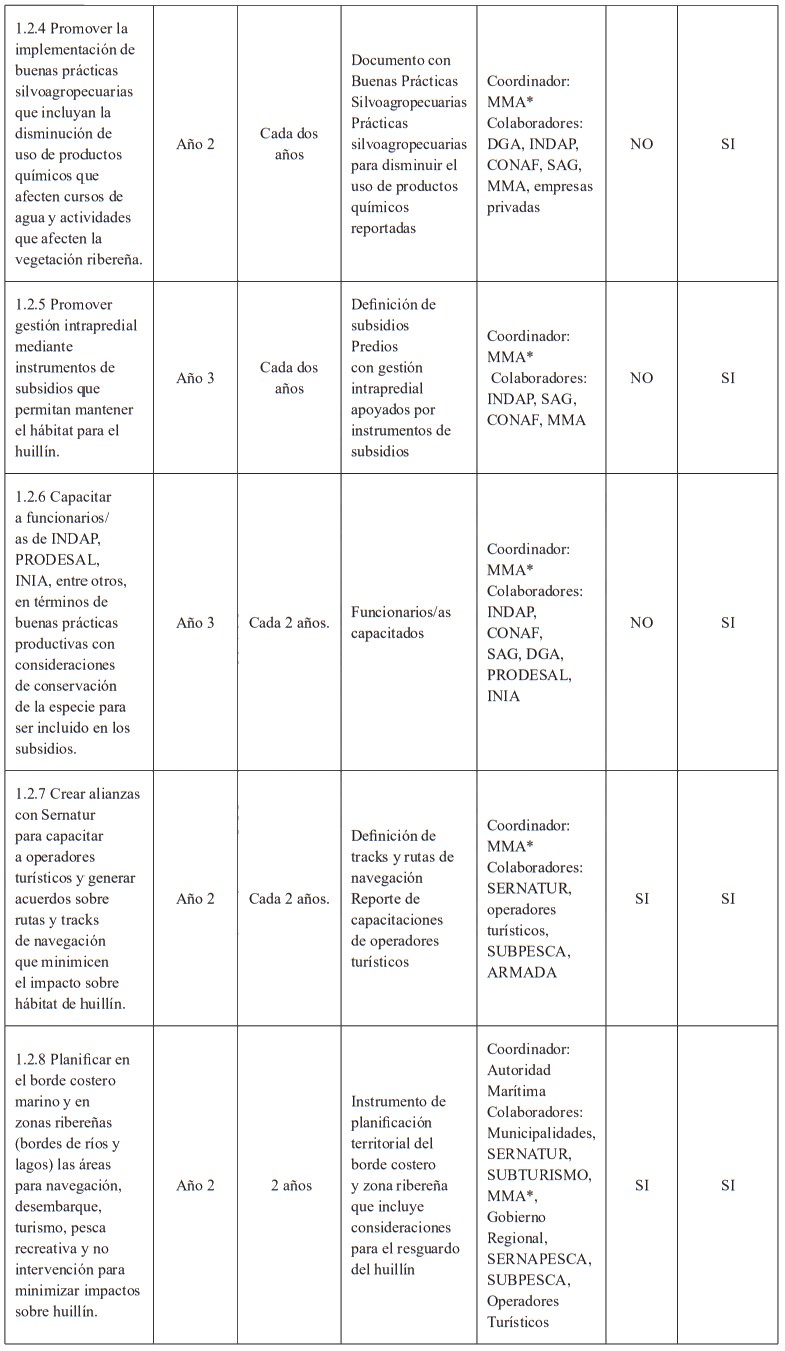
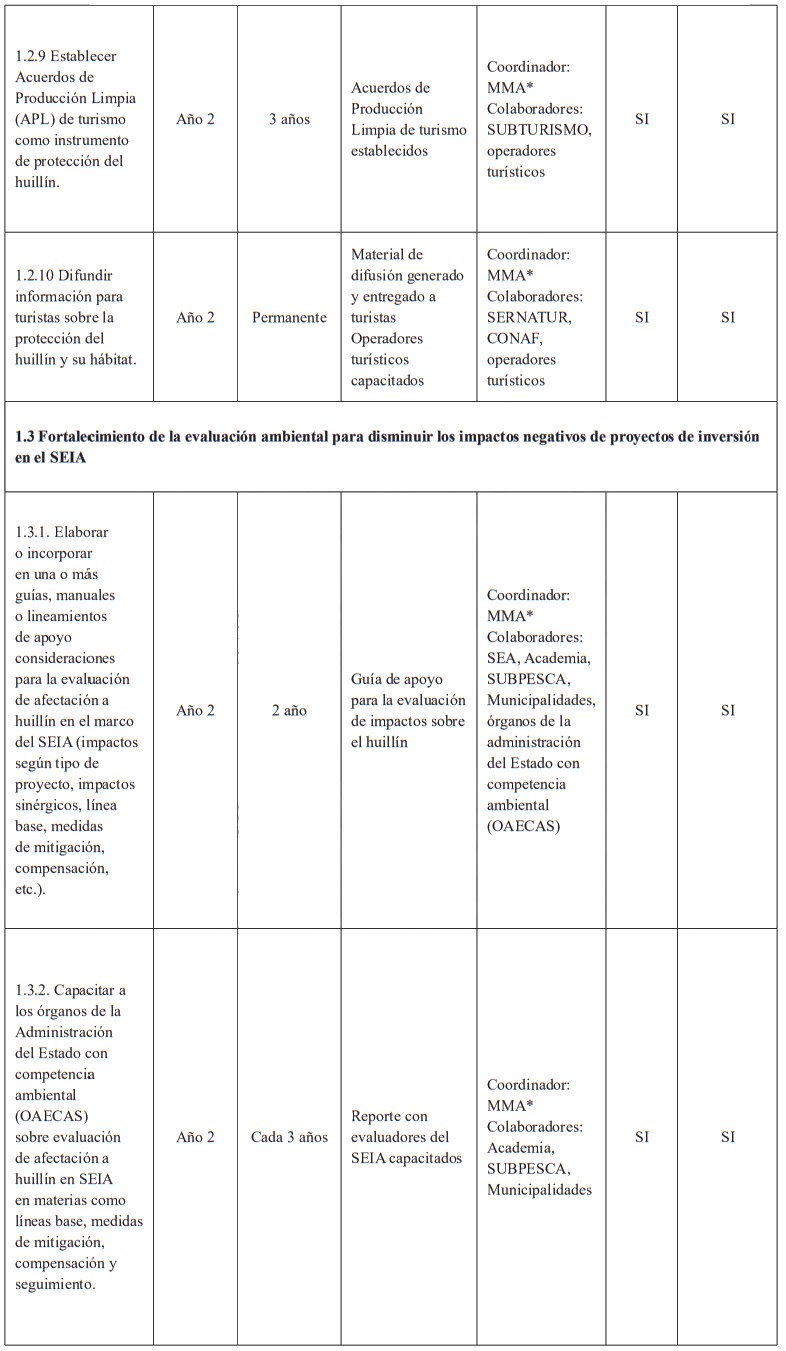
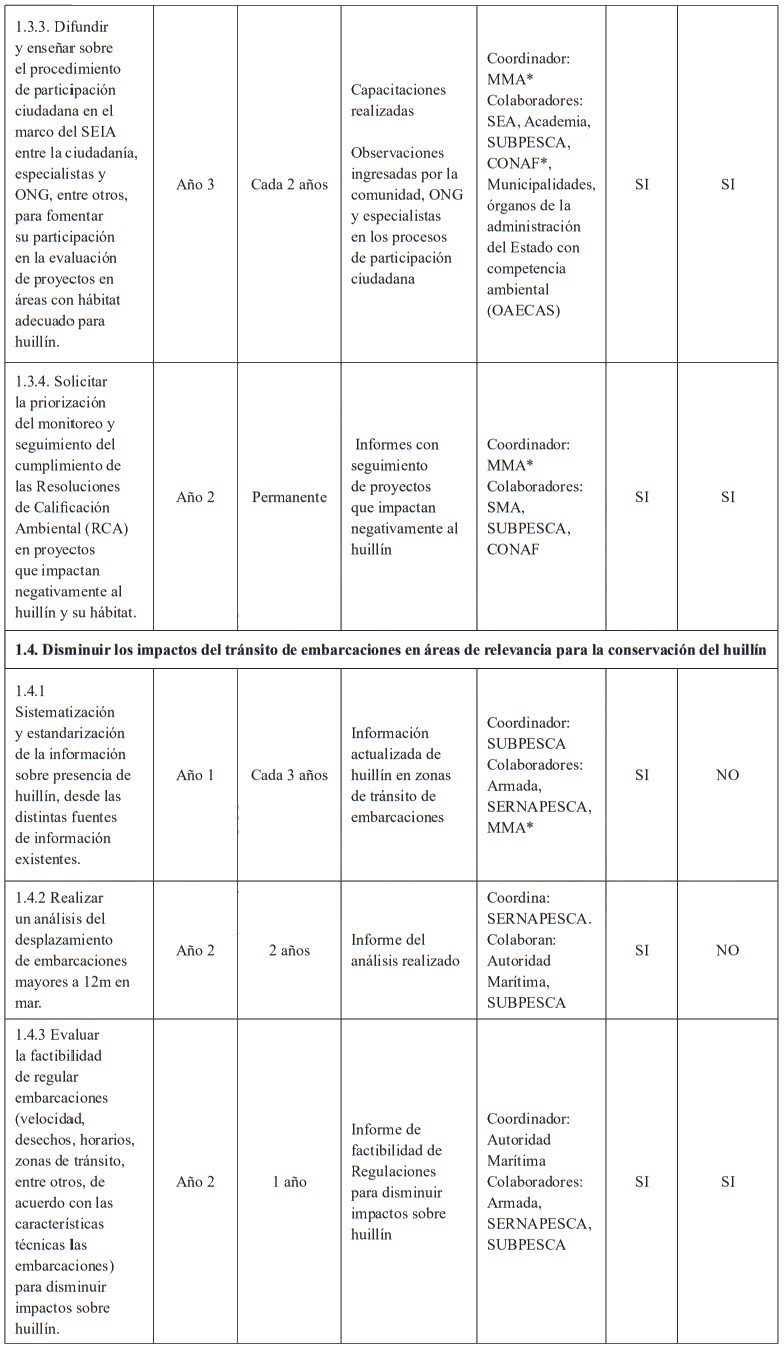
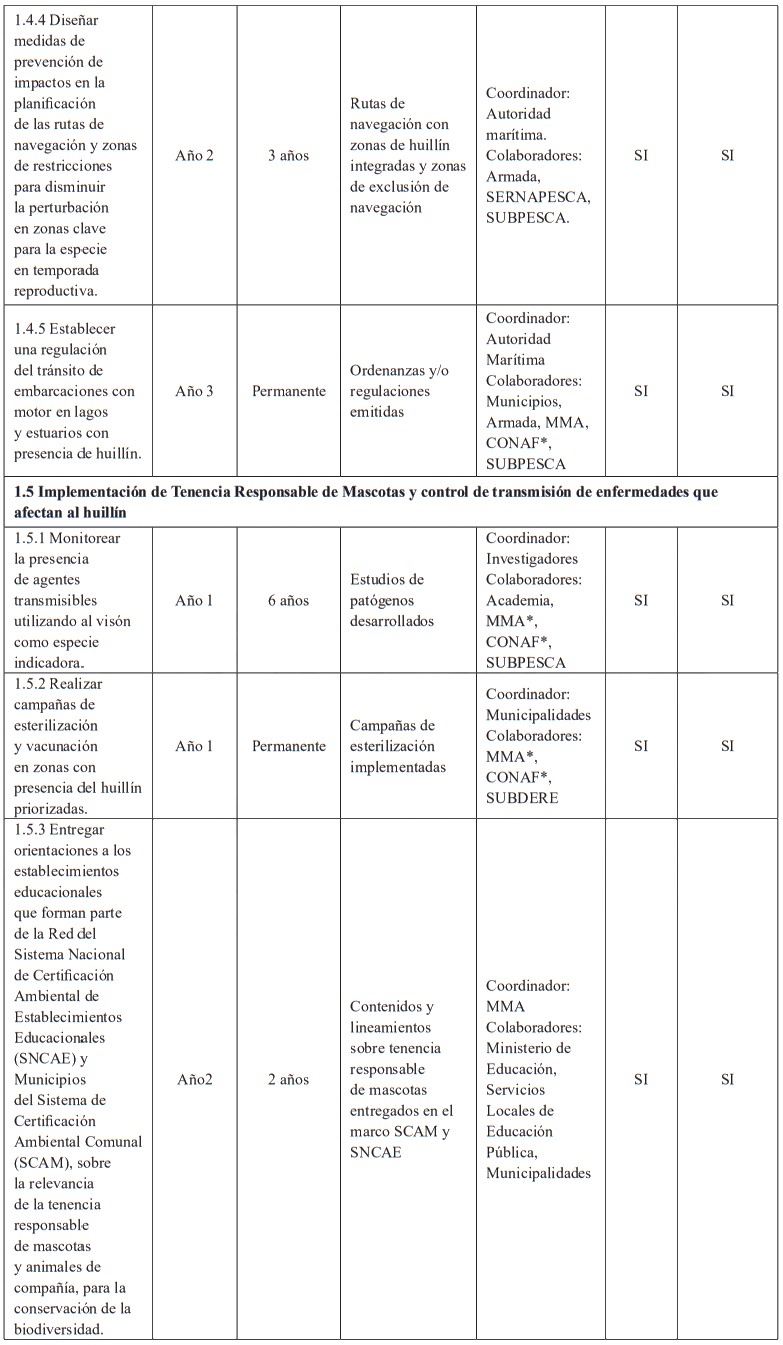
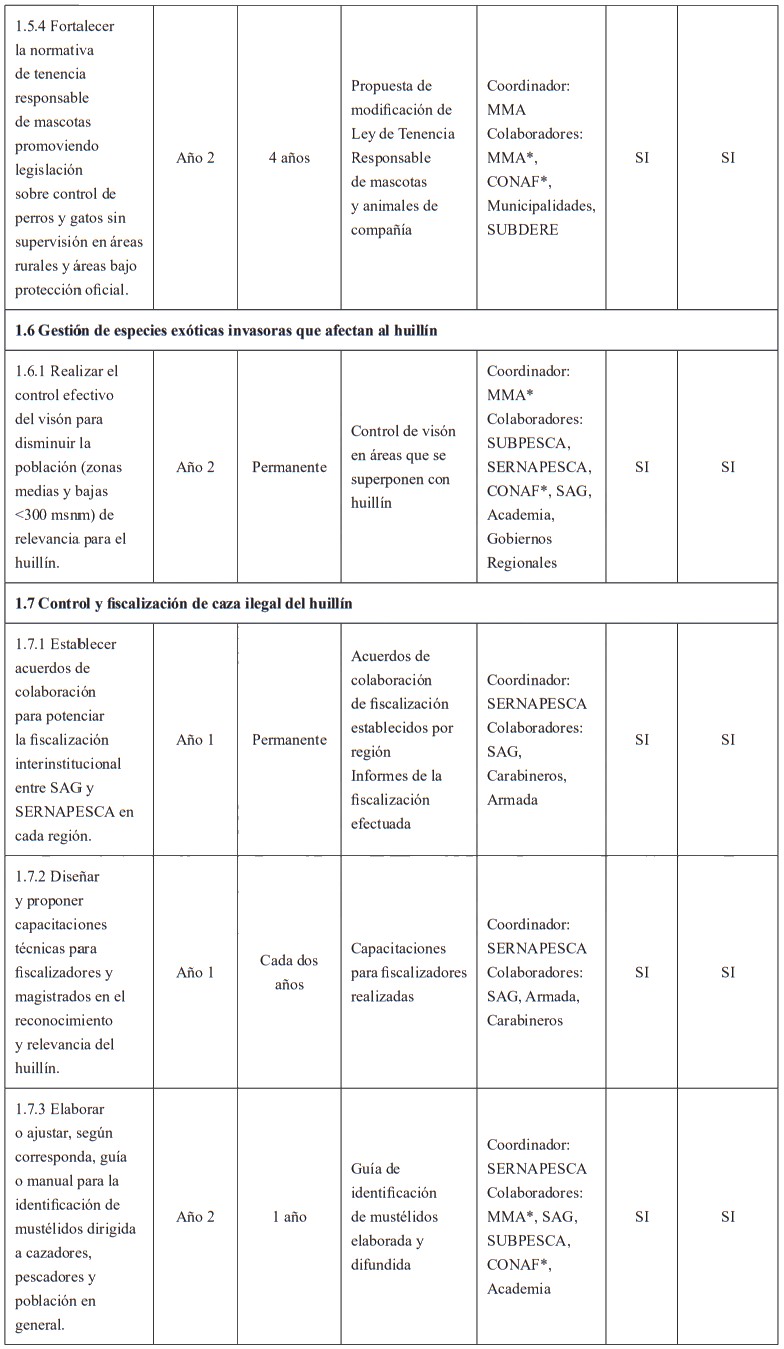
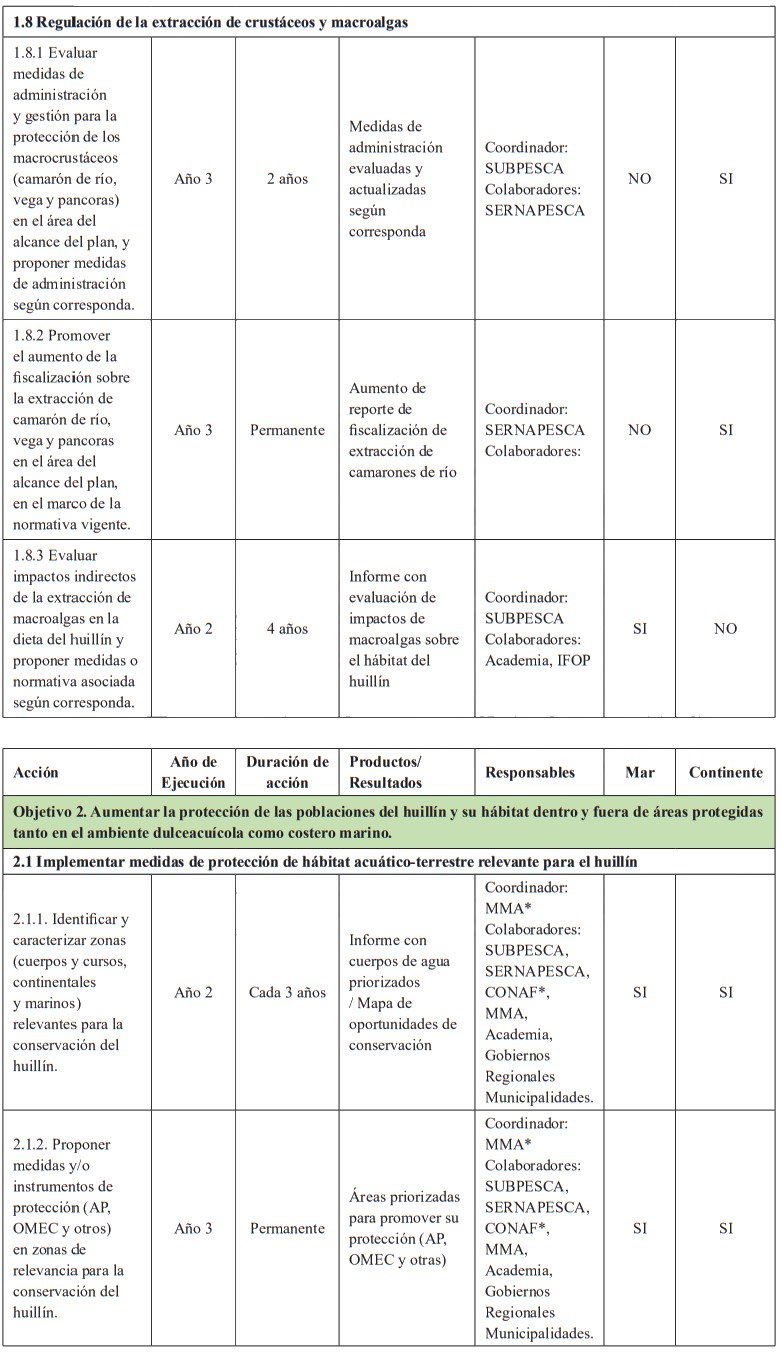
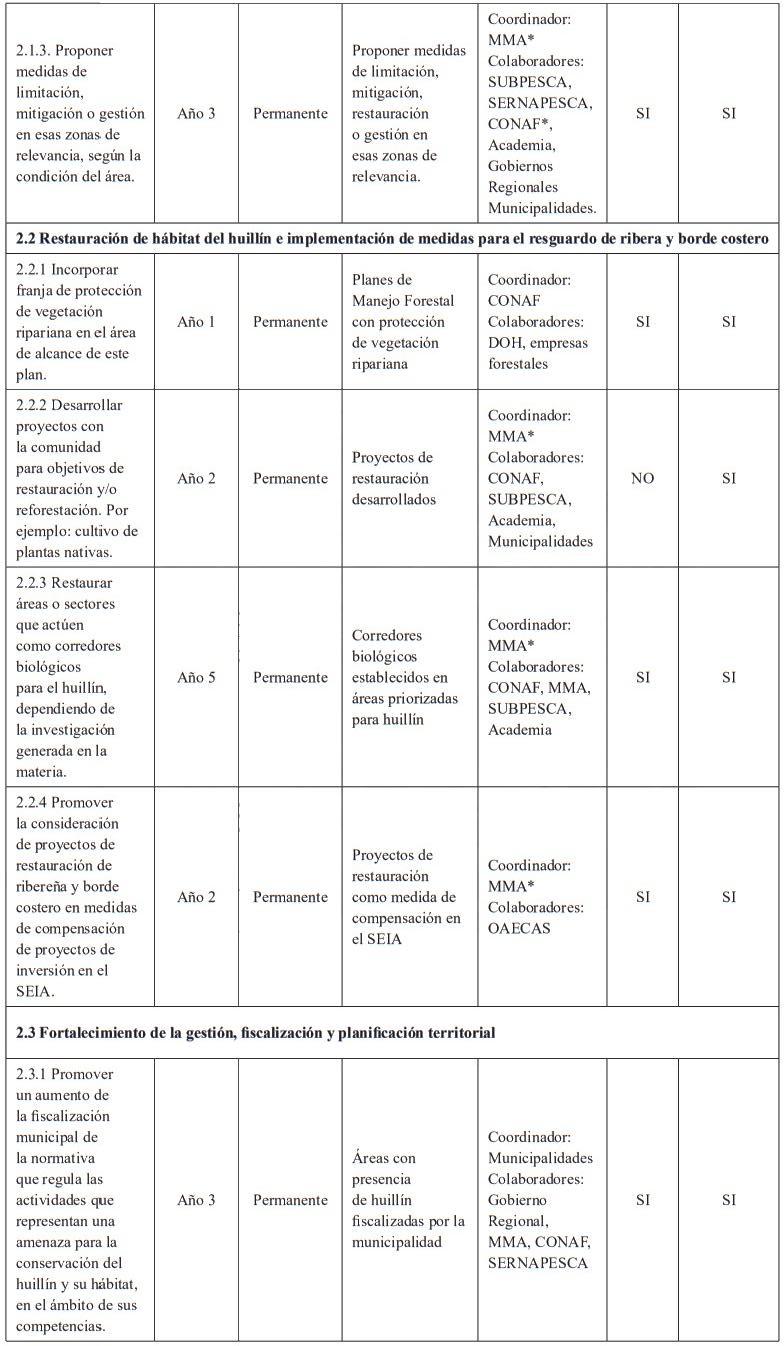
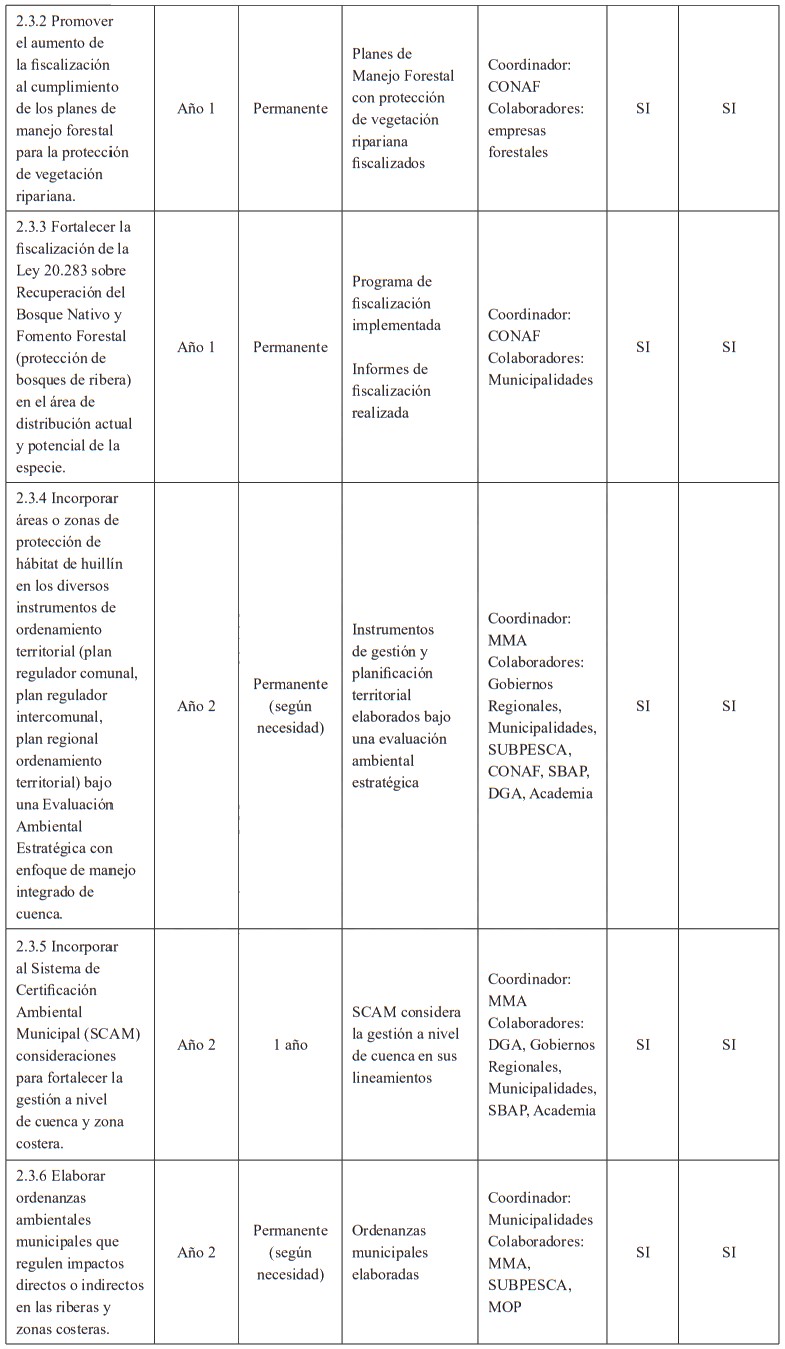
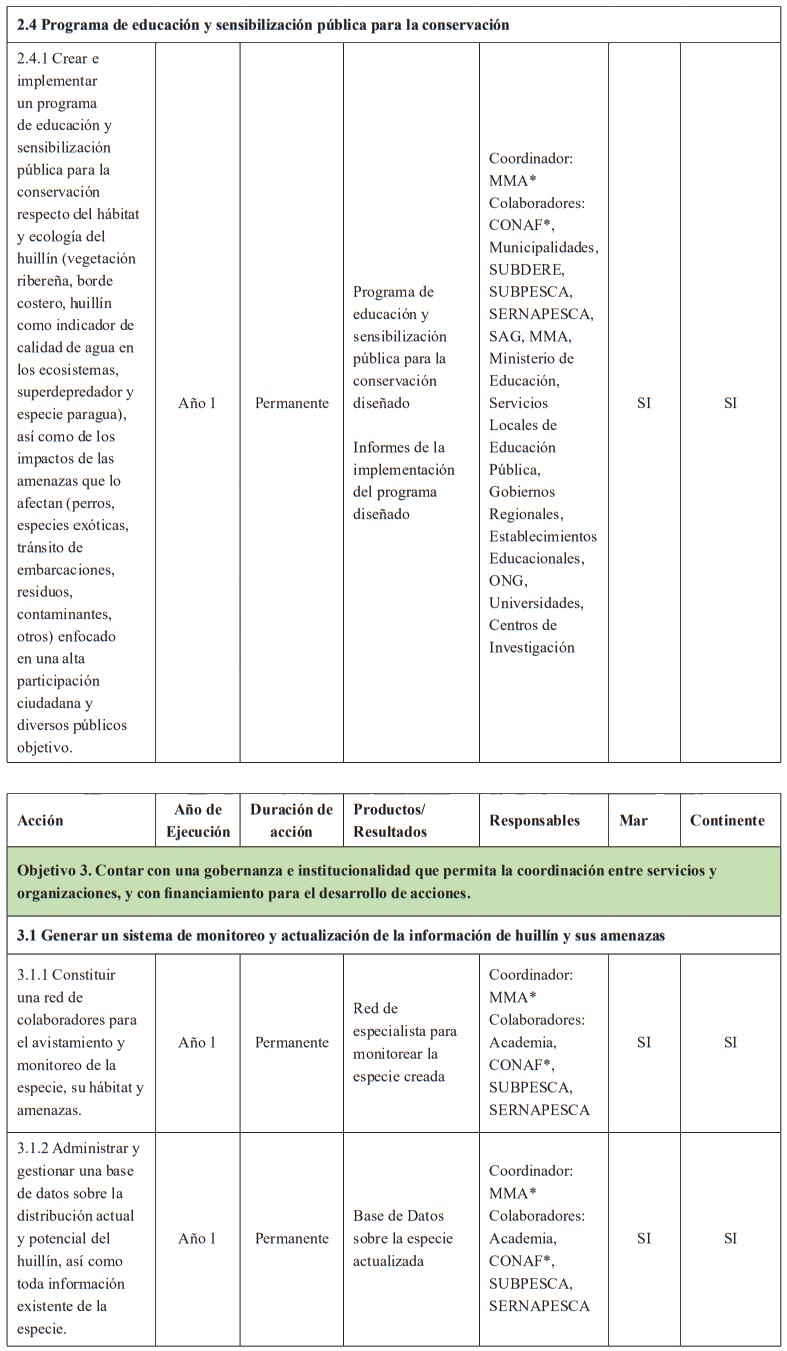
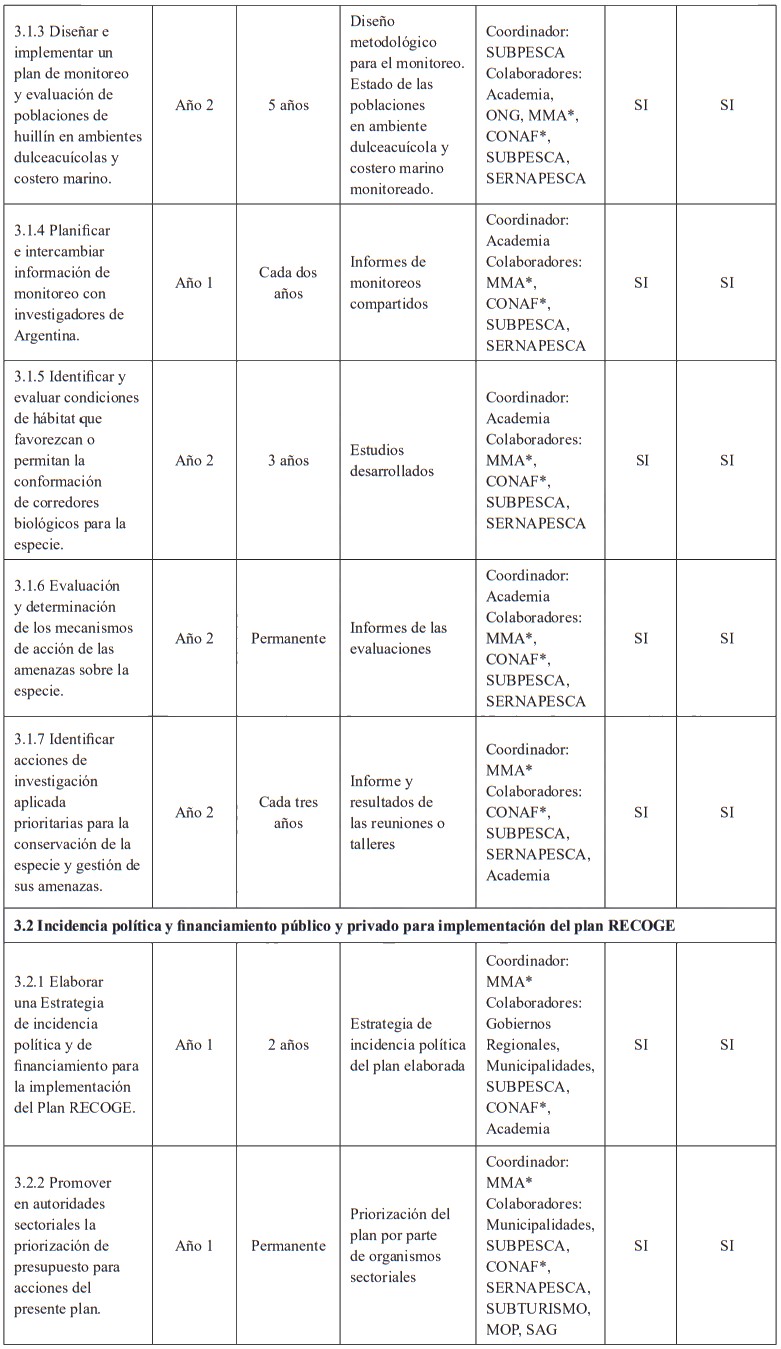
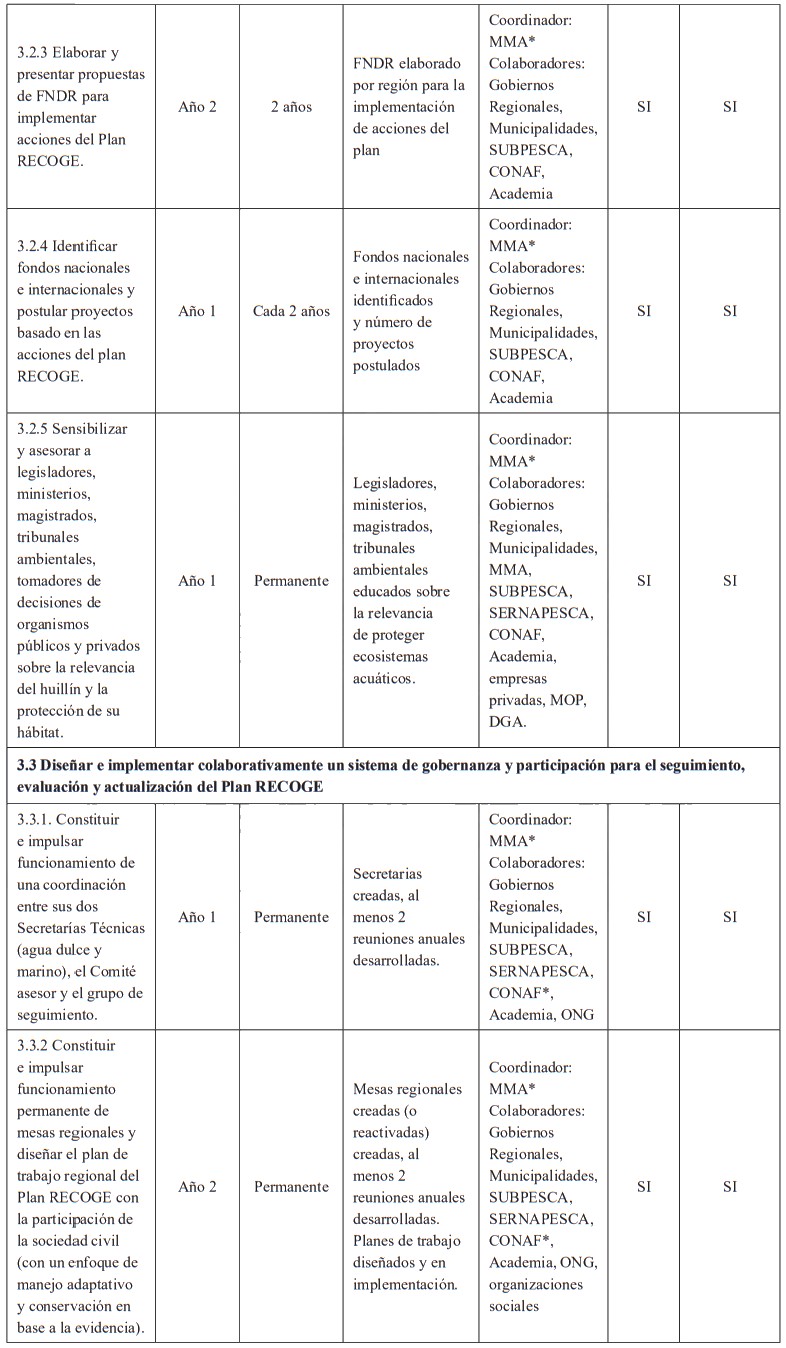
CONAF = Corporación Nacional Forestal, DGA = Dirección General de Aguas, DOH = Dirección de Obras Hidráulicas, FOSIS = Fondo de Solidaridad e Inversión Social, IFOP = Instituto de Fomento Pesquero, INDAP = Instituto Nacional de Desarrollo Agropecuario, INIA = Instituto Nacional de Investigaciones Agropecuarias, MMA = Ministerio del Medio Ambiente, MOP = Ministerio de Obras Públicas, PRODESAL = Programa de Desarrollo Local, SAG = Servicio Agrícola y Ganadero, SERNAPESCA = Servicio Nacional de Pesca y Acuicultura, SERNATUR: Servicio Nacional de Turismo, SUBPESCA = Subsecretaría de Pesca y Acuicultura, SUBTURISMO = Subsecretaría de Turismo, SUBDERE= Subsecretaría de Desarrollo Regional y Administrativo.
Nota: Dada la publicación de la Ley N° 21.600 que crea el Servicio de Biodiversidad y Áreas Protegidas (SBAP) y el Sistema Nacional de Áreas Protegidas, con asterisco (*) se señalan las instituciones cuyo rol o responsabilidad en la acción señalada, será transferida o de responsabilidad del SBAP una vez que éste entre en pleno funcionamiento, conforme a lo establecido en el artículo 5°, letra e), de la mencionada Ley N° 21.600, y sin perjuicio de lo que disponga el reglamento a que hace referencia el inciso segundo del artículo 42 del referido cuerpo legal. Asimismo, se ha considerado el Ministerio del Medio Ambiente como institución colaboradora en aquellas acciones que serán posteriormente coordinadas por el SBAP y en las que posee competencias conforme al artículo 70 de la Ley N° 19.300.
11. Grupo de Seguimiento y proceso de evaluación de la implementación del Plan
El Grupo de Seguimiento tiene como función realizar el seguimiento de las acciones comprometidas para el éxito del plan según lo señalado en el procedimiento y periodos de evaluación de la implementación del Plan, debiendo además, velar por que en la implementación del presente plan se considere, y tenga a la vista, la sinergia con las diversas políticas y estrategias públicas que en materia ambiental se han dictado, promoviendo además la colaboración entre el sector público, privado y la sociedad civil.
El grupo de seguimiento para el Plan de Recuperación, Conservación y Gestión del Huillín está conformado por:
. Representantes del Ministerio del Medio Ambiente
. Representantes de la Subsecretaría de Pesca y Acuicultura
. Representantes del Servicio Nacional de Pesca y Acuicultura
. Representantes de la Corporación Nacional Forestal
. Representantes de la Dirección General de Aguas del Ministerio de Obras Públicas
. Representantes de Obras Hidráulicas del Ministerio de Obras Públicas
. Representantes de CODEFF
. Representantes de Legado Chile.
La estructura del Grupo de Seguimiento está compuesta por dos niveles de coordinación y soporte, uno a nivel general y otro por tipo de ambiente. El ambiente dulceacuícola considera desde la Región de la Araucanía hasta la Región de Aysén y el ambiente costero marino desde la Región de Los Lagos hasta la Región de Magallanes.
La coordinación general del Grupo de Seguimiento estará inicialmente a cargo del Ministerio del Medio Ambiente, a través de la coordinación de la Secretaría Regional Ministerial del Medio Ambiente de Los Lagos, y del Servicio de Biodiversidad y Áreas Protegidas (SBAP), en su reemplazo, una vez que entre en pleno funcionamiento.
En la coordinación por ambiente estará constituido por un grupo público-privado los que darán los principales insumos a la coordinación general para la toma de decisiones para fortalecer la implementación del plan.
Además, se considera un nivel de gobernanza local e implementación, la que será desarrollada por cada región mediante las distintas mesas de trabajo público privadas que están operando a nivel territorial.
El Grupo de Seguimiento, tanto en el nivel general y como por ambiente, sesionará al menos dos veces por año para verificar el cumplimiento de las acciones definidas en el Plan. El cumplimiento de las acciones deberá ser reportadas al Ministerio por parte de el o los órganos, personas jurídicas o personas naturales asignadas para cada acción, para su correcto seguimiento.
La implementación del plan se llevará a cabo en un horizonte de 15 años, periodo durante el cual, el Grupo de Seguimiento evaluará cada 5 años, o según estimen conveniente, replantear aquellas acciones que no estén siendo efectivas para lograr alcanzar las metas propuestas en el Plan.
Una vez que el Servicio de Biodiversidad y Áreas Protegidas se encuentre en pleno funcionamiento y comience a ejercer sus competencias legales asociadas a los planes de recuperación, conservación y gestión de especies, conforme a lo dispuesto en el artículo 5°, letra e), de la ley N° 21.600, el seguimiento del presente plan será de responsabilidad del referido Servicio, sin perjuicio de lo que disponga el reglamento a que se refiere el inciso segundo del artículo 42 del referido cuerpo legal.
12. Costo estimado para la implementación del Plan
La implementación del Plan de Recuperación, Gestión y Conservación de Huillín se estima en US$3.417.652, considerando un horizonte de 15 años. Este se desglosa en US$1.106.673 para el cumplimiento del objetivo N°1, $1.514.459 para el cumplimiento del objetivo N°2, y $796.520 en el caso del Objetivo N° 3. La siguiente tabla presenta los costos del plan por objetivos y por línea de acción.
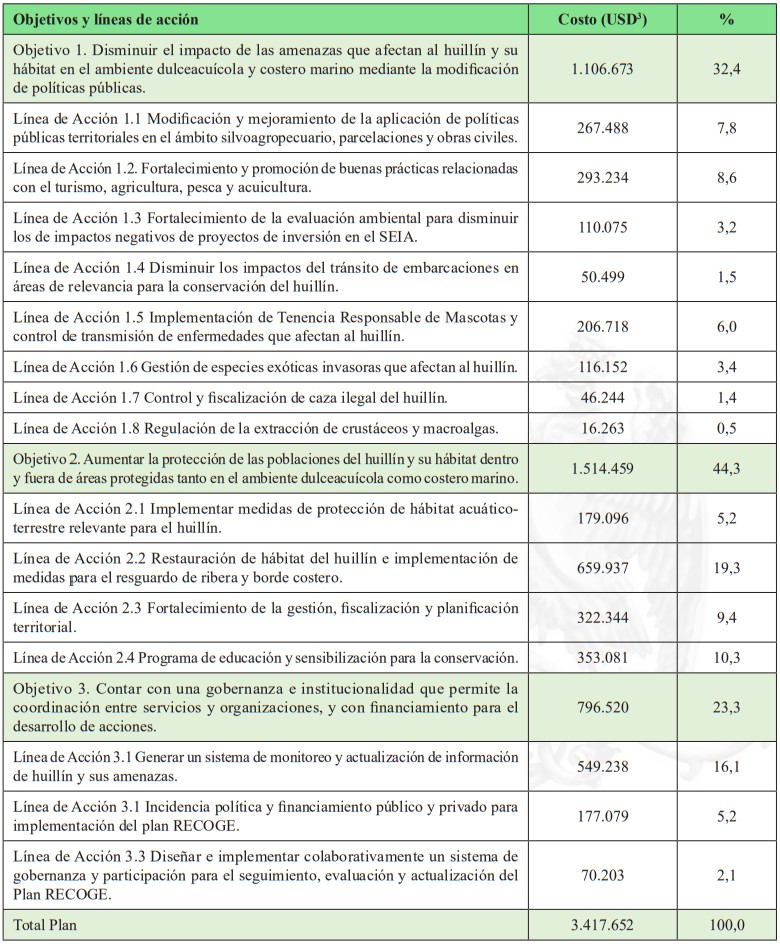
La estimación de costos calcula el valor presente neto para cada una de las acciones definidas por el plan (66 acciones), considerando una tasa de inversión social del 6% definida por el Ministerio de Desarrollo Social (4) para proyectos sociales y un periodo variable dependiendo de los plazos definidos para cada acción que van desde 1 año hasta 15.
Los costos presentados en este Plan corresponden a una evaluación de todas las acciones descritas en el mismo, pudiéndose valorar monetariamente 63 acciones que corresponde al 95% del total.
______________
(3) Promedio dólar norteamericano (USD) entre enero 2022 y mayo 2023. Fuente: https://www.sii.cl/valores_y_fechas/index_valores_y_fechas.html USD= 853,8 pesos chilenos.
(4) Precios Sociales 2017. Ministerio de Desarrollo Social (MDS). 2017.
13. Referencias bibliográficas
Acosta-Jamett G, Chalmers WSK, Cunningham AA, Cleaveland S, Handel IG, Bronsvoort BM de C (2011) Urban domestic dog populations as a source of canine distemper virus for wild carnivores in the Coquimbo region of Chile. Veterinary Microbiology 152(3): 247–257. https://doi.org/10.1016/j.vetmic.2011.05.008
Acosta Jamett G (2015) Perros como riesgo para la salud pública, la ganadería y para la conservación de especies silvestres en Chile: buscando soluciones en la ciencia. Avances en Ciencias Veterinarias 196. https://doi:10.5354/0719-5273.2015.36038
Acuña-Ruz T, Uribe D, Taylor R, Amézquita L, Guzmán MC, Merrill J, Martínez P, Voisin L., Mattar C. (2018). Anthropogenic marine debris over beaches: spectral characterization for remote sensing applications. Remote Sensing of Environment 217: 309-322.
Álvarez R (2013) Levantamiento de información bibliográfica y cartográfica de la especie huillín (Lontra provocax) en la Región de Los Ríos. Informe final. Ministerio del Medio Ambiente. 17 p.
Arismendi I, Soto D, Penaluna B, Jara C, Leal C, León-Muñoz J (2009) Aquaculture, non-native salmonid invasions and associated declines of native fishes in Northern Patagonian lakes. Freshwater Biology 54(5): 1135–1147.
Arismendi I, Penaluna BE, Dunham JB, García de Leaniz C, Soto D, Fleming IA, León-Muñoz J (2014). Differential invasion success of salmonids in southern Chile: Patterns and hypotheses. Reviews in Fish Biology and Fisheries 24(3): 919–941.
Armesto J, Rozzi R, Smith-Ramírez C & Arroyo M (1998) Conservation targets in South American temperate forest. Science, 282:1271-1272.
Bahamonde N & López MT (1963) Decápodos de aguas continentales en Chile. Invest. Zool. Chil. 10: 123-149.
Barbosa A, Real R, Olivero J & Vargas J (2003) Otter (Lutra lutra) distribution modelling at two resolution scales suited to conservation planning in the Iberian Peninsula. Biology Conservation 114: 377-387.
Barros M, Cabezon O, Dubey JP, Almeria S, Ribas MP, Escobar LE, Ramos B & Medina-Vogel G (2018) Toxoplasma gondii infection in wild mustelids and cats across an urban-rural gradient. PLoS ONE 13(6): e0199085. https://doi.org/10.1371/journal.pone.0199085
Barros E & Harcha J (2004) The Cape Horn Biosphere Reserve Initiative: analysis of a challenge for sustainable development in the Chilean Antarctic Province. En: R., Rozzi, F., Massardo, y C. B., Anderson (Eds.). The Cape Horn Biosphere Reserve. A proposal for conservation and tourism to achieve sustainable development at the southern end of the Americas, pp. 27-43, Punta Arenas, Chile: University of Magallanes Press.
Barros M, Medina G, Infante J & Drago F (2020) Distribución, abundancia y riesgos para la conservación del Huillín (Lontra provocax) en la cuenca del río Maullín. Fundación Legado Chile. 33 p.
Basulto S (2003) El largo viaje de los salmones: una crónica olvidada, propagación y cultivo de especies acuáticas en Chile. Editorial Maval Ltda: Santiago, Chile.
Beja PR (1996) An analysis of otter Lutra lutra predation on introduced American crayfish Procambarus clarkii in Iberian streams. J Appl Ecol 33, 1156-1170.
Bonnington C, Gaston KJ & Evans KL (2013) Fearing the feline: domestic cats reduce avian fecundity through trait-mediated indirect effects that increase nest predation by other species. Journal of Applied Ecology 50(1): 15–24. https://doi.org/10.1111/1365-2664.12025
Bouchon D, Souty-Grosset C, Mocquard JP, Chentoufi A & Juchault P (1992) Photoperiodism and seasonal breeding in aquatic and terrestrial Eumala-costraca. Invertebr. Reprod. Dev. 22: 203-212.
Brooker M (1985) The ecological effects of channelization. The Geographical Journal 151(1):63-69
Buschmann AH, Correa JA, Westermeier R, Hernández-González MC & Norambuena R (2001) Red algal farming in Chile: a review. Aquaculture 194: 203-220.
Buschmann H & Fortt A (2005) Efectos ambientales de la acuicultura intensiva y alternativas para un desarrollo sustentable. Ambiente y Desarrollo. Vol 20.
Buschmann AH, Riquelme VA, Hernández-González MC, Varela D, Jiménez JE, Henríquez LA, Vergara, PA, Guiñez R & Filún L (2006) A review of the impacts of salmonid farming on marine coastal ecosystems in the southeast Pacific. ICES Journal of Marine Science 63: 1338-1345.
Buschmann AH, Cabello F, Young K, Carvajal J, Varela DA & Henríquez L (2009) Salmon aquaculture and coastal ecosystem health in Chile: analysis of regulations, environmental impacts and bioremediation systems. Ocean y Coastal Management 52(5): 243-249.
Buschmann AH, Niklitschek EJ & Pereda S (2021). Acuicultura y sus impactos en la conservación de la Patagonia chi En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos pp 367-387. Santiago, Chile: Ediciones Universidad Católica de Chile.
Bustamante R & Castilla JC (1990) Impact of human exploitation on populations of the intertidal southern bull- kelp Durvillaea antarctica (Phaeophyta, Durvilleales) in central Chile. Biological Conservation 52: 205-220.
Caddy JF & Mahon R (1995) Reference points for fisheries management. FAO Fisheries Technical Paper Nº 347. Rome, FAO. 83 p.
Cardillo, M., Purvis, A., Sechrest, W., Gittlemen, J., Bielby, J., Mace, G. (2004). Human population density and extinction risk in the World's carnivores. PloS. Biol. 2: 909-914.
Carmanchahi P, Funes M, Bongiorno M y Monsalvo O (2006). Actualización de la distribución del huillín en la provincia del Neuquén. En: Cassini, M., & Sepúlveda, M. (2006). El Huillín Lontra provocax: Investigaciones sobre una nutria patagónica en peligro de extinción. Buenos Aires: Serie Fauna Neotropical 1, Publicación de la Organización PROFAUNA.
Caro T y O'Doherty G (1999) On the use of surrogate species in conservation biology. Conservation Biology 13: 805-814.
Castilla JC & Durán R (1985) Human exclusion from the rocky intertidal zone of central Chile: the effects on Concholepas concholepas (Mollusca: Gastropoda: Muricidae). Oikos 45: 391-399.
Centro de Energía (2016) Análisis de las condicionantes para el desarrollo hidroeléctrico en las cuencas del Maule, Biobío, Toltén, Valdivia, Bueno, Puelo y Yelcho, desde el potencial de generación a las dinámicas socio-ambientales. Informe final. Facultad de Ciencias Físicas y Matemáticas, Universidad de Chile. 819 p.
Chehébar C (1986) "El Huillín en Argentina". UICN, Boletín del Grupo de Especialistas en Nutrias.; 1: 17-19.
Chomel BB (2014) Emerging and re-emerging zoonoses of dogs and cats. Animals 4: 434–445.
Chopin T, Robinson SMC, Troell M, Neori A, Buschmann AH, Fang J (2008). Multitrophic integration for sustainable marine aquaculture. En: Jørgensen S. E., y B. D. Fath (Eds.), Ecological engineering. Vol. 3, Encyclopedia of Ecology, pp. 2463-2475. Oxford, UK: Elsevier.
Ciancio JE, Pascual MA, Lancelotti J, Rossi CMR & Botto F (2005) Natural colonization and establishment of a Chinook salmon, Oncorhynchus tshawytscha, population in the Santa Cruz River, an Atlantic basin of Patagonia. Environmental Biology of Fishes 74(2): 219–227.
CIS (2019) VIII Encuesta de Medio Ambiente. Centro de Investigación para la Sustentabilidad, Universidad Andrés Bello, Santiago, Chile.
Coe JM & Rogers D (2012) Marine debris: sources, impacts, and solutions. Springer, New York, NY.
Correa-Araneda F, Urrutia J & Figueroa R (2011) Estado del conocimiento y principales amenazas de los humedales boscosos de agua dulce de Chile. Revista Chilena de Historia Natural 84: 325-340.
Correa C, Bravo AP & Hendry AP (2012). Reciprocal trophic niche shifts in native and invasive fish: Salmonids and galaxiids in Patagonian lakes. Freshwater Biology 57(9): 1769–1781.
Correa C & Gross M (2008) Chinook salmon invade southern South America. Biological Invasions 10: 615-639.
CPPS/PNUMA (2007) Memorias del Taller de Trabajo sobre el Impacto de las Actividades Antropogénicas en Mamíferos Marinos en el Pacífico Sudeste. Bogotá, Colombia, 28 al 29 de noviembre de 2006. Guayaquil, Ecuador. 98 p.
Druehl LD & Breen D (1986) Some ecological effect of harvesting Macrocystis integrifolia. Botanica Marina 29: 97-103.
Dubey JP (2010) Toxoplasmosis en animales y humanos. 2a ed. CRC Press. Boca Ratón, FL.
Duplaix N & Savage M (2018) The Global Otter Conservation Strategy. IUCN/SSC Otter Specialist Group, Salem, Oregon, USA For individual authors, this is an example of the proper citation: Loy, A. (2018) Eurasian otter, In: Duplaix, N. and M. Savage, editors, Global Otter Conservation Strategy, IUCN Otter Specialist Group.
Echeverría C, Coomes D, Salas J, Rey-Benayas J & Lara A (2006) Rapid deforestation and fragmentation of chilean temperate forest. Biological Conservation 130:481-494.
Faúndez M (2020) Principales amenazas para la conservación del hábitat del huillín en Chile. Universidad de Chile. 51p.
Figueroa R, Suarez ML, Andreu A, Ruiz VH & Vidal-Abarca MR (2009) Caracterización ecológica de humedales de la zona semiárida en Chile Central. Gayana 73: 76-94.
Fleishman E, Murphy D & Blair R (2001) Selecting effective umbrella species. Cons. Biol. Pract. 2: 17-23.
Foster MS & Bariloti DC (1990) An approach to determining the ecological effects of seaweed harvesting: a summary. Hydrobiologia 204/205: 15 - 16.
Gompper ME (2014) Free-ranging dogs and wildlife conservation (M.E. Gommper Ed). Oxford University Press.
Goodwin P, Jorde K, Meier C & Parra O (2006) Minimizing environmental impacts of hydropower development: transfering lessons from the past projects to a proposed strategy for Chile. Journal of Hydroinformatics 8: 253-270.
Górski K, González JF, Vivancos A, Habit EM & Ruzzante DE (2017) Young of-the-year Coho Salmon Oncorhynchus kisutch recruit in fresh waters of remote Patagonian fjords in southern Chile (51° S). Biological Invasions 19(4): 1127–1136.
Granados D, Hernández M & López G (2006) Ecología de las zonas ribereñas. Revista Chapingo. Serie Ciencias Forestales y del Ambiente 12(1): 55-69
Guala C, Veloso K, Farías A & Sariego F (2021) Caracterización del desarrollo turístico asociado a las áreas silvestres protegidas de la Patagonia chi. En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos, pp 575-598. Santiago, Chile: Ediciones Universidad Católica de Chile.
Guevara G, Reinoso G, García JE, Franco LM, García LJ, Yara DC, Briñez N, Ocampo M, Quintana MI, Pava DY, Flórez NY, Ávila MF, Hernández EE, Lozano LA, Guapucal M, Borrero DA & Olaya EJ (2008) Aportes para el análisis de ecosistemas fluviales: una visión desde ambientes ribereños. Revista Tumbaga 3: 109-127.
Habit E & Victoriano P (2012) Composición, origen y valor de conservación de la Ictiofauna del Río San Pedro (Cuenca del Río Valdivia, Chile). Gayana 76: 10-23.
Habit E, Belk M, Tuckfield C & Parra O (2006) Response of the fish community to human-inducedchanges in the Biobío River i n Chile. Freshwater Biology 51: 1–11.
Habit E, González J, Ruzzante DE & Walde SJ (2012) Native and introduced fish species richness in Chilean Patagonian lakes: inferences on invasion mechanisms using salmonid-free lakes. Diversity and Distributions 18(12): 1153–1165.
Habit E, Górski K, Alò D, Ascencio E, Astorga A, Colin N, Contador T, de los Ríos P, Delgado V, Dorador C, Fierro P, García K, Parra O, Quezada- Romegialli C, Ried B, Rivera P, Soto-Azat C, Valdovinos C, Vera-Escalona I & Woelfl S (2019) Biodiversidad de ecosistemas de agua dulce. En: Marquet, P.A., Altamirano, A., Arroyo, M. T. K., Fernández, M., Gelcich, S., Górski, K., Habit, E., Lara, A., Maass, A., Pauchard, A., Pliscoff, P., Samaniego, H., Smith-Ramírez, C. (Eds.) (2019). Biodiversidad y cambio climático en Chile: evidencia científica para la toma de decisiones. Informe de la mesa de biodiversidad. Santiago, Chile: Comité Científico COP25; Ministerio de Ciencia, Tecnología, Conocimiento e Innovación. Obtenido de: http://www.minciencia.gob.cl/comitecientifico
Hauenstein E, González M, Pena-Cortes F, & Munoz-Pedreros A (2005) Diversidad vegetal en humedales costeros de la Región de la Araucanía. En: Historia Biodiversidad y Ecología de los Bosques Costeros de Chile, pp 197-205.
Hildebrand JA (2009) Anthropogenic and natural sources of ambient noise in the ocean. Marine Ecology Progress Series 395: 5-20.
Hinojosa IA & Thiel M (2009) Floating marine debris in fjords, gulfs, and channels of southern Chile. Marine Pollution Bulletin 58: 341-350.
Holdich MD (1993) A review of astaciculture: freshwater crayfish farming. Aquat. Living Res. 6(3): 307-317. https://doi.org/10.1007/s13280-018-1066-3
Hucke-Gaete R, Haro D, Torres-Florez JP, Montecinos Y, Viddi FA, Bedriñana L & Ruiz J (2013) A historical feeding ground for humpback whales in the eastern south Pacific revisited: the case of northern Patagonia, Chile. Aquatic Conservation: Marine and Freshwater Ecosystems 23: 858-867.
Hucke-Gaete R, Viddi FA & Simeone A (2021) Aves y mamíferos marinos de la Patagonia chi: especies focales para la conservación de los ecosistemas marinos. En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos, pp. 289-320. Santiago, Chile: Ediciones Universidad Católica de Chile.
Ibarra J, Habit E, Barra R & Solís K (2011) Juveniles de salmón Chinook (Oncorhynchus tshawytscha Walbaum, 1792) en ríos y lagos de la patagonia chi. Gayana (Concepción) 75(1): 17–25.
ICAM (2007) Humane dog population management guidance. International Companion Animal Management Coalition. Disponible en: https://rpawe.oie.int/fileadmin/uploadmaterials/humane_dog_population_management_guidance_english.pdf
Iriarte A & Jaksic F (2012) Los Carnívoros de Chile. Santiago: Ediciones Flora & Fauna Chile y CASEB. P.U. Católica de Chile.
Iriarte JA & Jaksic FM (1986) Fur trade in Chile: An overview of seventy-five years of export data (1910-1984). Biological conservation 38(3): 243-253.
Jackson D, Peres-Neto P & Olden J (2001) What controls who is where in freshwater fish communities the roles of biotic, abiotic, and spatial factors. Canadian Journal of Fisheries and Aquatic Sciences 58(1): 157-170.
Jara C (1977) Aegla rostrata n. sp., (Decapoda, Aeglidae), nuevo crustáceo dulceacuícola del Sur de Chile. Studies on Neotropical Fauna and Environment 12: 165-176.
Jara CG, Rudolph EH & González ER (2006) Estado de conocimiento de los malacostráceos dulceacuícolas de Chile. Gayana (Concepción) 70(1). doi:10.4067/s0717-65382006000100008
Kirk C, Rozzi R & Gelcich S (2018) El turismo como una herramienta para la conservación del elefante marino del sur (Mirounga leonina) y sus hábitats en Tierra del Fuego, Reserva de la Biósfera Cabo de Hornos, Chile. Magallania (Chile) 46(1): 65-78.
Kreuder C, Miller MA, Jessup DA, Lowenstine LJ, Harris MD, Ames JA, Carpenter TE, Conrad PA & Mazet JAK (2003) Patrones de mortalidad en nutrias marinas del sur (Enhydra lutris nereis) de 1998 a 2001. Revista de Enfermedades de la Vida Silvestre 39(3): 495-509. pmid:14567210.
Kruuk H (1995) Wild otters: predation and populations. Oxford University Press.
Laist DW (1997) Impacts of marine debris: entanglement of marine life in marine debris including a comprehe nsive list of species with entanglement and ingestion records. En: J. M. Coe y D. B. Rogers (Eds.), Marine debris: sources, impacts, and solutions, pp. 99-139. New York, USA: Springer.
Larivière S (1999) "Mustela vison". Archivos de especies de mamíferos 608: 1-9.
Larson G, Karlsson EK, Perri A, Webster MT, Ho SYW, Peters J, Stahl PW, Piper PJ, Lingaas F, Fredholm M, Comstock KE, Modiano JF, Schelling C, Agoulnik AI, Leegwater PA, Dobney K, Vigne JD, Vilà C, Andersson L, Lindblad-Toh K (2012) Rethinking dog domestication by integrating genetics, archeology, and biogeography. Proc. Natl Acad. Sci. 109: 8878 8883.
Loss SR, Will T & Marra PP (2013) The impact of free-ranging domestic cats on wildlife of the United States. Nature Communications 4 (1396): 1396–1397. https://doi.org/10.1038/ncomms2380
Lunney M, Jones A, Stiles E & Waltner-Toews D (2011) Assessing human-dog conflicts in Todos Santos, Guatemala: bite incidences and public perception. Preventive Veterinary Medicine 102(4): 315–320.
Marticorena F (2009) A pura memoria: Conocimientos y significados de la naturaleza en las localidades de Melinka y Repollal, litoral norte de la región de Aysén. Universidad Austral de Chile. 195 p.
Martinic M (2005) De la Trapananda al Aysén: Una mirada reflexiva sobre el acontecer de la Región de Aysén desde la prehistoria hasta nuestros días. 1st ed. Santiago: Pehuen.
Medina G (1991) The Status of the huillín (Lutra provocax) in Chile. Preliminary information on the current situation of populations, habitat conditions and illegal trade. In Reuther, C; Röchert, R (Eds): Proceedings of the V. International Otter Colloquium. Hankensbüttel. Habitat 6:63-69.
Medina G (1996a). Conservation and status of Lutra provocax in Chile. Pacific Conservation Biology 2: 414-419.
Medina G (1996b) Status and protection of southern river otter (Lutra provocax) in central south of Chile. Filial Valdivia, Project FZS 1104/1990. Comité Nacional pro Defensa de la Fauna y Flora (CODEFF).
Medina G (1997) A comparison of the diet and distribution of southern river otter (Lutra provocax) and mink (Mustela vison) in Southern Chile. Journal of Zoology, London 242: 291-297.
Medina G (1998) Seasonal variation and changes in the diet of southern river otter in different freshwater habitats in Chile. Acta Theriol (Warsz) 43:285-292.
Medina-Vogel G (2001) Expectations for the Latin American region from the Otter Action Plan. In: Reuther, C.; Santiapillai, C. (eds). How to implement the Otter Action Plan? Habitat 13:22-23.
Medina-Vogel G, Kaufman V, Monsalve R & Gómez V (2003) The influence of riparian vegetation woody debris, stream morphology and human activity on the use of rivers by southern river otters in Lontra provocax in Chile. Oryx 37:422-430.
Medina G, Bartheld JL & Sepúlveda M (2004) El huillín o nutria de río: Antecedentes generales y bases para su conservación en las cuencas del río Toltén y Queule, IX Región. CODEFF-FZS, Chile.
Medina-Vogel G (2004) Estrategia regional para la conservación del huillín (Lontra provocax) en Chile. En: Historia, biodiversidad y ecología de los bosques de la cordillera de la costa de Chile. Eds. C Smith Ramírez, J Armesto & C Valdovinos. Editorial Universitaria, Santiago, Chile.
Medina-Vogel G, Boher F, Flores G, Santibañez A & Soto-Azat C (2007) Spacing behavior of Marine otters (Lontra felina) in relation to land refuges and fishery waste in Central Chile. Journal of Mammalogy. vol 88, p. 487-494.
Medina G & Gonzalez C (2008) Habitat use and diet of endangered southern river otter Lontra provocax in a predominantly palustrine wetland in Chile. Wildlife Biol. 14(2):211–220. doi:10.2981/0909- 6396(2008)14[211:HUADOE]2.0.CO;2.
Millán J, Cabezón O, Pabón M, Dubey JP & Almería S (2009) Seroprevalencia de Toxoplasma gondii y Neospora caninum en gatos salvajes (Felis silvestris catus) en Mallorca, Islas Baleares, España. Parasitología Veterinaria 165(3): 323-326.
Miller MA, Gardner IA, Kreuder C, Paradies DM, Worcester KR, Jessup DA, Dodd E, Harris MD, Ames JA, Packham AE & Conrad PA (2002) La escorrentía costera de agua dulce es un factor de riesgo para la infección por Toxoplasma gondii de nutrias marinas del sur (Enhydra lutris nereis). Revista Internacional de Parasitología 32(8): 997-1006. pmid:12076629
Mims M & Olden J (2012) Life history theory predicts fish assemblage response to hydrologic regimes. Ecology 93: 35–45.
MINSAL (2017) Encuesta de Calidad de Vida y Salud (ENCAVI) 2015 – 2016. Ministerio de Salud. División de Planificación Sanitaria. Departamento de Epidemiología Unidad de Vigilancia de Enfermedades No Transmisibles, República de Chile.
Molinet C & Niklitschek EJ (2021) Pesquerías y conservación marina en la Patagonia chi. En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos, pp. 345-366. Santiago, Chile: Ediciones Universidad Católica de Chile.
Montecino-Latorre D & San Martín W (2018) Evidence supporting that human-subsidized free-ranging dogs are the main cause of animal losses in small-scale farms in Chile. Ambio 1972: 1–11.
Morales AI & Sobenes CP (2018) Evaluación de la calidad de un tramo de río urbano intervenido y selección de un paso para peces, Región del Biobío, Chile. Información Tecnológica 29(2): 155-164. http://dx.doi.org/10.4067/S0718-07642018000200155
Mori E, Menchetti M, Camporesi A, Cavigioli L, Tabarelli de Fatis K & Girardello M (2019) License to kill? Domestic cats affect a wide range of native fauna in a highly biodiverse Mediterranean country. Frontiers in Ecology and Evolution 7: 477. http://doi10.3389/fevo.2019.00477
Morita K & Yamamoto S (2002) Effects of Habitat Fragmentation by Damming on the Persistence of Stream-Dwelling Charr Populations. Conservation Biology 16(5): 1318-1323.
Morita K & Yokota A (2002) Population viability of stream-resident salmonids after habitat fragmentation: a case study with white-spotted charr (Salvelinus leucomaenis) by an individual based model. Ecological Modelling 155: 85–94.
Moseby KE, Peacock DE & Read JL (2015) Catastrophic cat predation: a call for predator profiling in wildlife protection programs. Biological Conservation 191: 331–340. https://doi.org/10.1016/j.biocon.2015.07.026
Niklitschek EJ, Soto D, Lafon A, Molinet C & Toledo P (2013) Southward expansion of the Chilean salmon industry in the Patagonian fjords: main environmental challenges. Reviews in Aquaculture 5(3): 72-195.
Ochoa C (2007) Usos conflictivos del agua: Búsqueda de soluciones. Dyna 74(152): 51-61.
OIE/WSPA (2017) The Stray Dog Problem. Terrestrial Animal Health Code, World Organization for Animal Health - World Society for the Protection of Animals.
Olavarría C, Álvarez R, Correa R, Badilla M & Carrasco H (2006) Impactos reales y potenciales de las actividades antropogénicas sobre mamíferos marinos en Chile: nutrias. Memorias del Taller de Trabajo sobre el Impacto de las Actividades Antropogénicas en Mamíferos Marinos en el Pacífico Sudeste. Bogotá, Colombia. 100 p.
Ortiz-Sandoval JJ, Górski K, González-Díaz A & Habit E (2015) Limnologica Trophic scaling of Percichthys trucha (Percichthyidae) in monospecific and multispecific lakes in western Patagonia. Limnologica 53: 50–59.
Owen, C. (1998). Hydrology and history: land use changes and ecological responses in an urban wetland. Wetlands Ecology and Management 6(4): 209-219.
Peña-Cortés F, Gutiérrez P, Rebolledo G, Escalona M, Hauenstein E, Bertrán C, Schlatter R & Tapia J (2006) Determinación del nivel de antropización de humedales como criterio para la planificación ecológica de la cuenca del lago Budi, IX Región de La Araucanía, Chile. Revista de Geografía Norte Grande 36: 75-91.
Pérez JR, Celada JD, Carral JM, Sáez-Royuela M, Muñoz C & Sierra A (1997) Métodos básicos de cría de astácidos en Europa. Invest. Agrop. San. Anim. 12(1-3): 86-97.
Pérez S (2017) Efectos potenciales de la presencia de salmones juveniles sobre la dieta de peces nativos de lagos y estuarios de los fiordos patagónicos. Tesis para optar al grado de Magíster en Ecología Marina. Facultad de Ciencias, Universidad Cató lica de la Santísima Concepción, Concepción, Chile. 89 p.
Pliscoff P & Fuentes-Castillo T (2011) Modelación de la distribución de especies y ecosistemas en el tiempo y en el espacio: una revisión de las nuevas herramientas y enfoques disponibles. Revista de Geografía del Norte Grande 48: 61-79.
Quiñones R, Fuentes M, Montes RM, Soto D, León-Muñoz J (2019) Environmental issues in Chilean salmon farming: a review. Reviews in Aquaculture 11: 375-402.
Randolph J (2004) Environmental Land Use Planning and Management. Island Press, Washington.
Reid B, Astorga A, Madriz I & Correa C (2021) Conservación de los ecosistemas dulceacuícolas de la Patagonia occidental austral. En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos, pp. 429-471. Santiago, Chile: Ediciones Universidad Católica de Chile.
Ribeiro S, Viddi FA, Cordeiro JL & Freitas TRO (2007) Fine-scale habitat selection of Chilean dolphins (Cephalorhynchus eutropia): interactions with aquaculture activities in southern Chiloé island, Chile. Journal of the Marine Biological Association of the United Kingdom 87: 119-128.
Rodríguez-Jorquera I & Sepúlveda M (2011) Trophic spatial variation in the souther river otter (Lontra provocax) in freshwater habitats, Chile. Proceedings of Xth International Otter Colloquium, IUCN Otter Spec. Group Bull. 28A: 70 – 75.
Romero FI, Cozano MA, Gangas RA & Naulin PI (2014) Zonas ribereñas: protección, restauración y contexto legal en Chile. Bosque 35(1): 3-12.
Rossi CMR, Pascual MA, Marchant EA, Basso N, Ciancio JE, Mezga B & Ernst-Elizalde B (2012) The invasion of Patagonia by Chinook salmon (Oncorhynchus tshawytscha): inferences from mitochondrial DNA patterns. Genetica 140(10–12): 439–453.
Rozzi R, Rosenfeld S, Armesto JJ, Man silla A, Núñez-Ávila M & Massardo F (2021) Conexiones ecológicas a través de la interfaz marino-terrestre en la Patagonia chi. En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos, pp. 391-425. Santiago, Chile: Ediciones Universidad Católica de Chile.
Rudolph EH (2002) Sobre la biología del camarón de río Samastacus spinifrons (Philippi, 1882) (Decapoda, Parastacidae). Gayana 66(2): 147-159.
Rudolph EH & Crandall KA (2007) A new species of burrowing crayfish Virilastacus retamali (Decapoda, Parastacidae) from the southern Chile peatland. J. Crust. Biol. 27(3): 502-512.
Schmitt WL (1942) The species of Aegla, endemic South American fresh-water crustaceans. Proceedings of the United States National Museum 91(3132):431-520, figs. 40-64, pls.25-28.
Sepulveda M, Bartheld JL, Monsalvec R, Gómez V, Medina-Vogel G (2007) Habitat use and spatial behaviour of the endangered Southern River otter (Lontra provocax) in riparian habitats of Chile: Conservation implications. Biological Conservations 140: 329 -338.
Sepúlveda M, Bartheld J, Meynard C, Benavides M, Astorga C, Parra D & Medina-Vogel G (2009) Landscape features and crustacean prey as predictors of the Southern river otter distribution in Chile. Animal Conservation 12:522-530.
Sepúlveda MA, Muñoz C, Rosenfeld C, Jara R, Pelican KM & Hill D (2011) Toxoplasma gondii in feral American minks at the Maullín river, Chile. Veterinary Parasitology 175: 60-65.
Sepúlveda MA, Singer RS, Silva-Rodríguez EA, Eguren A, Stowhas P & Pelican K (2014) Invasive American mink: linking pathogen risk between domestic and endangered carnivores. Ecohealth 11(3):409-19.
Sepúlveda M, Valenzuela A, Pozzi C, Medina-Vogel G & Chehébar C (2015) Lontra provocax. The UICN Red List of Threatened Especies 2015: eT12305A21938042.
Shumway SE (2011) Shellfish aquaculture and the environment. UK: Wiley-Blackwell.
Sielfeld W (1989) Sobreposición de nicho y patrones de distribución de Lutra felina y L. provocax (Mustelidae, Carnivora) en el medio marino de Sudamérica Austral. Ans. Mus. Hist. Nat. Valparaíso 20:103-108.
Sielfeld W (1990) Características del hábitat de Lutra felina (Molina) y L. provocax Thomas (Carnivora, Mustelidae) en Fuego Patagonia. Invest. Cient. y Tec., Serie: Ciencias del Mar 1: 30-36.
Sielfeld W (1992) Densidad y abundancia de Lutra felina (Molina, l782) y L. provocax Thomas, 1908 en el litoral de Chile austral. Invest. Cient. y Tec., Serie: Ciencias del Mar 2: 3-11.
Sielfeld W (2006) Biología y conservación del huillín en los canales magallánicos de Chile. Pp. 46–53. In: Cassini., M & M. Sepúlveda (eds.). El huillín Lontra provocax. Investigaciones sobre una nutria patagónica amenazada de extinción. Serie Fauna Neotropical 1. Ediciones PROFAUNA, Buenos Aires, República Argentina. 162 pp.
Sielfeld W (2014) Huillín y chungungo en Chile Austral (1979-2014). Centro de Investigación en Medio Ambiente (CENIMA), Universidad Arturo Prat, Chile, Informe Técnico, 240 pp.
Sielfeld W & Castilla J (1999) Estado de conservación y conocimiento de las nutrias en Chile. Estudios Oceanológicos 18: 69-79.
Silva-Rodríguez EA, Verdugo C, Aleuy OA, Sanderson JG, Ortega-Solís GR, Osorio-Zúñiga F & González-Acuña D (2009) Evaluating mortality sources for the vulnerable pudu Pudu puda in Chile: abril 2021 – Página 22 implications for the conservation of a threatened deer. Oryx 44(1): 97–103. https://doi.org/10.1017/S0030605309990445
Silva-Rodríguez EA, Ortega-Solís GR & Jiménez JE (2010) Conservation and ecological implications of the use of space by chilla foxes and free-ranging dogs in a human-dominated landscape in southern Chile. Austral Ecology 35(7): 765–777. https://doi.org/10.1111/j.1442-9993.2009.02083.x
Simpson E (1870) Exploraciones hechas por la Corbeta Chacabuco al mando del Capitán de Fragata don Enrique M. Simpson en los Archipiélagos de Guaitecas, Chonos i Taitao. Santiago: Imprenta Nacional.
Smith VH, Tilman GD & Nekola JC (1999) Eutrophication: impacts of excess nutrient inputs on freshwater, marine, and terrestrial ecosystems. Environmental Pollution 100: 179-196.
Soto D, Arismendi I, Prinzio CDI & Jara F (2007) Establishment of Chinook salmon (Oncorhynchus tshawytscha) in Pacific basins of southern South America and its potential ecosystem implications. Revista Chilena de Historia Natural 80(1): 81–98.
Soto D, Jara F & Moreno C (2001) Escaped Salmon in the Inner Seas, Southern Chile: Facing Ecological and Social Conflicts Published by Ecological Society of America Escaped Salmon In The Inner Seas, Southern Chile: Facing Ecological And Social Conflicts. Ecological Society of America 11(6): 1750–1762.
SUBPESCA (2018) Programa de manejo de salmón Chinook (Oncorhynchus tshawytscha) en la cuenca del Río Toltén. Dirección Zonal de Pesca y Acuicultura, La Araucanía – Los Ríos, Chile. 46 p.
Suski C & Cooke S (2007) Conservation of aquatic resources through the use of freshwater protected areas: opportunities and challenges. Biodiversity Conservation 16: 2015-2029.
Svensson G & Farías A (2010) Uso de fragmentos de bosque y consumo de fauna nativa por perros y gatos domésticos en un agroecosistema de Chiloé (X región, Chile). Escuela de Ciencias Veterinarias, Licenciatura, Universidad Austral de Chile. 73 pp.
Tecklin D, Farías A, Peña MP, Gélvez X, Castilla JC, Sepúlveda M, Viddi FA & Hucke- Gaete R (2021) Protección costero-marina en la Patagonia chi: situación presente, avances y desafíos. En: J. C., Castilla, J. J., Armesto y M. J., Martínez-Harms (Eds.), Conservación en la Patagonia chi: evaluación del conocimiento, oportunidades y desafíos, pp. 259-288. Santiago, Chile: Ediciones Universidad Católica de Chile.
Tenter AM, Heckeroth AR & Weiss LM (2000) Toxoplasma gondii: de animales a humanos. Revista Internacional de Parasitología.; 30(12): 1217-1258.
Torrejón F, Bizama G, Araneda A, Aguayo M, Bertrand S & Urrutia R (2013) Descifrando la historia ambiental de los archipiélagos de Aysén, Chile: El influjo colonial y la explotación económica-mercantil republicana (siglos XVI-XIX). Magallania 41: 29-52.
Valenzuela AEJ (2011) Ecología y distribución del visón americano (Neovison vison) en Tierra del Fuego: efectos de este predador exótico en la fauna nativa. Tesis de Doctorado, Universidad de Buenos Aires, Buenos Aires, Argentina.
VanWormer E, Fritz H, Shapiro K, Mazet JA & Conrad PA (2013) Moléculas para modelar: ooquistes toxoplasma gondii en la interfaz hombre-animal-ambiente. Inmunología Comparada, Microbiología y Enfermedades Infecciosas 6(3): 217–31. pmid:23218130
Vásquez JA (1995) Ecological effects of brown seaweed harvesting. Botanica Marina 38: 251- 257.
Vásquez JA & Santelices B (1984) Comunidades de macroinvertebrados en discos adhesivos de Lessonia nigrescens Bory (Phaeophyta) en Chile central. Revista Chilena de Historia Natural 57: 131-154.
Vásquez JA, Piaget N, Tala F, Vega JMA, Bodini A, Morales S, Jorquera L, Sáez C & Muñoz P (2010) Evaluación de la biomasa de praderas naturales y prospección de potenciales lugares de repoblamiento de algas pardas en la costa de la XV, I y II regiones. Informe Final Proyecto FIP 2008-38.
Vianna JA, Medina-Vogel G, Chehébar C, Sielfeld W, Olavarría C & Faugeron S (2011) Filogeografía de la nutria patagónica Lontra provocax: ¿divergencia adaptativa con el hábitat marino o firma de refugios glaciares del sur? Biología Evolutiva de BMC 11(1), 1.
Vitousek PM, Mooney HA, Lubchenko J & Melillo JM (1997) Human domination of Earth's ecosystems. Science 277: 494-499.
Vucinic M & Vucicevic M (2019) Children are victims of dog bites due to irresponsible dog ownership, parenthood and managers of school institutions in Serbia. Journal of Veterinary Behavior 30: 61-68. https://doi.org/10.1016/j.jveb.2018.12.005
Williams JG, Smith SG, Zabel RW, Muir WD, Scheuerell MD, Sandford BP, Marsh DM., McNatt RA & Achord S (2005) Effects of the federal Columbia River power system on salmonid populations. U.S. Dept. Commer., NOAA Tech. Memo.NMFS-NWFSC-63, 150 p.
Woodroffe R (1998) Edge effects and the extinction of populations inside protected areas. Science 280: 2116-2128.
Woodroffe R & Ginsberg J (2000) Ranging behaviour and vulnerability to extinction in carnivores. Conservation Biology Series - Cambridge, pp 125-140.
Young JK, Olson KA, Reading RP, Amgalanbaatar A & Berger J (2011) Is wildlife going to the dogs? Impacts of feral and free-roaming dogs on wildlife populations. Bioscience 61: 125–132. http://doi.org/10.1525/bio.2011.61.2.7
Anótese, tómese razón y publíquese.- GABRIEL BORIC FONT, Presidente de la República.- María Heloísa Rojas Corradi, Ministra del Medio Ambiente.- Nicolás Grau Veloso, Ministro de Economía, Fomento y Turismo.- Esteban Valenzuela Van Treek, Ministro de Agricultura.
Lo que transcribo para Ud. para los fines que estime pertinentes.- Maximiliano Proaño U., Subsecretario del Medio Ambiente.
CONTRALORÍA GENERAL DE LA REPÚBLICA
División Jurídica
Cursa con alcance el decreto N° 36, de 2024, del Ministerio del Medio Ambiente
N° E202048/2025.- Santiago, 26 de noviembre de 2025.
Esta Contraloría General ha dado curso al decreto singularizado en el epígrafe, que Aprueba Plan de Recuperación, Conservación y Gestión del Huillín (Lontra provocax), pero es necesario hacer presente que, al tenor de lo previsto en los preceptos legales que regulan la materia, el referido plan busca fortalecer la recuperación, conservación y gestión de dicha especie, contemplando las políticas a seguir en dicho ámbito, y su contenido no reviste carácter normativo, de manera que los objetivos y acciones que en él se fijan, deberán sujetarse en su concreción a las disposiciones del ordenamiento jurídico vigente. Por ende, en su implementación, las instituciones responsables y colaboradoras consideradas en el mismo, no podrán exceder el límite de las atribuciones que la ley les asigna en relación con las acciones que les corresponde ejecutar.
A continuación, respecto de aquellas acciones que señalan como indicadores de cumplimiento la aprobación de actos administrativos o normativos corresponde emitir a entidades distintas de las responsables, cabe precisar que la obligación se considerará satisfecha cuando se inicie o persevere en la tramitación del respectivo proyecto, según sea el caso.
A su vez, las menciones que se hagan a la Corporación Nacional Forestal deberán entenderse efectuadas al Servicio de Biodiversidad y Áreas Protegidas o al Servicio Nacional Forestal, según corresponda a la competencia de que se trate, una vez que entren en pleno funcionamiento tales organismos que la reemplazan, acorde con las leyes N°s 21.600 y 21.744, respectivamente.
Con los alcances que anteceden, se ha tomado razón del instrumento del rubro.
Saluda atentamente a Ud., Víctor Hugo Merino Rojas, Contralor General de la República (S).
A la señora
Ministra del Medio Ambiente
Presente