APRUEBA PLAN DE RECUPERACIÓN, CONSERVACIÓN Y GESTIÓN DE LAS RANITAS DE DARWIN (RHINODERMA DARWINII Y R RUFUM)
Núm. 38.- Santiago, 2 de septiembre de 2025.
Vistos:
Lo dispuesto en los artículos 19 N° 8 y 32 N° 6, de la Constitución Política de la República de Chile, cuyo texto refundido, coordinado y sistematizado fue fijado por el decreto supremo N° 100, de 2005, del Ministerio Secretaría General de la Presidencia; en los artículos 37, 70 letra i), 71 letra f) y 73 de la ley N° 19.300, sobre Bases Generales del Medio Ambiente; en la ley N° 21.600, que crea el Servicio de Biodiversidad y Áreas Protegidas y el Sistema Nacional de Áreas Protegidas; en el Convenio sobre Diversidad Biológica, promulgado como ley de la República mediante el decreto supremo N° 1.963, de 1994, del Ministerio de Relaciones Exteriores; en el decreto con fuerza de ley N° 1-19.653, de 2000, del Ministerio Secretaría General de la Presidencia, que fijó el texto refundido, coordinado y sistematizado de la Ley N° 18.575, Orgánica Constitucional de Bases Generales de la Administración del Estado; en la ley N° 19.880, que establece Bases de los Procedimientos Administrativos que Rigen los Actos de los Órganos de la Administración del Estado; en el decreto supremo N° 1, de 2014, del Ministerio del Medio Ambiente, que aprueba el Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies; en el decreto supremo N° 42, de 2011, del Ministerio del Medio Ambiente, que aprueba y oficializa el séptimo proceso de Clasificación de especies según su estado de conservación; en carta de 11 de septiembre de 2024, de la ONG Ranita de Darwin; en la resolución exenta N° 5.181, de 10 de octubre de 2024, del Ministerio del Medio Ambiente, que inicia el procedimiento abreviado para la elaboración del Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin (Rhinoderma darwinii y R. rufum); en el acuerdo N° 16/2025, del Consejo de Ministros para la Sustentabilidad y el Cambio Climático, adoptado el 24 de julio de 2025; en la resolución N° 36, de 2024, de la Contraloría General de la República, que fija normas sobre exención de trámite de toma de razón; y,
Considerando:
1. Que, conforme al artículo 19 N° 8 de la Constitución Política de la República, es deber del Estado tutelar la preservación de la naturaleza.
2. Que, conforme lo dispone el literal i) del artículo 70 de la ley N° 19.300, sobre Bases Generales del Medio Ambiente ("ley N° 19.300"), es atribución del Ministerio del Medio Ambiente proponer políticas y formular planes, programas y acciones que establezcan los criterios básicos y las medidas preventivas para favorecer la recuperación y conservación de los recursos hídricos, genéticos, las plantas, algas, hongos y animales silvestres, los hábitats, los paisajes, ecosistemas y espacios naturales, en especial los frágiles y degradados, contribuyendo al cumplimiento de los convenios internacionales de conservación de la biodiversidad.
3. Que, originalmente, el artículo 37 de la ley N° 19.300 atribuía la competencia para aprobar los planes de recuperación, conservación y gestión de especies ("Planes RECOGE") al Ministerio del Medio Ambiente.
4. Que, el artículo 144 de la ley N° 21.600, que crea el Servicio de Biodiversidad y Áreas Protegidas ("SBAP") y crea el Sistema Nacional de Áreas Protegidas ("ley N° 21.600"), reemplazó el artículo 37 de la ley N° 19.300, en orden a señalar que el mencionado Servicio deberá aprobar los Planes RECOGE, de acuerdo con lo dispuesto en la referida ley.
5. Que el artículo primero transitorio de la ley N° 21.600, dispuso que será un decreto con fuerza de ley, que deberá ser dictado dentro del plazo de un año de publicada la ley, el que establecerá la fecha en que el SBAP entrará en funcionamiento.
6. Que, el decreto con fuerza de ley N° 1, de 2024, del Ministerio del Medio Ambiente estableció en su artículo 3° que la entrada en funcionamiento del SBAP contemplará un período para su implementación, y otro de entrada en operaciones, añadiendo que el período de implementación se extenderá desde la publicación del referido decreto con fuerza de ley N° 1 en el Diario Oficial; hecho que sucedió el 9 de marzo de 2024, y hasta el día anterior a la fecha de su entrada en operaciones propiamente tal.
7. Que el decreto con fuerza de ley N° 2, de 2024, del Ministerio del Medio Ambiente, estableció en su artículo 7° que el Servicio de Biodiversidad y Áreas Protegidas entrará en operaciones a contar del 1 de febrero de 2026.
8. Que, atendido a que el SBAP se encuentra en un período de implementación, en la elaboración y aprobación de los Planes RECOGE se debe seguir el principio de continuidad de la función pública, establecido en los artículos 3° y 28 de la ley N° 18.575, en virtud del cual los órganos de la Administración del Estado tienen por finalidad promover el bien común atendiendo las necesidades públicas en forma continua y permanente, por lo que la potestad para aprobar los Planes RECOGE, se mantiene en el Ministerio del Medio Ambiente, hasta la entrada en operaciones del SBAP (aplica criterio adoptado por la Contraloría General de la República, entre otros en su dictamen N° 26190, de 2012).
9. Que, el decreto supremo N° 1, de 2014, del Ministerio del Medio Ambiente, que aprueba el Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies, define los Planes RECOGE como un instrumento administrativo que contiene el conjunto de metas, objetivos y acciones que deberán ejecutarse para recuperar, conservar y manejar una o más especies que hayan sido clasificadas en el marco del Reglamento para la Clasificación de Especies Silvestres según Estado de Conservación.
10. Que, en el mismo sentido, la ley N° 21.600, define plan de manejo como "instrumento de gestión ambiental basado en la mejor evidencia posible, que establece metas, principios, objetivos, criterios, medidas, plazos y responsabilidades para la gestión adaptativa de la biodiversidad", y Planes de recuperación, conservación y gestión de especies como aquel plan de manejo destinado a mejorar el estado de conservación de una o más especies clasificadas de conformidad a lo establecido en el artículo 37 de la ley N° 19.300.
11. Que, a través del decreto supremo N° 42, de 2011, del Ministerio del Medio Ambiente, que aprobó y oficializó el séptimo proceso de Clasificación de Especies según su Estado de Conservación, se clasificó a la especie ranita de Darwin del norte (Rhinoderma rufum) bajo la categoría En Peligro Crítico, y, la especie ranita de Darwin (Rhinoderma darwinii) bajo la categoría En Peligro.
12. Que, las Ranitas de Darwin (Rhinoderma darwinii y R rufum) se encuentran amenazadas por la pérdida y fragmentación de su hábitat, incendios forestales, la presencia de enfermedades como la Quitridiomicosis, el cambio climático, entre otras.
13. Que, siguiendo lo establecido en el artículo 21 del decreto supremo N° 1, de 2014, del Ministerio de Medio Ambiente, que aprueba el Reglamento para la elaboración de Planes de Recuperación, Conservación y Gestión de Especies, a través de resolución exenta N° 5.181, de 10 de octubre de 2024, del Ministerio del Medio Ambiente, se dio inicio al procedimiento abreviado para la elaboración del Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin (Rhinoderma darwinii y R rufum).
14. Que, en conformidad con lo establecido en el literal f) del artículo 71, de la ley N° 19.300, y en artículo 19 del decreto supremo N° 1, de 2014, del Ministerio de Medio Ambiente, el Consejo de Ministros para la Sustentabilidad y el Cambio Climático, en sesión ordinaria de 24 de julio de 2025, adoptó por unanimidad el acuerdo N° 16/2025, de proponer a S.E. el Presidente de la República, el Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin (Rhinoderma darwinii y R rufum).
Decreto:
Artículo único.- Apruébase el siguiente Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin (Rhinoderma darwinii y R rufum).
PLAN DE RECUPERACIÓN, CONSERVACIÓN Y GESTIÓN DE LAS RANITAS DE DARWIN (RHINODERMA Darwinii Y R rufum)
1. Introducción
El año 2010 es promulgada en Chile la ley N° 20.417 que crea el Ministerio del Medio Ambiente, el Servicio de Evaluación Ambiental y la Superintendencia del Medio Ambiente, modificando, entre otros cuerpos legales, la ley N° 19.300 sobre Bases Generales del Medio Ambiente, sustituyendo su artículo 37 para entregarle al Ministerio del Medio Ambiente (MMA), la competencia de aprobar Planes de Recuperación, Conservación y Gestión de Especies (RECOGE) que hayan sido clasificadas según su estado de conservación. Luego, conforme a la referida competencia se dictó el decreto supremo N° 1, de 2014, del Ministerio del Medio Ambiente, que aprobó el reglamento que establece los procedimientos para la elaboración de planes RECOGE, lo que formalmente dio inicio a la creación de estos planes y al funcionamiento del Comité de Planes, entidad encargada de asesorar y apoyar al MMA en la formulación de los planes.
Según el reglamento para la elaboración de los planes RECOGE, el principal objetivo de este instrumento de protección ambiental es mejorar la conservación de las especies nativas de Chile, optimizando la coordinación entre los distintos Órganos de la Administración del Estado para lograr una gestión eficaz en esta tarea. Asimismo, se busca involucrar al sector privado y a la sociedad civil en la conservación de la biodiversidad, contribuyendo así al desarrollo sustentable de Chile. El Artículo 2 de este decreto establece que los planes RECOGE son un instrumento administrativo que contiene el conjunto de elementos de planificación estratégica para recuperar, conservar y gestionar una o más especies que hayan sido clasificadas según su estado de conservación, siguiendo el proceso establecido en el Reglamento para la Clasificación de Especies Silvestres (RCE), el cual es también administrado y coordinado por el MMA (Decreto N° 29, de 2011, del Ministerio del Medio Ambiente).
Posteriormente, el 6 de septiembre de 2023, fue publicada en el Diario Oficial la ley N° 21.600, que crea el Servicio de Biodiversidad y Áreas Protegidas ("SBAP") y el Sistema Nacional de Áreas Protegidas ("ley N° 21.600"), cuyo artículo 144 modificó nuevamente el artículo 37 de la ley N° 19.300, trasladando la competencia para aprobar Planes RECOGE desde el MMA al SBAP, de acuerdo con lo dispuesto en la referida ley (en especial artículos 42 y 43).
Ahora bien, atendido a que el SBAP se encuentra en un período de implementación, y que conforme al decreto con fuerza de ley N° 2, de 2024, del Ministerio del Medio Ambiente, el SBAP entrará en operaciones a contar del 1 de febrero de 2026, en la elaboración y aprobación de los Planes RECOGE se debe seguir el principio de continuidad de la función pública, establecido en los artículos 3° y 28 de la ley N° 18.575, en virtud del cual los órganos de la Administración tienen por finalidad promover el bien común atendiendo las necesidades públicas en forma continua y permanente, por lo que la potestad para aprobar los Planes RECOGE, se mantiene en el Ministerio del Medio Ambiente, hasta la entrada en operaciones del SBAP.
En este contexto, en septiembre de 2024 la "Asociación Ranita de Darwin" presentó la propuesta de Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin, siguiendo lo establecido por el artículo 21 del citado decreto supremo N° 1, de 2014, del Ministerio de Medio Ambiente, corroborándose en su proceso de revisión por parte del Comité de Planes y por el propio MMA que la propuesta da cumplimiento a lo señalado en el artículo 43 de la ley N° 21.600, precepto que establece los contenidos mínimos que debe poseer un plan RECOGE.
Las Ranitas de Darwin, Rhinoderma darwinii y R. rufum, son dos especies nativas de Chile que han sido clasificadas siguiendo el proceso del RCE en las categorías En Peligro (EN) y En Peligro Crítico (CR), respectivamente (Decreto supremo N° 42, de 2011, del Ministerio del Medio Ambiente). Adicionalmente, estas especies han sido definidas por el Comité de Planes como prioritarias para la elaboración de planes RECOGE. La propuesta se enmarca de manera global dentro de las recomendaciones del Plan de Acción de Conservación de Anfibios (IUCN SSC Amphibian Specialist Group 2024), y regionalmente dentro de las acciones de la Estrategia Binacional de Conservación de las Ranitas de Darwin (UICN CSE Grupo Especialista en Anfibios 2018), ambas iniciativas coordinadas e implementadas mediante procesos participativos por el Grupo Especialista en Anfibios de la Comisión para la Supervivencia de las Especies de la Unión Internacional para la Conservación de la Naturaleza. Además, la formalización e implementación de este plan RECOGE contribuirá a alcanzar las metas 3 y 4 del Marco mundial Kunming-Montreal de la diversidad biológica, las que se refieren a avanzar en la protección de al menos el 30% de las zonas terrestres, de aguas continentales y costeras y marinas, especialmente las zonas de particular importancia para la biodiversidad, mediante áreas protegidas u otras medidas en la conservación del área; y adoptar con urgencia medidas de gestión para la recuperación y conservación de las especies, en particular, especies amenazadas.
2. Presentación del Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin (Rhinoderma darwinii y Rhinoderma rufum)
La ranita de Darwin del Norte o sapito vaquero (Rhinoderma rufum) y la ranita de Darwin del Sur (R. darwinii) son las únicas especies de anfibios conocidas donde el macho cría a los renacuajos dentro de su saco vocal (UICN CSE Grupo Especialista en Anfibios 2018). La distribución histórica de R. rufum se extiende casi exclusivamente a lo largo de la cordillera de la Costa de Chile, desde Zapallar (Región de Valparaíso) hasta Ramadillas (Región del Biobío) (Azat et al. 2021). Lamentablemente, R. rufum no ha sido observada desde 1981 y en la actualidad está categorizada como En Peligro Crítico (Posiblemente Extinta) por la Lista Roja de Especies Amenazadas de la Unión Internacional para la Conservación de la Naturaleza (UICN) y como En Peligro Crítico por el RCE (Azat et al. 2021). Si esta especie se encontrase extinta, esto representaría la primera extinción documentada de un animal nativo de Chile en tiempo contemporáneo. La distribución histórica de R. darwinii ocupa un área que comprende tanto las cordilleras de la Costa y de los Andes desde Concepción (Región del Biobío) hasta Aysén (Región de Aysén) en Chile, e incluyendo un área de la Cordillera de los Andes de Argentina en las provincias de Neuquén y Río Negro. También existen registros de esta especie en partes de la depresión intermedia del centro sur de Chile entre Temuco y el sur de Valdivia. Esta especie está clasificada como En Peligro tanto por la Lista Roja de la UICN como por el RCE (Azat et al. 2021). Ambas especies de Ranita de Darwin son conocidas como especies EDGE - Especies Evolutivamente Únicas y Globalmente Amenazadas - lo que significa que tienen pocos parientes cercanos, siendo una parte irremplazable del patrimonio natural del mundo (Safi et al. 2013).
Diversas poblaciones históricas de R. darwinii han desaparecido durante los últimos 40 años, pero desde el año 2000, existen registros de la persistencia de al menos 56 poblaciones locales de esta especie en Chile y 10 en Argentina (Azat et al. 2021). Estas poblaciones son generalmente pequeñas (<100 individuos) y se encuentran altamente aisladas, algunas presentando un alto riesgo de extinción debido a amenazas como la pérdida y degradación del hábitat, la quitridiomicosis y el cambio climático (UICN CSE Grupo Especialista en Anfibios 2018, Azat et al. 2021). Desde los últimos 15 años ha existido un creciente interés en la investigación y conservación de ambas especies de Ranitas de Darwin. Por ejemplo, en la última década se ha generado aproximadamente el 75% de las publicaciones indexadas en la Web of Science que tienen relación con el género Rhinoderma y se han iniciado diversos proyectos de conservación in situ y ex situ enfocados en estas especies (UICN CSE Grupo Especialista en Anfibios 2018, Azat et al. 2021). Por ejemplo, actualmente existen dos proyectos de conservación ex situ enfocados en Rhinoderma: uno liderado por la Universidad de Concepción en conjunto con el Zoológico de Leipzig (iniciado en 2009) y otro liderado por el Zoológico Nacional del Parque Metropolitano de Santiago (iniciado en 2010). Por su parte, la Asociación Ranita de Darwin lidera varios proyectos de conservación in situ y educación ambiental enfocados en estas especies, incluido un programa de conservación de tierras donde propietarios/as privados forman parte de la conservación de las Ranitas de Darwin. (1)
Aprovechando el interés de diferentes sectores de la sociedad en la conservación de las Ranitas de Darwin, en 2017 el Grupo Especialista en Anfibios de la UICN da inicio al proceso que crea en 2018 la Estrategia Binacional de Conservación de las Ranitas de Darwin. Esta iniciativa de planificación reúne a 24 organizaciones gubernamentales, organizaciones no gubernamentales sin fines de lucro y privadas de Chile, Argentina, Alemania y el Reino Unido. Utilizando un enfoque participativo (Figura 1) y basado en evidencia, esta estrategia busca implementar acciones prioritarias para la conservación de las Ranitas de Darwin y los bosques nativos de Chile y Argentina. Una de las acciones prioritarias de esta estrategia de conservación es conseguir la elaboración de un Plan RECOGE de las Ranitas (2) de Darwin. Esto permitirá conseguir el reconocimiento oficial de esta estrategia de conservación en Chile, ayudando a fortalecer su implementación y la participación de los diferentes actores relevantes, incluyendo (pero no limitándose) a organismos públicos tales como el MMA y el Servicio Agrícola y Ganadero de Chile.
___________________
(1) https://www.ranitadedarwin.org/conservaciondetierras
(2) www.estrategiarhinoderma.org
La presente propuesta de Plan RECOGE de las Ranitas de Darwin ha sido liderada por la Asociación Ranita de Darwin en un proceso participativo que buscó adaptar la Estrategia Binacional de Conservación de las Ranitas de Darwin siguiendo el proceso estipulado por el Reglamento para la elaboración de Planes RECOGE. En esta tarea, se ha contado con la participación de diversos actores clave, incluyendo representantes del Ministerio del Medio Ambiente, Corporación Nacional Forestal, Servicio Agrícola y Ganadero, Universidad Andrés Bello, Sociedad Zoológica de Londres, Forestal Arauco, Zoológico Nacional de Chile, Red Chilena de Herpetología, Universidad Católica de Temuco, Universidad de Concepción, Universidad de Chile, Zoológico de Leipzig, Fundación Huilo Huilo, Parque Tantauco, Reserva Elemental Melimoyu, Fundación Nahuelbuta Natural, entre otros (Figura 1).
La metodología y terminología utilizada para la elaboración de la propuesta de Plan RECOGE de las Ranitas de Darwin se basó en los Estándares Abiertos para la Práctica de la Conservación (Versión 4.0; Conservation Measures Partnerships 2020). Esta metodología facilita la sistematización de la planificación, gestión y monitoreo de proyectos de conservación a través de cinco etapas (conceptualizar, planificar, implementar, analizar y adaptar, y compartir) integradas en un proceso adaptativo, lo que permite definir y alcanzar metas y mejorar continuamente los esfuerzos de conservación. Además, se siguieron algunas de las recomendaciones presentes en el manual para la implementación de los Estándares Abiertos de la Foundation of Success (Foundation of Success 2009) y del Manual para la planificación del manejo de las áreas protegidas del SNASPE (Conaf 2017).
 Figura 1. Actividades participativas de planificación que permitieron la creación de la propuesta del Plan de Recuperación, Conservación, y Gestión de las Ranitas de Darwin. (a) Simposio "Construyendo una Estrategia de Conservación para las Ranitas de Darwin (Santiago, septiembre 2017). (b) Taller de trabajo para la elaboración de la Estrategia Binacional de Conservación de las Ranitas de Darwin (Neltume, septiembre 2017). (c) Ceremonia de lanzamiento oficial de la Estrategia Binacional de Conservación de las Ranitas de Darwin (Santiago, enero 2018). (d) y (e) Taller de trabajo para la actualización de la Estrategia Binacional de Conservación de las Ranitas de Darwin (Santiago, enero 2024). (f) Reunión de trabajo y presentación facilitadora de la Estrategia Binacional de Conservación de las Ranitas de Darwin (en línea, mayo 2024).
Figura 1. Actividades participativas de planificación que permitieron la creación de la propuesta del Plan de Recuperación, Conservación, y Gestión de las Ranitas de Darwin. (a) Simposio "Construyendo una Estrategia de Conservación para las Ranitas de Darwin (Santiago, septiembre 2017). (b) Taller de trabajo para la elaboración de la Estrategia Binacional de Conservación de las Ranitas de Darwin (Neltume, septiembre 2017). (c) Ceremonia de lanzamiento oficial de la Estrategia Binacional de Conservación de las Ranitas de Darwin (Santiago, enero 2018). (d) y (e) Taller de trabajo para la actualización de la Estrategia Binacional de Conservación de las Ranitas de Darwin (Santiago, enero 2024). (f) Reunión de trabajo y presentación facilitadora de la Estrategia Binacional de Conservación de las Ranitas de Darwin (en línea, mayo 2024). 3. Antecedentes generales de las Ranitas de Darwin
3.1. El género Rhinoderma
El naturalista inglés Charles Darwin fue el primero en recolectar, para su descripción científica, un ejemplar de ranita de Darwin. Darwin encontró esta especie en diciembre de 1834 en la Isla de Lemuy, Archipiélago de Chiloé, durante su viaje a bordo del H.M.S. Beagle (Chancellor y Van Wyhe 2009). En aquella ocasión Darwin registró las siguientes observaciones sobre la especie: "Tiene el iris de color óxido. La pupila negra. –Ojos pequeños. –Apariencia muy bonita y curiosa. –Nariz finamente punteada. –Salta como una rana. Habita densos y oscuros bosques." (Keynes 2000). Los ejemplares recolectados por Darwin fueron enviados primero al Reino Unido y posteriormente a Francia, donde los zoólogos André Marie Constant Duméril y Gabriel Bibron la describieron como Rhinoderma darwinii en honor a su colector (Duméril y Bibron 1841).
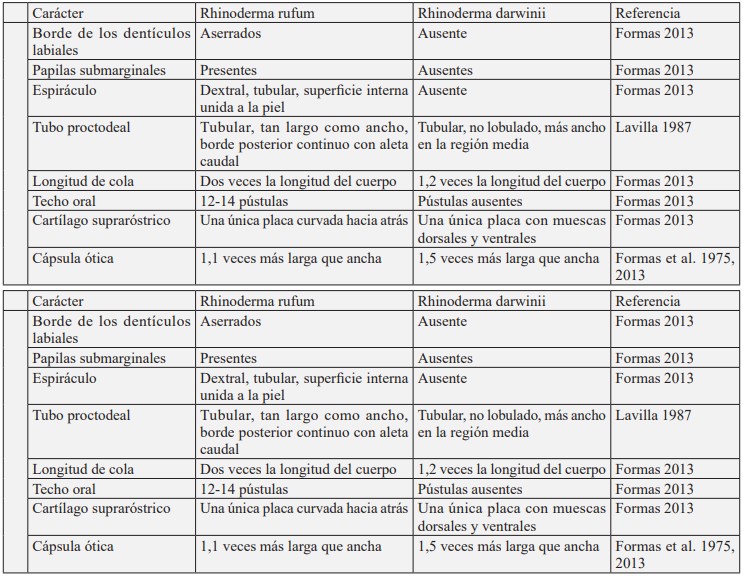
En 1902, Rodulfo Amando Philippi describió la especie Heminectes rufus en base a un solo ejemplar recolectado entre 1861 y 1862 por L. Landbek en Vichuquén, Chile central. La descripción de H. rufus hace referencia a caracteres morfológicos que podrían atribuirse al género Rhinoderma. Sin embargo, la falta del ejemplar tipo y la descripción confusa implicó que la especie no fuera reconocida como válida por Cei (1958), considerándose por largo tiempo como una posible forma local de R. darwinii (Cei 1962, Donoso-Barros 1970). Formas et al. (1975) determinaron, basados en rasgos de la morfología craneal y desarrollo, que el género Heminectes es efectivamente un sinónimo de Rhinoderma. Sin embargo, estos autores argumentaron que existe suficiente evidencia para considerar a R. darwinii y H. rufus especies diferentes, en este último caso proponiendo la nueva combinación Rhinoderma rufum (Philippi 1902). Desde esa fecha, se considera que el género Rhinoderma está compuesto por dos especies: R. rufum (Ranita de Darwin del Norte o sapito vaquero) y R. darwinii (Ranita de Darwin del Sur) (Formas et al. 1975). Los caracteres morfológicos que sustentan la diferenciación de ambas especies se detallan en la Tabla 1, mientras que otras diferencias relacionadas al desarrollo y canto son mencionadas más adelante en el texto.
Tabla 1. Diferencias morfológicas entre los adultos y larvas de Rhinoderma rufum y R. darwinii
 3.2. Cuidado parental, desarrollo embrionario y larval
3.2. Cuidado parental, desarrollo embrionario y larval En la descripción de R. darwinii realizada por Guichenot, se menciona que las hembras de la especie serían vivíparas (Gay 1848). Posteriormente, Jiménez de la Espada (1872) realizó una disección detallada de algunos ejemplares de esta misma especie, percatándose que eran los individuos machos los que llevaban a los renacuajos en el saco vocal (Goicoechea et al. 1986). En efecto, durante el amplexo la hembra deposita los huevos en pequeños refugios ubicados en el suelo húmedo del bosque, entre la hojarasca, musgos y helechos (Figura 2a; Busse 2004, Valenzuela-Sánchez et al. 2014a). Estos huevos son de gran tamaño en relación con el tamaño de la hembra (~5 mm; Bürger 1905) y aparentemente son depositados exactamente en el mismo sitio donde el macho se encontraba realizando las vocalizaciones para atraer a la hembra (Pflaumer 1935, Busse 2004). Durante aproximadamente dos semanas ocurren en este sitio de ovipostura las primeras etapas del desarrollo embrionario; luego de este periodo, durante los primeros días del movimiento muscular de los embriones, el macho incorpora las larvas en su saco vocal (Figura 2b, c). Cabeza-Alfaro et al. (2021) describieron la presencia de cuidado aloparental masculino en R. darwinii, basado en la observación realizada en cautiverio de un macho que incorporó larvas provenientes de huevos que habían sido fecundados por otro macho.
 Figura 2. (a) Huevos de Rhinoderma darwinii sobre el musgo en un sitio en el sur de Chiloé, Chile. En (b) un macho ha incorporado tres de estos embriones en su saco vocal y se prepara a incorporar el embrión restante. Los machos de esta especie (c) pueden criar hasta 22 larvas en su saco vocal (Wilhelm 1927), adquiriendo la apariencia de estar preñados. Fotografías: Asociación Ranita de Darwin.
Figura 2. (a) Huevos de Rhinoderma darwinii sobre el musgo en un sitio en el sur de Chiloé, Chile. En (b) un macho ha incorporado tres de estos embriones en su saco vocal y se prepara a incorporar el embrión restante. Los machos de esta especie (c) pueden criar hasta 22 larvas en su saco vocal (Wilhelm 1927), adquiriendo la apariencia de estar preñados. Fotografías: Asociación Ranita de Darwin. Rhinoderma darwinii posee generalmente un desarrollo larval completo al interior del saco vocal del macho, por un periodo que habitualmente dura entre 6 a 8 semanas y que ocurre entre primavera y otoño (UICN CSE Grupo Especialista en Anfibios 2018). Sin embargo, machos criando larvas a lo largo de los fríos meses de invierno sugieren que este periodo se puede extender por varios meses en algunas ocasiones (Wilhelm 1927). Durante el tiempo en el que las larvas permanecen dentro del saco vocal, el macho les provee de alimento y oxígeno a través de su epitelio, y las larvas absorben estos componentes a través de la piel e intestinos (Wilhelm 1927, Jorquera et al. 1972, Goicoechea et al. 1986). En el caso de R. darwinii, el máximo número de crías registradas en el saco vocal de un macho es de 22 larvas (Wilhelm 1927). Finalmente, los juveniles recientemente metamorfoseados son expulsados desde el saco vocal del macho hacia el medio terrestre (Jorquera et al. 1972, Busse 2004). Se ha observado que renacuajos de R. darwinii que son liberados antes de tiempo pueden completar la metamorfosis en sustrato húmedo (Pflaumer 1935, Busse 1970); si bien esta situación debe ser poco frecuente en condiciones naturales, esto no ha sido estudiado detalladamente. De manera diferente, las larvas de R. rufum permanecen en el saco vocal del macho sólo por un periodo que no superaría las dos semanas, luego del cual estas serían expulsadas al agua para completar su desarrollo y alcanzar la metamorfosis (Barros 1918, Formas 1979). En concordancia con esto, y a diferencia de las larvas de R. darwinii (ver Lavilla 1987), las larvas de R. rufum poseen rostrodontes (piezas bucales queratinizadas presentes en los renacuajos de muchas especies) e intestinos bien desarrollados, características adecuadas para la vida libre en el medio acuático (Formas 2013). Existe evidencia de que en R. rufum podría existir también una relación trófica entre el macho y las larvas durante el acotado tiempo de desarrollo dentro del saco vocal (Jorquera et al. 1982).
3.3. Distribución histórica
Bourke et al. (2012) proponen un mapa con la distribución del hábitat adecuado para R. rufum basados en 19 registros históricos de esta especie provenientes de la literatura, animales de museos, comunicaciones personales y considerando variables bioclimáticas y de uso del suelo. Adicionalmente, basados en 13 registros encontrados en la literatura, siete localidades obtenidas desde animales de museo y una comunicación personal, Soto-Azat et al. (2013a) proponen que la distribución histórica de R. rufum se extiende desde Zapallar (Región de Valparaíso) hasta Ramadillas (Región de Biobío), limitándose principalmente a la cordillera de la Costa entre los 0 y los 500 m de altitud, pero incluyendo un registro en los faldeos de la Cordillera de los Andes de la Región de O'Higgins (Figura 3, Barros 1918, Cuevas 2014).
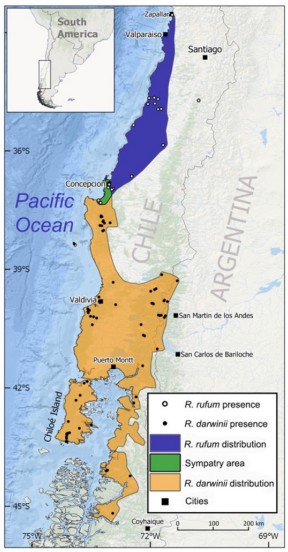 Figura 3. Distribución histórica de Rhinoderma darwinii (naranjo) y R. rufum (azul), incluyendo el área de simpatría de estas especies (verde). Los puntos negros indican las 66 localidades actuales de R. darwinii incluidas en Azat et al. (2021). Un total de 56 localidades se encuentran presentes en Chile. Los puntos blancos muestran las localidades históricas de R. rufum, incluyendo un registro inusual en los faldeos de la Cordillera de los Andes. Obtenido de Azat et al. (2021).
Figura 3. Distribución histórica de Rhinoderma darwinii (naranjo) y R. rufum (azul), incluyendo el área de simpatría de estas especies (verde). Los puntos negros indican las 66 localidades actuales de R. darwinii incluidas en Azat et al. (2021). Un total de 56 localidades se encuentran presentes en Chile. Los puntos blancos muestran las localidades históricas de R. rufum, incluyendo un registro inusual en los faldeos de la Cordillera de los Andes. Obtenido de Azat et al. (2021). Por otra parte, basados en 24 registros encontrados en la literatura y 90 registros de localidades obtenidas desde especímenes almacenados en museos, Soto-Azat et al. (2013a) proponen que la distribución histórica de R. darwinii se extiende desde Concepción hasta Aysén (Región de Aysén), incluyendo a Isla Mocha y el archipiélago de Chiloé, encontrándose también en una estrecha franja de los Andes argentinos en las provincias de Neuquén y Río Negro (Figura 3). Esta franja en los faldeos orientales de la Cordillera de los Andes representa el límite oriental de distribución de la especie y está totalmente contenida en dos Parques Nacionales de Argentina, el PN Lanín y el PN Nahuel Huapi (Úbeda y Pastore 2021). Ambas especies son simpátricas en la zona de Concepción, aparentemente sintópicas en el pasado en localidades tales como Chiguayante, Hualqui y Ramadillas (Formas et al. 1975, Penna y Veloso 1990, Soto-Azat et al. 2013a).
3.4. Distribución actual
Rhinoderma rufum no ha sido registrada desde 1981 (Serrano et al. 2021), pese a varios esfuerzos por encontrar poblaciones de la especie (Busse 2002, Bourke et al. 2012, Soto-Azat et al. 2013a, Cuevas 2014).
Por otra parte, según UICN CSE Grupo Especialista en Anfibios (2018) en la actualidad existen 56 localidades con registros actuales de poblaciones o individuos de R. darwinii en Chile (Figura 3), siendo la más septentrional la correspondiente a Cuyinco Alto en la Cordillera de Nahuelbuta (C. Castro, comunicación personal). Sin embargo, desde esa fecha se han publicado registros adicionales en el Monumento Natural Lahuen Ñadi en la Región de Los Lagos (González 2021), alrededores del Santuario El Cañi en la Región de la Araucanía (Novoa et al. 2018) y existen registros no publicados de la especie en el Parque Nacional Conguillío en la Región de La Araucanía (M. Saavedra y A. Valenzuela-Sánchez, comunicación personal 2020). Por otra parte, algunas poblaciones en el extremo sur de la Isla Grande de Chiloé podrían encontrarse extintas (A. Valenzuela-Sánchez, comunicación personal 2024). Esto evidencia la necesidad de mantener una base de datos actualizada sobre las localidades actuales de esta especie.
Rhinoderma darwinii ha desaparecido aparentemente de localidades en las que fue abundante hasta hace algunos años en Chile (Crump y Veloso 2005, Soto-Azat et al. 2013a). Por ejemplo, Soto-Azat et al. (2013a) no lograron detectar individuos de R. darwinii en el Monumento Nacional Cerro Ñielol (Temuco, Región de la Araucanía), localidad que registraba alta abundancia de la especie en el pasado (Rageot 1978). Estos autores también documentan la declinación severa de la especie en el Parque Nacional Nahuelbuta y en la localidad de Melimoyu, donde la especie era abundante hasta finales del siglo XX (Crump 2002). Preocupantemente, varias de las localidades con presencia actual de R. darwinii albergan poblaciones locales con una baja abundancia de individuos. Considerando la limitada capacidad de dispersión de la especie (Valenzuela-Sánchez 2017), muchas de estas poblaciones locales se encontrarían altamente aisladas (Soto-Azat et al. 2013a).
En la actualidad se cuenta con registro de Rhinoderma darwinii en las siguientes áreas protegidas: Parque Nacional Nahuelbuta, Santuario de la Naturaleza El Natri (área privada), Monumento Natural Contulmo, Reserva Nacional Isla Mocha, Parque Nacional Huerquehue, Parque Nacional Villarrica, Parque Nacional Alerce Costero, Parque Nacional Puyehue, Parque Nacional Chiloé y Parque Nacional Queulat. Para Rhinoderma rufum no hay registros históricos de su presencia en áreas protegidas.
3.5. Ecología de las Ranitas de Darwin
3.5.1. Generalidades
Casi la totalidad del conocimiento sobre la ecología de Rhinoderma se basa en estudios enfocados en R. darwinii. Esta es una especie completamente terrestre, que no requiere de cuerpos de agua para completar su desarrollo larval (Jorquera et al. 1972). Como muchos otros anfibios completamente terrestres (Müller et al. 2013), R. darwinii vive asociada a ambientes boscosos (Figura 4), habitando específicamente el bosque templado de Chile y Argentina (Soto-Azat et al. 2013a). Si bien la especie es ampliamente reconocida como especialista de bosque nativo (Valenzuela-Sánchez et al. 2019a), existen registros anecdóticos de que la especie puede ocupar plantaciones de árboles exóticos como pino y eucaliptus (C. Cuevas, comunicación personal), especialmente cuando estas plantaciones tienen presencia de sotobosque conformado por especies nativas (A. Valenzuela-Sánchez, comunicación personal). Dentro del bosque, los individuos no se distribuyen homogéneamente, sino que se congregan en sitios acotados, generalmente menores a 0,5 hectáreas (Crump 2002, Soto-Azat et al. 2013a, Valenzuela-Sánchez et al. 2014a, 2017). Los recursos y condiciones que determinan la selección del hábitat por parte de esta especie no son totalmente conocidos, pero parcelas del bosque que poseen una menor variación micro-climática diaria y una mayor área basal (una medida de biomasa de los árboles vivos) poseen una mayor abundancia de ranas (Valenzuela-Sánchez et al. 2019a). Aspectos sociales de la especie podrían jugar también un rol importante en la selección del hábitat, y, por ende, en la agrupación espacial de los individuos (Serrano 2019).
 Figura 4. Vista del bosque templado austral en un sitio que alberga una población de Rhinoderma darwinii en el sur de Chiloé, Chile. El sitio ha sido demarcado para el estudio de la ecología de movimientos de esta especie. Fotografía: Asociación Ranita de Darwin.
Figura 4. Vista del bosque templado austral en un sitio que alberga una población de Rhinoderma darwinii en el sur de Chiloé, Chile. El sitio ha sido demarcado para el estudio de la ecología de movimientos de esta especie. Fotografía: Asociación Ranita de Darwin. 3.5.2. Vocalizaciones
La actividad vocal de Rhinoderma spp. 3 es predominantemente diurna, aunque algunas poblaciones pueden vocalizar de manera continua durante la noche entre los meses de noviembre y marzo (Serrano et al. 2020a, 2020b). El canto de anuncio de ambas especies de Rhinoderma consiste en la repetición de una a siete notas suaves y de frecuencia media. Los cantos están compuestos por la repetición de una a seis notas, aunque lo más frecuente en distintas poblaciones es que el canto posea cuatro o cinco notas (Bidart 2021).
Los cantos en las diferentes poblaciones de Rhinoderma difieren por la duración de los intervalos entre notas, la frecuencia dominante y la duración del caos (Bidart 2021, Serrano et al. 2020a). Tales diferencias están probablemente influidas por el tamaño corporal, pues estas características acústicas están relacionadas con la variación del tamaño de hocico de cloaca (Serrano et al. 2020a). Penna y Veloso (1990) proveen un análisis preliminar de los cantos de R. darwinii y R. rufum indicando la distinción entre estas especies. Sin embargo, dicho estudio se basó en un número limitado de individuos y no consideró análisis estadísticos. En un análisis más profundo que incluyó un mayor número de grabaciones de ambas especies, Bidart (2021) encontró que no existe evidencia estadística para la delimitación de estas especies en base a sus rasgos acústicos. Este autor propone que la divergencia observada entre las especies y poblaciones de Rhinoderma puede atribuirse a una variación geográfica dependiente de los regímenes ambientales a lo largo del rango histórico de una única unidad evolutiva.
Durante la temporada reproductiva (generalmente entre septiembre y abril, pero esto depende de la zona geográfica), machos y hembras de R. darwinii vocalizan activamente durante el día, siendo características de la duración y frecuencia dominante, las que varían entre el canto de los distintos sexos (Serrano 2019).
3.5.3. Variaciones intraespecíficas en tamaño corporal y coloración
La tasa de crecimiento y el tamaño corporal de los individuos de R. darwinii presentan una variación intraespecífica (Valenzuela-Sánchez et al. 2015, 2017). El tamaño corporal de los adultos, que en promedio es de alrededor de 24 mm de longitud hocico-cloaca (rango: 18,5-37,5 mm), se correlaciona positivamente con la estacionalidad de temperatura (Valenzuela-Sánchez et al. 2015). En este sentido, se plantea que individuos que hibernan por un periodo más largo de tiempo poseen mayores tamaños corporales como un mecanismo para reducir los costos asociados a la hibernación, o alternativamente, como un beneficio producto de la hibernación (Valenzuela-Sánchez et al. 2015). En concordancia con esto último, se ha observado que individuos de poblaciones en localidades más estacionales poseen una mejor condición corporal post-hibernación (Valenzuela-Sánchez et al. 2015). La hibernación se ha asociado positivamente en otras especies de anuros de zonas templadas con la probabilidad de sobrevivencia (Reading 2007) y el éxito reproductivo en cautiverio (Santana et al. 2015), y probablemente juega un rol crucial en diferentes procesos biológicos en R. darwinii (Valenzuela-Sánchez et al. 2015). El tamaño corporal además varía entre sexos, siendo las hembras generalmente de mayor tamaño que los machos (Crump 2002, Bourke 2012, Valenzuela-Sánchez et al. 2014a).
___________________
(3) Se aclara que el término "spp." hace referencia a todas las especies del género previamente mencionado, por lo tanto al hablar de Rhinoderma spp., se debe entender que la frase alude a ambas especies de Ranitas de Darwin, es decir, Rhinoderma darwinii y Rhinoderma rufum.
La coloración dorsal de los individuos de R. darwinii, que puede variar de tonos verdes a marrones (Figura 5), también muestra variación entre sexos (Bourke et al. 2011a). Por ejemplo, en la zona de Coñaripe (Región de Los Ríos) las hembras son mayoritariamente marrones (Bourke et al. 2011a). Crump (2002) y Bourke et al. (2011a) sugieren que los individuos utilizan sustratos que coinciden con su coloración dorsal. La diferencia intersexual en la coloración dorsal puede asociarse a la disponibilidad localidad-específica de diversos sustratos y a la selección diferencial de microhábitats entre machos y hembras. En poblaciones norteñas, los sustratos verdes (e.g. musgos, helechos) son menos abundantes y utilizados preferentemente por los machos, probablemente porque representan sitios adecuados para la ovipostura (Bourke et al. 2011a, Valenzuela-Sánchez et al. 2014a). En cambio, en las poblaciones sureñas los sustratos verdes son extremadamente abundantes; en estas poblaciones la proporción de hembras con coloraciones verdes es mucho mayor que en las poblaciones septentrionales (A. Valenzuela-Sánchez, comunicación personal). Los individuos de R. darwinii tienen también la capacidad de cambiar su coloración dorsal en el transcurso de algunas semanas a meses (Bourke et al. 2011b).
 Figura 5. Patrones de coloración dorsal en una población de Rhinoderma darwinii en Coñaripe, sur de Chile. (a) "doble V", (b) "hoja de bambú", (c) "verde completo", (d) "brazos blancos", y (e) "teñido". Obtenido de Bourke et al. (2012).
Figura 5. Patrones de coloración dorsal en una población de Rhinoderma darwinii en Coñaripe, sur de Chile. (a) "doble V", (b) "hoja de bambú", (c) "verde completo", (d) "brazos blancos", y (e) "teñido". Obtenido de Bourke et al. (2012). 3.5.4. Dieta
Rhinoderma darwinii es un depredador con un comportamiento de sentarse y esperar (del inglés "sit-and-wait"), donde los individuos consumen presas que se encuentran cerca de su alcance, no realizando una búsqueda activa de estas (Crump 2002). Esta especie tiene una dieta relativamente generalista y es un consumidor secundario en los ambientes que habita, con una posición trófica estimada de 2,9 (Molina-Burgos et al. 2018). Basados en un análisis de isótopos estables y contenido estomacal, Molina-Burgos et al. (2018) encontraron que las principales presas de esta especie son invertebrados herbívoros, los cuales fueron detectados en el 68,1% del alimento asimilado en individuos de R. darwinii recolectados en Neltume y Puyehue, en el sur de Chile. Las presas más comúnmente consumidas fueron mosquitos, moscas, saltamontes, grillos y hormigas. Otros invertebrados detritívoros y carnívoros también fueron detectados en la dieta, pero en menores proporciones (Molina-Burgos et al. 2018). Previo a este estudio, la única referencia a la dieta de R. darwinii fue realizada por Wilhelm (1927), citando el trabajo del profesor Carlos Schneider, quien describe en el contenido estomacal de individuos de esta especie "la presencia de insectos del género Musca, Hiperalomia, Tipúlidas, Agrion, Perla, Gyrinus, Aechna, y Cordulia" (algunas de estas clasificaciones taxonómicas ya no están en uso). Según nuestro conocimiento, no existen estudios sobre la dieta de R. rufum, pero probablemente las presas consumidas y sus proporciones asimiladas sean similares a las descritas para R. darwinii.
3.5.5. Ecología poblacional y abundancia
La tasa de crecimiento poblacional en R. darwinii es generalmente más sensible a la sobrevivencia de los adultos que a otros parámetros demográficos (Valenzuela-Sánchez et al. 2017), aunque existe una gran variación interpoblacional en las estrategias de historia de vida de esta especie (Valenzuela-Sánchez et al. 2022). Lo último quiere decir que existen poblaciones de R. darwinii que son más rápidas, donde la longevidad de los individuos es menor, pero tienen una mayor fecundidad anual, y otras poblaciones más lentas, donde los individuos viven más años, pero tienen una fecundidad anual menor (Valenzuela-Sánchez et al. 2022). Esta variación interpoblacional en parámetros demográficos se ha asociado también con variaciones en la senescencia de mortalidad (i.e. aumento en el riesgo de morir a medida que los individuos envejecen) en R. darwinii, existiendo una senescencia acelerada en poblaciones más rápidas (Valenzuela-Sánchez et al. 2023). En promedio la sobrevivencia de R. darwinii en vida silvestre es entre 7 a 8 años (Valenzuela-Sánchez et al. 2023), pero existen registros de captura-recaptura de individuos que podrían haber alcanzado los 15 años en vida silvestre (A. Valenzuela-Sánchez, comunicación personal).
Los individuos de R. darwinii tienden a congregarse en lugares específicos del bosque, generalmente en un área que no supera las 0,5 hectáreas (Valenzuela-Sánchez et al. 2017). En parches de bosque con la suficiente superficie y las condiciones ambientales adecuadas para la especie, se pueden encontrar varias de estas poblaciones locales formando una población estructurada espacialmente. Siguiendo la terminología utilizada por la Lista Roja de la UICN, una población estructurada espacialmente podría considerarse como una subpoblación de R. darwinii. Asimismo, el área del bosque que alberga una subpoblación podría considerarse una localidad. Esta es la definición que ocupamos en este plan (ver también definición utilizada en Tabla 2).
Desde 2018, se han estudiado poblaciones estructuradas espacialmente de R. darwinii ubicadas en Neltume y Contulmo 4 , con una distancia promedio entre pares de poblaciones locales de alrededor de 70 metros. Incluso a esta escala espacial fina, la dispersión de individuos entre poblaciones locales en una escala anual es muy baja (promedio de probabilidad de dispersión, Contulmo = 0.046 [0.023-0.075], Neltume = 0.040 [0.024-0.059]) (A. Valenzuela-Sánchez, comunicación personal), concordante con estudios previos sugiriendo una limitada capacidad de dispersión en esta especie (ver subsección 3.5.6). Interesantemente, la dinámica de las subpoblaciones de R. darwinii podría variar según los niveles de dispersión entre poblaciones locales. Si las poblaciones locales muestran dinámicas asincrónicas (por ejemplo, por variación a la exposición con el hongo quítrido), la existencia de dispersión condición-dependiente podría permitir la estabilización de las subpoblaciones y disminuir el riesgo de extinción de la población estructurada espacialmente (Duncan et al. 2015). Este es un aspecto que merece esfuerzos de investigación, ya que permitiría entender de mejor forma la dinámica poblacional de esta especie.
La abundancia en poblaciones locales de R. darwinii (estimada utilizando modelos de captura-recaptura) es relativamente baja, variando entre los 10 y los 145 individuos (Soto-Azat et al. 2013a, Valenzuela-Sánchez et al. 2017). En Argentina, a partir de los años 90' no se han registrado capturas numerosas de individuos (<10 individuos por localidad; C. Úbeda, comunicación personal). En poblaciones pequeñas se espera que las diferentes fuentes de estocasticidad (demográfica, ambiental, proporción de sexos y heterogeneidad demográfica) sean mayores en comparación a poblaciones grandes, aumentando así el riesgo de extinción (Melbourne y Hastings 2008). Esta situación puede verse empeorada si las poblaciones locales se encuentran altamente aisladas.
___________________
(4) https://www.ranitadedarwin.org/emerge
3.5.6. Movimientos y rango de hogar
Los individuos adultos de R. darwinii son altamente sedentarios y poseen una alta fidelidad de sitio (Crump 2002, Valenzuela-Sánchez et al. 2019b). El rango de hogar promedio estimado durante tres meses en la estación reproductiva en una población local ubicada al sur de Chiloé fue de 1,82 m 2 , no observándose mayores diferencias entre edades (juveniles vs adultos) y sexos (machos vs hembras; Valenzuela-Sánchez et al. 2014a). Los individuos de esta población sobreponen en gran medida sus rangos de hogar, no presentando mayores signos de territorialidad, pero sí un aparente espaciamiento de los machos que se encuentran cantando (una observación también descrita por Busse (2004) en individuos mantenidos en cautiverio).
Utilizando datos de captura-recaptura espacial colectados durante un período de 4 años en poblaciones silvestres de R. darwinii ubicadas en Neltume, en combinación con modelos estadísticos y de simulación, Valenzuela-Sánchez et al. (2019b) encontraron evidencia de que la dispersión en esta especie es realizada principalmente por los juveniles. En contraste, los adultos mostraron una alta fidelidad al sitio, con un desplazamiento anual medio de 3,64 m (Figura 6). Valenzuela-Sánchez (2017) estimó que, luego de una corrección por el tamaño limitado de las áreas de estudio utilizando modelos de caminatas aleatorias, solo el 1% de los juveniles podría dispersar a una distancia de 146 m en el transcurso de un año. Esta limitada capacidad de dispersión se debería al hecho de que esta especie vive en ambientes relativamente estables y continuos en el espacio y el tiempo, en comparación con los ambientes utilizados por anfibios que crían en pozas (paisajes altamente heterogéneos y ambientes reproductivos menos estables), en donde se han observado eventos de dispersión que superan en varios órdenes de magnitud los estimados para R. darwinii (Cayuela et al. 2020).
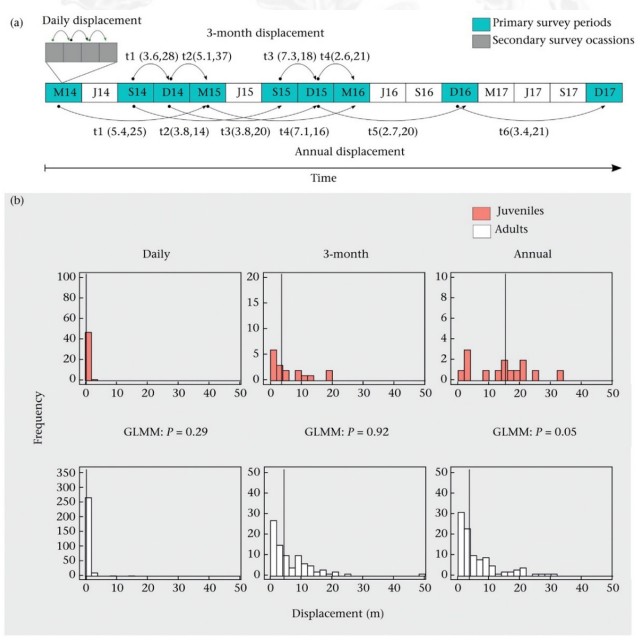 Figura 6. (a) Configuración temporal del estudio de captura-recaptura espacial de Rhinoderma darwinii, mostrando los diferentes intervalos de tiempo (t1, t2,...t total ) durante los cuales se obtuvieron datos de desplazamiento. Entre paréntesis se muestra la mediana de los desplazamientos en metros y el número total de registros para cada intervalo de tiempo. En (b), se muestran los histogramas específicos por edad (juveniles en rojo, adultos en blanco) del desplazamiento en las tres escalas temporales evaluadas (de izquierda a derecha: diario, 3 meses, anual). La línea vertical negra indica la mediana de desplazamiento. La captura-recaptura de ranas se realizó en dos sitios de estudio en Neltume, sur de Chile. Obtenido de Valenzuela-Sánchez et al. (2019b).
Figura 6. (a) Configuración temporal del estudio de captura-recaptura espacial de Rhinoderma darwinii, mostrando los diferentes intervalos de tiempo (t1, t2,...t total ) durante los cuales se obtuvieron datos de desplazamiento. Entre paréntesis se muestra la mediana de los desplazamientos en metros y el número total de registros para cada intervalo de tiempo. En (b), se muestran los histogramas específicos por edad (juveniles en rojo, adultos en blanco) del desplazamiento en las tres escalas temporales evaluadas (de izquierda a derecha: diario, 3 meses, anual). La línea vertical negra indica la mediana de desplazamiento. La captura-recaptura de ranas se realizó en dos sitios de estudio en Neltume, sur de Chile. Obtenido de Valenzuela-Sánchez et al. (2019b). 3.6. Estado de conservación de las Ranitas de Darwin
3.6.1. Clasificación en el RCE y Lista Roja de Especies Amenazadas de la UICN
Rhinoderma rufum está categorizada en Peligro Crítico (Posiblemente Extinta (CR [PE])) por la Lista Roja de la UICN utilizando el criterio D (IUCN SSC Amphibian Specialist Group 2015). La justificación para esta categorización es que la especie no ha sido observada desde 1981 a pesar de reiterados intentos por encontrar poblaciones (IUCN SSC Amphibian Specialist Group 2015), aplicándose el criterio D porque se infiere una población menor a 50 individuos maduros. Asimismo, el Reglamento de Clasificación de Especies (RCE) de Chile, la considera como en Peligro Crítico de extinción. Basado en modelos de distribución de especies, Bourke et al. (2012) desarrollaron mapas de distribución potencial de R. rufum con el fin de dirigir búsquedas para encontrar poblaciones de esta especie. Por otro lado, usando registros de avistamientos históricos y un modelo de estimación óptima lineal, Soto-Azat et al. (2013a) sugieren que la especie puede haberse extinguido el año 1982 (intervalo de confianza del 95%: 1980-2000).
Rhinoderma darwinii está categorizada En Peligro de extinción (EN) por la Lista Roja de la UICN utilizando los criterios B2ab(iii) (IUCN SSC Amphibian Specialist Group 2018). La justificación para esta categoría se basa en una limitada área de ocupación (estimada en 264 km2), severa fragmentación de sus poblaciones y continua declinación. Asimismo, esta especie está categorizada como En Peligro según el RCE de Chile. En Argentina en cambio, esta especie está categorizada como Amenazada según el Ministerio de Ambiente y Desarrollo Sustentable (Resolución 1055/13), categoría que se obtuvo como producto de la recategorización del estado de conservación de los Anfibios de Argentina realizada en un taller de especialistas (Vaira et al. 2012) siguiendo la metodología descrita por Giraudo et al. (2012).
3.6.2. Clasificación en el Estado Verde de las Especies de la UICN
El Estado Verde de las Especies de la UICN es un instrumento que evalúa el potencial de recuperación de las especies y el impacto pasado, presente y futuro de los esfuerzos de conservación (Grace et al. 2021). Rhinoderma darwinii ha sido categorizada como Críticamente Depletada (Critically Depleted) el Estado Verde (Azat y Valenzuela-Sánchez 2021), mientras que R. rufum no ha sido categorizada.
La categoría asignada a R. darwinii en el Estado Verde se debe a que la especie se ha extinto en la mayor parte de su rango histórico de distribución y está amenazada en muchas de las áreas donde aún permanece (Azat y Valenzuela-Sánchez 2021).
El Estado Verde tiene cuatro métricas para medir el impacto de la conservación: 1) Legado de Conservación, 2) Dependencia de Conservación, 3) Ganancia de Conservación, 4) Potencial de Recuperación. Rhinoderma darwinii tiene un Legado de Conservación alto, lo que significa que, sin acciones de conservación pasadas, se espera que R. darwinii estuviese casi extinta en el presente. La especie tiene también una Dependencia de Conservación alta; si se detuviera la protección de la especie y su hábitat, se espera que la pérdida y degradación del hábitat ocurran en muchas áreas donde la especie aún permanece durante un período de 10 años. Rhinoderma darwinii tiene una Ganancia de Conservación de cero; en un período de 10 años, se espera que las acciones de conservación planificadas, aunque beneficiosas, principalmente prevengan una mayor declinación durante ese período de tiempo. Finalmente, en un período de 100 años, sería posible reintroducir R. darwinii en algunas partes del rango donde el hábitat permanece o podría ser restaurado, y que podría recuperarse a poblaciones funcionales ecológicamente en partes de su rango. Por lo tanto, el Potencial de Recuperación en esta escala de tiempo para la especie es alto (Azat y Valenzuela-Sánchez 2021).
3.6.3. Análisis de viabilidad del estado de las Ranitas de Darwin según atributo ecológico clave
La evaluación de la viabilidad de las especies en las que se enfoca este plan (i.e. nuestros objetos de conservación según terminología Estándares Abiertos) permiten determinar la situación actual de estas especies, y cómo lucirían los atributos ecológicos claves de estos objetos de conservación si se encontrasen en un estado saludable (Foundation of Success 2009). De esta forma, este análisis permite definir objetivos y metas para un plan de conservación que sean adecuadas, viables y medibles. En esta sección seguimos los procedimientos para el análisis de viabilidad descritos en Foundation of Success (2009).(5)
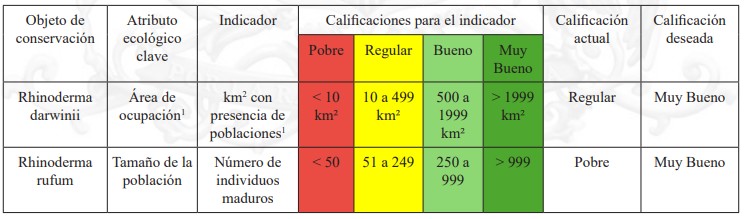
En la Tabla 2, presentamos un resumen del análisis de viabilidad, indicando la calificación actual y deseada para los atributos ecológicos claves de cada especie de ranita de Darwin. Es importante destacar que hemos utilizado una aproximación pragmática para determinar los atributos claves de cada especie y para definir los valores para las diferentes categorías de los indicadores utilizados para medir el estado de estos atributos ecológicos clave. Específicamente, para cada especie hemos definido como atributo clave el principal criterio utilizado para asignar su estado de conservación en la evaluación de la Lista Roja de la UICN (ver 3.6.1). De esta forma, una calificación deseada en estos indicadores significaría que las especies estarían fuera de una categoría de amenaza en base a los criterios utilizados para definir cada atributo ecológico clave. Esta aproximación permite definir metas realistas e indicadores que consideramos viables de medir. Además, consideramos que estos indicadores cumplen con los cuatro criterios recomendados por la Foundation of Success (2009) para un buen indicador (i.e. medible, preciso, consistente, y sensible). Lamentablemente, esta decisión conlleva el compromiso de que la calificación deseada no refleja precisamente un estado óptimo de nuestros objetos de conservación, lo que en nuestro caso es especialmente evidente para la especie con mayor riesgo de extinción (R. rufum) donde la calificación deseada se puede alcanzar con un número de individuos maduros que podría considerarse limitado (1.000 individuos). Incluso alcanzando la calificación deseada, R. rufum podría ser hipotéticamente asignada a una categoría de amenaza en la Lista Roja de la UICN o RCE utilizando otros criterios de la Lista Roja distintos al criterio utilizado para su categorización actual (p. ej. criterio B en lugar del D).
___________________
(5) Según los Estándares Abiertos, los atributos ecológicos claves son: "Aspectos de la biología o ecología de un objeto de conservación que, de estar presentes, definen un objeto de conservación saludable" (Conservation Measures Partnerships 2020).
Además, es necesario destacar que, para ambas especies, y en concordancia con la evaluación de R. darwinii para el Estado Verde de la UICN (Azat y Valenzuela-Sánchez 2021), se espera que la calificación deseada se alcance en el largo plazo (i.e. dentro de los próximos 100 años) y no dentro del periodo de implementación del presente plan (i.e. próximos 15 años). El cambio esperado en el estado de nuestros objetos de conservación durante la implementación de este plan se define en la sección 8 ("Meta del Plan").
Tabla 2. Resumen de evaluación de viabilidad para los dos objetos de conservación del plan RECOGE de las Ranitas de Darwin
 4. Diagnóstico e identificación de amenazas y sus efectos sobre las Ranitas de Darwin
4. Diagnóstico e identificación de amenazas y sus efectos sobre las Ranitas de Darwin En esta sección realizamos una evaluación de las amenazas directas que afectan a las Ranitas de Darwin. Para esto utilizamos la información disponible a la fecha de la elaboración de este plan, 6 la que fue obtenida desde la literatura científica y desde la opinión de expertos en los diferentes talleres de trabajo y revisiones del borrador del presente plan RECOGE, realizado por miembros de la Estrategia Binacional de Conservación de las Ranitas de Darwin. La evaluación de amenazas es un componente crucial de la etapa de conceptualización del proceso de planificación definido en los Estándares Abiertos que permite determinar las amenazas prioritarias (o "amenazas críticas") sobre las cuales es más importante enfocar las acciones del plan (Conservation Measures Partnerships 2020).
___________________
(1) El estado actual del Área de Ocupación (AOO) de esta especie ha sido calculado siguiendo los lineamientos de la Lista Roja de la UICN (IUCN Standards and Petitions Committee 2024), en específico utilizando una grilla con celdas cuadradas de 2 x 2 km, y asumiendo que 66 de estas celdas se encuentran ocupadas por poblaciones de la especie.
(6) Según los Estándares Abiertos, las amenazas directas son "principalmente actividades humanas que directamente generan degradación de uno o más objetos de conservación (p. ej., pesca no sostenible, caza no sostenible, perforación petrolera, construcción de carreteras, aguas residuales industriales o introducción de especies exóticas invasoras)." (Conservation Measures Partnerships 2020). Fenómenos naturales afectados por actividades humanas también podrían considerarse como amenazas directas.
4.1. Calificación o priorización de amenazas
En esta subsección presentamos los resultados de la priorización de las amenazas críticas (i.e. las amenazas directas que serán abordadas en el presente plan RECOGE) que afectan a las Ranitas de Darwin. Estas amenazas son descritas en detalle más adelante en la subsección 4.3.
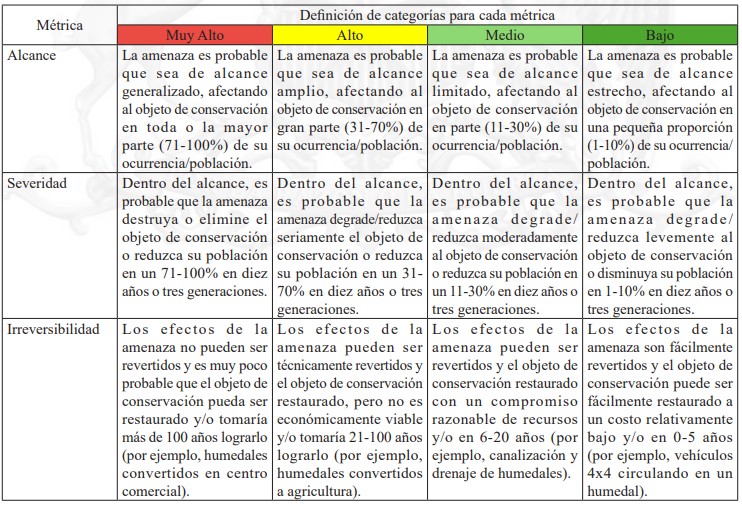
Para la priorización de amenazas se pueden utilizar distintas aproximaciones (Conservation Measures Partnerships 2020); el presente documento utiliza la descrita por la Foundation of Success (2009) ya que esta ha sido la aproximación implementada tanto en el software Miradi como en el Manual para la planificación del manejo de las áreas protegidas del SNASPE (Conaf 2017) y en diferentes planes RECOGE que han sido aprobados a la fecha. Esta priorización se basa en la utilización de tres métricas. Las dos primeras (alcance y severidad) miden la magnitud general de la amenaza. El alcance mide la proporción del objeto de conservación que será afectado por la amenaza en un periodo de 10 años bajo condiciones actuales (Foundation of Success 2009). La severidad mide el nivel de daño causado al objeto de conservación por la amenaza en los próximos 10 años (Foundation of Success 2009). La tercera métrica, conocida como irreversibilidad, mide el escenario hipotético de que, si la amenaza cesara de existir y en qué grado los impactos de esta amenaza sobre el objeto de conservación podrían ser revertidos (Foundation of Success 2009). En la Tabla 3 detallamos los valores utilizados para las categorías de cada una de estas métricas.
Tabla 3. Métricas utilizadas para la priorización de las amenazas críticas que afectan a las Ranitas de Darwin. Información obtenida de Foundation of Success (2009, p. 60)
 La priorización se realizó para cada objeto de conservación por separado (Tablas 4 y 5). Para obtener el resumen de las calificaciones de cada amenaza para cada objeto de conservación se utilizó la metodología implementada en el software Miradi, la que da un mayor peso a las métricas de severidad y alcance que a la de irreversibilidad (ver Apéndice B en Foundation of Success (2009) para ver los detalles de la metodología).
La priorización se realizó para cada objeto de conservación por separado (Tablas 4 y 5). Para obtener el resumen de las calificaciones de cada amenaza para cada objeto de conservación se utilizó la metodología implementada en el software Miradi, la que da un mayor peso a las métricas de severidad y alcance que a la de irreversibilidad (ver Apéndice B en Foundation of Success (2009) para ver los detalles de la metodología). Tabla 4. Calificación de las amenazas críticas para Rhinoderma darwinii
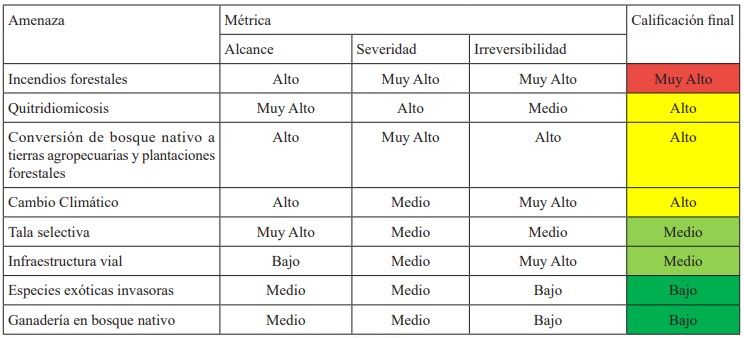 Tabla 5. Calificación de las amenazas críticas para Rhinoderma rufum
Tabla 5. Calificación de las amenazas críticas para Rhinoderma rufum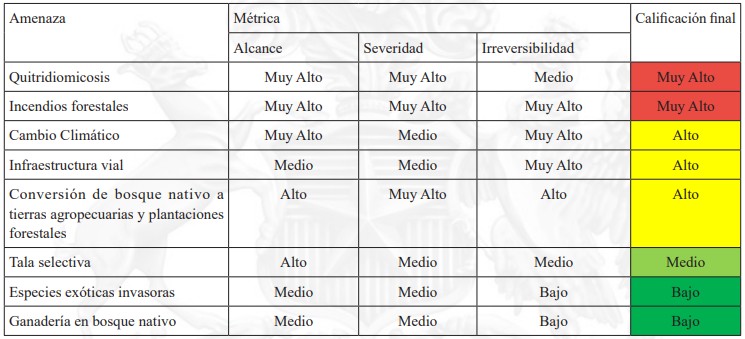 4.2. Análisis situacional
4.2. Análisis situacional Para la elaboración de la Estrategia Binacional de Conservación de las Ranitas de Darwin (UICN Grupo de Especialistas de Anfibios Chile 2018) se realizó un análisis situacional que permitió entender el contexto de dicha estrategia de conservación, y que puede resultar relevante para el presente plan RECOGE. En dicho análisis se identificaron las amenazas directas que afectan a las Ranitas de Darwin y también los factores clave que impulsan estas amenazas, incluyendo amenazas indirectas y barreras7 . El análisis reconoce la falta de información en diversos aspectos de la biología y ecología de las especies, o del nivel de impacto de algunas amenazas por lo que en el Plan RECOGE se incluye a varias bajo el carácter de amenaza potencial para promover medidas que, de manera precautoria, contribuyan a levantar información y la determinación del posible impacto. En la Figura 7 presentamos el modelo conceptual que resume dicho análisis situacional.(8)
___________________
(7) Según los Estándares Abiertos, una amenaza indirecta es "un factor identificado en el análisis situacional del proyecto como impulsor de una amenaza directa" (Conservation Measures Partnerships 2020). También conocidas como causas subyacentes, factores contribuyentes, o causas raíz.
(8) En la Estrategia Binacional de Conservación de las Ranitas de Darwin las barreras fueron definidas de manera ad-hoc y hacen alusión específicamente a la ausencia de información que actúa como una barrera para la elaboración de metas, estrategias y actividades óptimas. La falta de conocimiento científico que pueda ser usado de manera efectiva por los profesionales practicantes de la conservación ("actionable science") ha sido identificada como una barrera para la práctica
de la conservación en el contexto global. La Estrategia Binacional está disponible en https://www.estrategiarhinoderma.org/
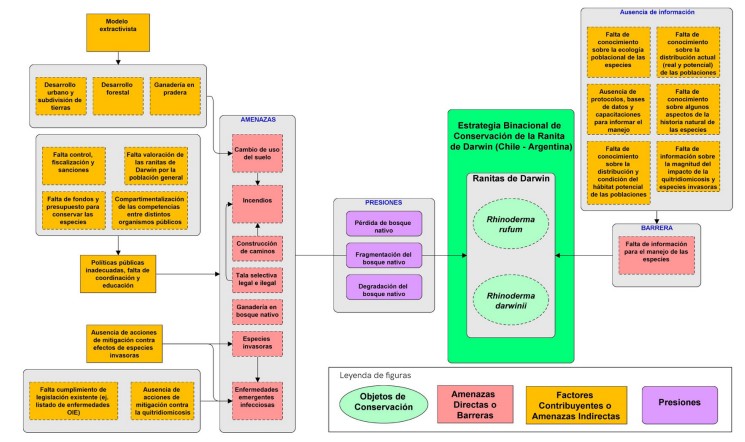 Figura 7. Mapa conceptual desarrollado para la Estrategia Binacional de Conservación de las Ranitas de Darwin que detalla la relación entre las amenazas directas, amenazas indirectas, y los objetos de conservación de este plan RECOGE. Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
Figura 7. Mapa conceptual desarrollado para la Estrategia Binacional de Conservación de las Ranitas de Darwin que detalla la relación entre las amenazas directas, amenazas indirectas, y los objetos de conservación de este plan RECOGE. Obtenido de UICN CSE Grupo Especialista en Anfibios (2018). 4.3. Descripción de las amenazas críticas
4.3.1. Incendios forestales
A la fecha, no existen registros publicados de extinción de poblaciones del género Rhinoderma por el efecto de incendios forestales, pero es muy probable que esta sea una amenaza muy importante para estas especies, especialmente en el escenario actual y futuro de cambio climático.
Los incendios forestales tienen la capacidad de producir la destrucción de la vegetación y del hábitat de diversas especies en grandes extensiones de terreno, además de causar mortalidad directa sobre la fauna (Abom y Schwarzkopf 2016, Zuniga et al. 2021, Moyo 2022). Además, los incendios intensifican las condiciones de vulnerabilidad en los ecosistemas boscosos afectados, al aumentar la erosión de suelos y facilitar la invasión de especies exóticas invasoras (Keeley et al. 2012, Silva et al. 2018, Lucas-Borja et al. 2024). Los incendios forestales pueden representar una amenaza para las poblaciones de anfibios, especialmente en especies terrestres y especies que crían en esteros (Hossack y Pilliod 2011), como es el caso de las especies del género Rhinoderma.
En Chile, los incendios forestales han tenido impactos devastadores en los bosques nativos (Urrutia‐Jalabert et al. 2018, González et al. 2020) que son vitales para la biodiversidad, el bienestar humano, y para la persistencia de las especies del género Rhinoderma. La recuperación de estos ecosistemas tras un incendio es un proceso largo y complejo, y en muchos casos la vegetación original es reemplazada por especies menos diversas y más inflamables, lo que, a su vez, aumenta el riesgo de futuros incendios y perpetúa un ciclo de degradación ambiental (Brooks et al. 2004, Taylor et al. 2017).
En las últimas décadas, los incendios forestales han incrementado considerablemente en frecuencia y extensión en diversas regiones del mundo (Flannigan et al. 2009). Chile no ha sido la excepción, experimentando un aumento sostenido en el número de incendios forestales desde el año 2010, acompañado de una extensión significativa en la temporada que estos ocurren. Por ejemplo, según las Estadísticas de Incendios Forestales de Chile, entre los años 2013 y 2023 el total de superficie total afectada fue de 1.659.354 hectáreas, donde solamente en la temporada de 2016 y 2017 la superficie total afectada fue de 570.197 hectáreas, representando un récord en el registro histórico disponible. Las regiones que presentaron mayor superficie afectada en el último período (2013-2023) en Chile incluyen regiones con presencia de Rhinoderma spp., específicamente la Región del Biobío con 391.326 ha, la Región del Maule con 381.146 ha, y la Región de la Araucanía con 369.072 ha.
Antes del 2010, los incendios forestales en Chile se limitaban generalmente a los meses entre finales de noviembre y finales de abril (González et al. 2020). Actualmente, la temporada de incendios se extiende desde octubre hasta mayo del año siguiente, lo que representa una ampliación considerable del periodo de riesgo y una mayor exposición de los ecosistemas a este tipo de perturbaciones (González et al. 2020).
Además, es importante destacar la retroalimentación positiva que ocurre entre el cambio climático y la ocurrencia de incendios (Liu et al. 2014). Bajo escenarios de cambio climático se proyecta que las temperaturas aumenten y las precipitaciones disminuyan, particularmente en la zona centro sur de Chile, lo que podría incidir en el aumento de la ocurrencia de incendios forestales y el área afectada (González et al. 2011).
4.3.2. Conversión de bosque nativo a tierras agropecuarias y plantaciones forestales
Rhinoderma rufum se encuentra principalmente asociada al bosque deciduo Maulino, que se extiende por la Cordillera de la Costa entre el río Mataquito (35° S) y el río Biobío (37° S; Smith-Ramírez 2004). El área cubierta por este tipo de bosque templado disminuyó su extensión desde la colonización española (Armesto et al. 2010), continuando su disminución hasta las últimas décadas principalmente por el cambio de uso de suelo a tierras agrícolas y plantaciones forestales de especies exóticas (Figura 8). Por ejemplo, Echeverría et al. (2006) estudiaron la pérdida de bosque Maulino entre 1975 y 2000 (coincidente con el periodo de desaparición de R. rufum) en un área de 578.164 hectáreas entre el río Maule (35°20'S) y la ciudad de Cobquecura (36°S). Entre los citados años el porcentaje del área de estudio cubierta por bosque nativo se redujo de un 21% a un 7%, mientras que el porcentaje del área cubierta por plantaciones forestales de especies exóticas aumentó de un 5% a un 36%. En efecto, la principal razón de la pérdida de bosque Maulino y otros tipos de bosque templado durante ese periodo es el reemplazo por monocultivos comerciales de pino insigne (Pinus radiata) y eucalipto común (Eucalyptus globulus; Smith-Ramírez 2004, Echeverría et al. 2006) (Figura 8).
 Figura 8. Tala rasa de monocultivos de Pino insigne (Pinus radiata) en la Cordillera de la Costa de la Región del Maule. Estos cerros se encontraban en el pasado cubiertos por bosque deciduo Maulino, un tipo de bosque templado en el cual habita Rhinoderma rufum. Fotografía: Claudio Azat.
Figura 8. Tala rasa de monocultivos de Pino insigne (Pinus radiata) en la Cordillera de la Costa de la Región del Maule. Estos cerros se encontraban en el pasado cubiertos por bosque deciduo Maulino, un tipo de bosque templado en el cual habita Rhinoderma rufum. Fotografía: Claudio Azat. Sumado a la reducción de la cobertura total de bosque nativo en el área estudiada por Echeverría et al. (2006), también disminuyó el área promedio de los parches y aumentó la fragmentación. Por ejemplo, en 1975, cerca de un 44% del área total cubierta por bosque Maulino se distribuía en parches muy pequeños (<100 ha), mientras que para el año 2000 este porcentaje había incrementado al 69% (Echeverría et al. 2006). Rhinoderma rufum requiere de cursos de agua para completar su reproducción (última fase del desarrollo larval; Jorquera et al. 1981) y es sabido que plantaciones de P. radiata y E. globulus están asociadas a la reducción de flujos de agua superficial tanto a pequeña (Lara et al. 2010) como a gran escala (Little et al. 2009). Paralelamente, en el área donde se ubica el bosque Maulino existe una baja representación de áreas protegidas, todas las cuales son de reducido tamaño (por ejemplo, las Reservas Nacionales Los Queules de 147,3 hectáreas y Los Ruiles de 89,06 hectáreas y, el Parque Nacional Nonguén de 3.036 hectáreas, este último de reciente creación tras su recategorización de reserva a parque nacional el año 2021. En efecto, para el año 2004, el área de bosque deciduo Maulino incluido dentro de las entonces áreas silvestres protegidas era comparativamente sólo un 4,3% del área protegida en la cordillera de los Andes a la misma latitud (Smith-Ramírez 2004). La situación es similar para el área comprendida entre el río Mataquito y el límite norte de la distribución de la especie (Zapallar; 32°S), donde desde la colonización española el bosque nativo ha sido extensamente reemplazado por otros usos del suelo (Armesto et al. 2010, Smith-Ramírez 2004, Soto-Azat et al. 2013a).
Según el Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile (Conaf 2017), en el 28% de la distribución histórica de R. rufum el bosque templado austral ha sido reemplazado por otros usos de suelo (Figura 9). Por ejemplo, la conversión de bosque nativo a tierras agropecuarias y plantaciones forestales ha ocurrido en gran magnitud, especialmente en el centro de Chile (Echeverría et al. 2006, Smith-Ramírez 2004). Otras causas de pérdida de hábitat, tales como la urbanización y desarrollo de infraestructura, también pueden haber jugado un rol en la desaparición de poblaciones locales de Rhinoderma (Soto-Azat et al. 2013b). Por ejemplo, tierras alrededor del Lago Vichuquén, Zapallar y Concepción, han cambiado drásticamente producto del desarrollo urbano y turístico.
Figu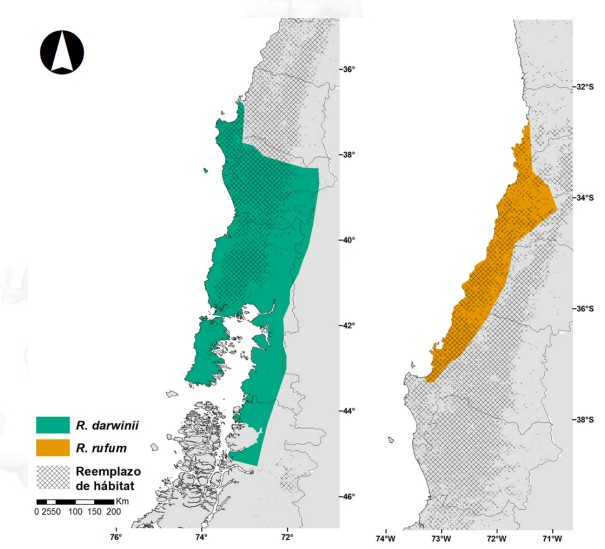 ra 9. Reemplazo de bosque nativo por otros usos de suelo (achurado) en la distribución histórica de Rhinoderma darwinii (verde) y Rhinoderma rufum (naranja) según el Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile (CONAF 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
ra 9. Reemplazo de bosque nativo por otros usos de suelo (achurado) en la distribución histórica de Rhinoderma darwinii (verde) y Rhinoderma rufum (naranja) según el Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile (CONAF 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
 ra 9. Reemplazo de bosque nativo por otros usos de suelo (achurado) en la distribución histórica de Rhinoderma darwinii (verde) y Rhinoderma rufum (naranja) según el Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile (CONAF 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
ra 9. Reemplazo de bosque nativo por otros usos de suelo (achurado) en la distribución histórica de Rhinoderma darwinii (verde) y Rhinoderma rufum (naranja) según el Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile (CONAF 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018). Para el caso de R. darwinii, la situación de pérdida de hábitat es similar; sin embargo, aún existen extensas áreas de bosque nativo tanto en la Cordillera de los Andes como en el centro-sur de Chiloé, muchas resguardadas bajo la figura de áreas protegidas públicas y privadas (Urbina-Casanova et al. 2016). El bosque templado al sur de Concepción permaneció relativamente inalterado por la actividad humana hasta la colonización de la Araucanía en el siglo XIX, aunque existen registros de polen de la zona de la Araucanía y crónicas de los primeros españoles que llegaron a esta región que sugieren que extensas zonas podrían haber estado ya deforestadas debido a su uso como campos agrícolas, especialmente a lo largo de las principales cuencas fluviales (Armesto et al. 2010). La colonización republicana del sur de Chile incentivó la quema de miles de hectáreas de bosque nativo, principalmente en los valles centrales para la habilitación de terrenos con fines agrícolas y posteriormente también plantaciones forestales de árboles exóticos (Armesto et al. 2010). La quema del bosque no sólo se extendió hasta Chiloé, sino que también llegó hasta la Región de Aysén hacia mediados del siglo XX (Armesto et al. 2010). Como un ejemplo de la extensa pérdida de bosque nativo en la distribución de R. darwinii, los bosques primarios en Chiloé actualmente ocupan una extensión de solo un tercio de la distribución original de estos bosques (Pérez et al. 2009).
Según el Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile (Conaf 2017), en el 27% de la distribución histórica de R. darwinii el bosque templado austral de Chile ha sido reemplazado por otros usos de suelo (Figura 9).
4.3.3. Quitridiomicosis
La única enfermedad infecciosa que se ha identificado como una amenaza para Rhinoderma spp. es la quitridiomicosis (Valenzuela-Sánchez et al. 2014b). La infección por Ranavirus ha sido detectada en anfibios silvestres de Chile (Soto-Azat et al. 2016), pero aún no existe evidencia de infección en las especies de Rhinoderma.
La quitridiomicosis de los anfibios es una enfermedad infecciosa emergente producida por el hongo Batrachochytrium dendrobatidis (Bd), considerada como una de las enfermedades infecciosas más devastadoras registradas para la biodiversidad (Scheele et al. 2019). Esta enfermedad ha sido vinculada con la disminución de la población de al menos 501 especies de anfibios en todo el mundo, adicionalmente contribuyendo a la presunta extinción de 90 especies de anfibios (Scheele et al. 2019). La quitridiomicosis permanece como la principal causa de extinciones contemporáneas de anfibios (Luedtke et al. 2023).
El hongo Bd infecta la piel de anfibios susceptibles y los individuos que desarrollan la enfermedad exhiben hiperqueratosis, lo que lleva a una pérdida de la capacidad osmorregulatoria y a la pérdida de electrolitos que eventualmente puede causar la muerte por paro cardiaco asistólico (Voyles et al. 2009).
En Chile, los registros más antiguos existentes del hongo Bd corresponden a infecciones en individuos de R. rufum, R. darwinii y Pleurodema thaul (sapito de cuatro ojos), todos recolectados entre 1970 y 1978, intervalo de tiempo que es coincidente con la enigmática desaparición de R. rufum (Soto-Azat et al. 2013b). En Argentina, el registro de quitridiomicosis más cercano al área de distribución de R. darwinii ha sido reportado para P. thaul en la Laguna Fantasma, en el sudoeste de la Provincia de Río Negro y distante a 30 km de la localidad más cercana conocida de R. darwinii en Argentina (Ghirardi et al. 2014, Úbeda y Pastore 2021).
En el presente, se ha identificado que Chile centro-sur, entre Valparaíso y Concepción, sería un punto caliente de presencia de Bd (James et al. 2015, Bacigalupe et al. 2017, 2019), y por lo tanto las poblaciones de R. rufum tendría un mayor riesgo de exposición a este patógeno que R. darwinii. Sin embargo, el hongo Bd se encuentra ampliamente distribuido en Chile, habiéndose detectado a lo largo de toda la distribución de R. darwinii (Bacigalupe et al. 2019). Incluso en la zona sur de la Isla Grande de Chiloé, un área que había sido identificada como un refugio para R. darwinii debido a una muy baja probabilidad de presencia de Bd (Bacigalupe et al. 2019), en 2023 se detectó la invasión de este patógeno con efectos devastadores para las poblaciones locales de R. darwinii (A. Valenzuela-Sánchez, comunicación personal).
El genoma de aislados del hongo Bd obtenidos en Chile desde Xenopus laevis (rana africana), Calyptocephalella gayi (rana grande chilena) y Batrachyla antartandica (rana jaspeada) indican que el hongo presente en el país pertenece al Linaje Pandémico Global de Bd (Valenzuela-Sánchez et al. 2018, Alvarado-Rybak et al. 2021). Este es un linaje hipervirulento de Bd que se dispersó desde el este de Asia a diferentes partes del mundo durante el siglo XX y que ha estado asociado con mortalidades masivas y extinción de especies de anfibios en múltiples continentes (O'Hanlon et al. 2018).
En los últimos años se ha acumulado evidencia sobre la susceptibilidad e impactos de la quitridiomicosis en Rhinoderma spp. Por ejemplo, esta enfermedad fue asociada con un evento de mortalidad de un grupo de 30 individuos de R. darwinii exportados a Alemania en 2007, donde la enfermedad fue diagnosticada; sin embargo, los efectos de factores estresantes (tales como el viaje y la mantención en cautiverio) también pueden haber jugado un rol en la mortalidad de los individuos (Werning 2009, Bourke et al. 2010).
Los primeros registros contemporáneos de infección con Bd en individuos silvestres de R. darwinii fueron descritos por Bourke et al. (2010) en animales recolectados el año 2005 en Chile en Coñaripe y Neltume. Asimismo, en 2012, un individuo silvestre de R. darwinii fue encontrado muerto en vida silvestre y los análisis posteriores revelaron altas cargas de infección con Bd y hallazgos histopatológicos consistentes con quitridiomicosis (Soto-Azat et al. 2013b). Valenzuela-Sánchez et al. (2017) demostraron que la probabilidad de sobrevivencia anual de individuos de R. darwinii infectados con Bd es cercana a cero (Figura 10), entregando evidencia robusta de que la enfermedad es altamente letal en individuos de vida silvestre. Estudios posteriores en poblaciones monitoreadas por más de 10 años han confirmado estos resultados (A. Valenzuela-Sánchez, comunicación personal). Las cargas de infección con Bd en R. darwinii en vida silvestre son generalmente altas (Figura 10; Soto-Azat et al. 2013b, Valenzuela-Sánchez et al. 2017), lo que es coincidente con especies susceptibles a la enfermedad.
Debido a que el estado de vida infectivo de Bd es una zoospora acuática, y que R. darwinii es una especie completamente terrestre, Valenzuela-Sánchez et al. (2017) han hipotetizado que R. darwinii podría adquirir las infecciones con Bd desde otros anfibios que utilizan tanto ambientes acuáticos como terrestres (p. ej. Eupsophus spp y Batrachyla spp). De esta forma, estos autores proponen que la exclusión de anuros sintópicos en poblaciones de R. darwinii utilizando cercados perimetrales podría ser una medida de mitigación contra la quitridiomicosis a corto o mediano plazo en poblaciones silvestres de R. darwinii (Valenzuela-Sánchez et al. 2017). 9
Figur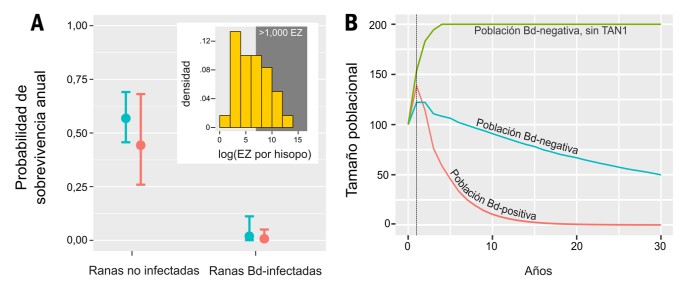 a 10. (a) Probabilidad de sobrevivencia anual en adultos (celeste) y juveniles (rojo) silvestres de Rhinoderma darwinii no infectados e infectados con el hongo Batrachochytrium dendrobatidis (Bd). En el inserto se muestra la carga parasitaria (expresada en equivalentes de zoosporas por hisopo) de los individuos infectados. En (b) se muestra la predicción del tamaño poblacional para una ventana de 30 años en poblaciones locales (sin dispersión) negativas y positivas a la infección con Bd. Para la población no infectada, también se muestra la proyección del tamaño poblacional excluyendo los datos de una de las cuatro poblaciones locales negativas estudiadas (TAN1), ya que esta poseía estimados de sobrevivencia muy diferentes a las otras tres poblaciones. Modificado de Valenzuela-Sánchez et al. (2017).
a 10. (a) Probabilidad de sobrevivencia anual en adultos (celeste) y juveniles (rojo) silvestres de Rhinoderma darwinii no infectados e infectados con el hongo Batrachochytrium dendrobatidis (Bd). En el inserto se muestra la carga parasitaria (expresada en equivalentes de zoosporas por hisopo) de los individuos infectados. En (b) se muestra la predicción del tamaño poblacional para una ventana de 30 años en poblaciones locales (sin dispersión) negativas y positivas a la infección con Bd. Para la población no infectada, también se muestra la proyección del tamaño poblacional excluyendo los datos de una de las cuatro poblaciones locales negativas estudiadas (TAN1), ya que esta poseía estimados de sobrevivencia muy diferentes a las otras tres poblaciones. Modificado de Valenzuela-Sánchez et al. (2017).
 a 10. (a) Probabilidad de sobrevivencia anual en adultos (celeste) y juveniles (rojo) silvestres de Rhinoderma darwinii no infectados e infectados con el hongo Batrachochytrium dendrobatidis (Bd). En el inserto se muestra la carga parasitaria (expresada en equivalentes de zoosporas por hisopo) de los individuos infectados. En (b) se muestra la predicción del tamaño poblacional para una ventana de 30 años en poblaciones locales (sin dispersión) negativas y positivas a la infección con Bd. Para la población no infectada, también se muestra la proyección del tamaño poblacional excluyendo los datos de una de las cuatro poblaciones locales negativas estudiadas (TAN1), ya que esta poseía estimados de sobrevivencia muy diferentes a las otras tres poblaciones. Modificado de Valenzuela-Sánchez et al. (2017).
a 10. (a) Probabilidad de sobrevivencia anual en adultos (celeste) y juveniles (rojo) silvestres de Rhinoderma darwinii no infectados e infectados con el hongo Batrachochytrium dendrobatidis (Bd). En el inserto se muestra la carga parasitaria (expresada en equivalentes de zoosporas por hisopo) de los individuos infectados. En (b) se muestra la predicción del tamaño poblacional para una ventana de 30 años en poblaciones locales (sin dispersión) negativas y positivas a la infección con Bd. Para la población no infectada, también se muestra la proyección del tamaño poblacional excluyendo los datos de una de las cuatro poblaciones locales negativas estudiadas (TAN1), ya que esta poseía estimados de sobrevivencia muy diferentes a las otras tres poblaciones. Modificado de Valenzuela-Sánchez et al. (2017). El monitoreo a largo plazo de poblaciones de R. darwinii 10 ha permitido evidenciar que algunas poblaciones de esta especie tienen la capacidad de contrarrestar la alta mortalidad producida por la quitridiomicosis mediante una alta tasa reproductiva de los machos, lo que llevaría a que un gran número de juveniles y adultos se integren a la población cada año (Valenzuela-Sánchez et al. 2021). Esta situación permitiría la estabilidad poblacional en R. darwinii pese a la presencia del hongo Bd (Valenzuela-Sánchez et al. 2022). Estas observaciones son concordantes con una respuesta conocida como reclutamiento compensatorio, la que ha sido observada en otras especies de anfibios afectadas por la quitridiomicosis (Hardy et al. 2022). Sin embargo, la evidencia disponible sugiere que no todas las poblaciones de R. darwinii tendrían esta capacidad (Valenzuela-Sánchez et al. 2022). Las poblaciones de R. darwinii que no son capaces de contrarrestar los efectos negativos de la quitridiomicosis podrían extinguirse a causa de esta enfermedad (Valenzuela-Sánchez et al. 2022), tal como lo sugiere el patrón histórico de declinaciones y extinciones locales en el género Rhinoderma (Soto-Azat et al. 2013b), modelos matriciales poblacionales (Valenzuela-Sánchez et al. 2017), y recientes observaciones del colapso abrupto de poblaciones de R. darwinii en un área intensamente monitoreada dentro del Parque Tantauco, Isla Grande de Chiloé.
El Parque Tantauco es un área privada protegida de más de 100.000 hectáreas ubicada en la zona sur de la Isla Grande de Chiloé. En el bosque nativo maduro del sector de Inio, en el extremo sur de esta área protegida, se encontraban las poblaciones contemporáneas más grandes que se conocían de R. darwinii (Soto-Azat et al. 2013a, Valenzuela-Sánchez et al. 2022).
___________________
(9) https://www.ranitadedarwin.org/emerge
(10) https://www.ranitadedarwin.org/monitoreo
En base a un intensivo monitoreo epidemiológico que comenzó el año 2010 y que incluyó 1.183 muestras colectadas en anfibios de vida libre para la detección molecular de Bd, el sector de Inio había sido considerado como libre de este patógeno y con una muy baja probabilidad de presencia de este hongo (Bacigalupe et al. 2019). En 2023, como parte del monitoreo a largo plazo de R. darwinii liderado por Asociación Ranita de Darwin, fue posible detectar la invasión de Bd en Inio, comprobándose infecciones tanto en R. darwinii como en otros anfibios silvestres. La prevalencia de infección durante una semana de monitoreo alcanzó valores de 20% y 40% de los individuos encontrados de R. darwinii, representando la prevalencia más alta detectada en poblaciones de esta especie para un periodo similar de muestreo.
Luego de la invasión de Bd, la abundancia en dos poblaciones previamente sanas de R. darwinii se redujo en un 89,1% y 95,5% en solo un año. En estudio intensivo de seguimiento realizado en marzo de 2024, que involucró la búsqueda de la especie en 28 parcelas de estudio distribuidas en hábitat adecuado para R. darwinii en Inio, solo se encontraron 11 individuos a lo largo de cuatro parcelas de estudio, estimándose una muy baja probabilidad de ocupación (0,187, intervalo de confianza del 95%: 0.063-0.378) y evidenciándose la extinción aparente de al menos cinco poblaciones locales de la especie en el área (A. Valenzuela-Sánchez, comunicación personal). No se han observado otros factores aparte de la invasión de Bd que podrían explicar esta declinación abrupta de R. darwinii, tales como cambios en calidad o estructura del bosque, especies invasoras, o condiciones climáticas.
4.3.4. Cambio climático
El cambio climático se espera que afecte con mayor intensidad a especies con baja vagilidad como los anfibios (Janson 2009). Frente a cambios ambientales que no permitan la ocupación de una especie en un área determinada, además de la plasticidad (fisiológica, comportamiento, etc.), los individuos tienen dos posibilidades para evitar la extirpación local de sus poblaciones: 1) adaptación mediante evolución, por ejemplo, de los límites de tolerancia térmica y/u óptimos térmicos; y 2) dispersión a áreas con condiciones ambientales adecuadas (Ruiz-Aravena et al. 2014). En Rhinoderma spp. no existe información acerca de respuestas genéticas o plasticidad frente al cambio climático, siendo un tópico urgente de investigación para poder predecir de mejor manera la respuesta de ambas especies al cambio climático. Uribe-Rivera et al. (2017) desarrollaron modelos de distribución de especies basados en registros históricos de R. darwinii (1950-1975) y capas bioclimáticas para predecir la distribución actual de esta especie (2000-2014). Los autores destacan que al incluir la limitada capacidad de dispersión de R. darwinii en estos modelos, la precisión de las predicciones aumenta de manera considerable. Los autores estimaron que entre 1970 y 2010 se produjo una reducción del rango de distribución de R. darwinii de entre un 23% y 40% considerando una capacidad de dispersión baja, pero incluso levemente superior a la estimada por Valenzuela-Sánchez (2017) en poblaciones silvestres. Cabe destacar que estas predicciones son probablemente subestimaciones de la realidad, ya que estos modelos no incorporan otras amenazas como la pérdida de hábitat por reemplazo de bosque nativo hacia otros usos del suelo, o los impactos de la quitridiomicosis.
Los efectos del cambio climático futuro sobre el hábitat climáticamente adecuado para R. darwinii han sido evaluados por Bourke et al. (2018). Estos autores reportan una expansión en el área con hábitat climáticamente adecuado para la especie en el año 2080, principalmente debido a una expansión de esta área hacia mayores latitudes debido al aumento de la temperatura ambiental. Por el contrario, debido a la limitada capacidad de dispersión de esta especie, el hábitat potencial (i.e. climáticamente adecuado y a la vez accesible para la especie) podría disminuir en el futuro (Uribe-Rivera et al 2017). Utilizando el modelo de distribución descrito por Uribe-Rivera et al. (2017), se proyectó la distribución del hábitat potencial de esta especie en el futuro (2050 y 2080) bajo dos escenarios de cambio climático (RCP4.5 y RCP8.5; D. Uribe-Rivera, comunicación personal).
Estos escenarios representan diferentes trayectorias en el balance de gases de efecto invernadero entre el 2014 y 2100. Estos escenarios consideran emisiones directas de gases de efecto invernadero, así como también proyecciones de crecimiento poblacional, cambio de uso de suelo, crecimiento económico, desarrollo tecnológico, gestión global del cambio climático (por ejemplo, la puesta en práctica de medidas concretas de manejo), factibilidad (económica y tecnológica) de la utilización masiva de energías más limpias, entre otros factores (van Vuuren et al. 2011). El RCP4.5, calificado como un escenario optimista, considera entre otras cosas una estabilización en el crecimiento poblacional en la segunda mitad del siglo XXI, que las nuevas tecnologías de producción energética permitirán que el mercado de la energía limpia se incline hacia su masificación, y que las políticas de uso de suelo permitan ralentizar la pérdida de bosques. El escenario RCP8.5, calificado como pesimista, considera tan solo la estabilización de la población, pero casi nulo impacto del manejo del cambio climático dada la falta de voluntad política, que le daría prioridad al crecimiento económico acelerado, con consecuencias sobre la pérdida de bosques y uso masivo de combustibles fósiles (van Vuuren et al. 2011).
Considerando la limitada capacidad de dispersión de R. darwinii, las predicciones muestran que la tendencia se mantiene hacia una reducción en la extensión del rango de distribución de esta especie (Azat et al. 2021). La distribución potencial de R. darwinii se espera que se reduzca entre un 33% y un 50% respecto al presente (UICN CSE Grupo Especialista en Anfibios 2018). Como es de esperar, dadas las trayectorias de los escenarios de cambio climático evaluados, en la ventana temporal 2050 no hay grandes diferencias en los cambios de distribución predichos para ambos escenarios. Sin embargo, la disminución del rango de distribución para el escenario pesimista (RCP8.5) proyectada a 2080 es notablemente mayor que para al escenario optimista (RCP4.5), ya que éste último contempla la reversión de las tendencias actuales de calentamiento global.
Al representar dichas tendencias en un mapa, podemos observar que, tanto para los escenarios optimista como pesimista, conforme la temperatura aumenta, la distribución geográfica de los climas adecuados se desplaza hacia el sur o hacia mayores altitudes (ver también Bourke et al. 2018). Como consecuencia, vastas áreas en la parte norte y este de la distribución actual de R. darwinii se tornarán climáticamente inadecuadas para su subsistencia, explicando en gran medida la disminución predicha de la distribución potencial de la especie en el futuro (Figura 11). Esto resalta la relevancia de priorizar los esfuerzos de conservación en esta sección de la distribución histórica de R. darwinii, la cual actualmente y más aún en el futuro, se verá sometida a fuertes presiones ambientales (e.g. pérdida de hábitat, enfermedades infecciosas y cambio climático) que amenacen la persistencia de sus poblaciones.
Finalmente, se espera que la mayoría de las áreas que se tornen climáticamente adecuadas para R. darwinii (i.e. que en la actualidad no son adecuadas, pero lo serán en el futuro) no serán colonizadas de forma natural por la especie en una escala de tiempo ecológica, debido a su limitada capacidad de dispersión (deudas de colonización; Valenzuela-Sánchez et al. 2019b; Figura 11).
Figur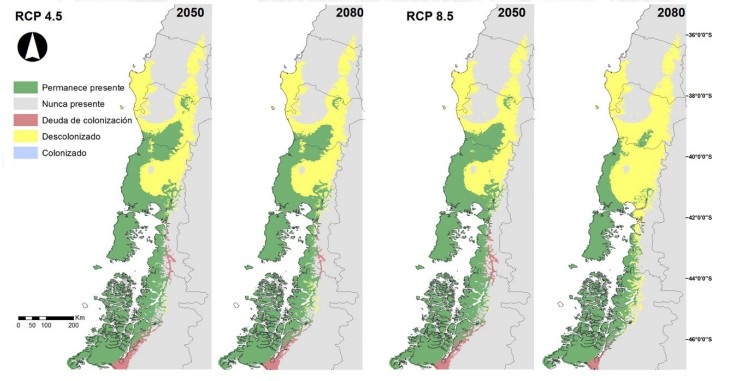 a 11. Distribución potencial de Rhinoderma darwinii en 2050 y 2080 frente a dos escenarios de cambio climático (RCP4.5 y RCP8.5). Las predicciones son generadas utilizando un modelo de distribución de especies que considera variables climáticas, capacidad de dispersión y generación de propágulos (detalles de la metodología en Uribe-Rivera et al. 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
a 11. Distribución potencial de Rhinoderma darwinii en 2050 y 2080 frente a dos escenarios de cambio climático (RCP4.5 y RCP8.5). Las predicciones son generadas utilizando un modelo de distribución de especies que considera variables climáticas, capacidad de dispersión y generación de propágulos (detalles de la metodología en Uribe-Rivera et al. 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
 a 11. Distribución potencial de Rhinoderma darwinii en 2050 y 2080 frente a dos escenarios de cambio climático (RCP4.5 y RCP8.5). Las predicciones son generadas utilizando un modelo de distribución de especies que considera variables climáticas, capacidad de dispersión y generación de propágulos (detalles de la metodología en Uribe-Rivera et al. 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018).
a 11. Distribución potencial de Rhinoderma darwinii en 2050 y 2080 frente a dos escenarios de cambio climático (RCP4.5 y RCP8.5). Las predicciones son generadas utilizando un modelo de distribución de especies que considera variables climáticas, capacidad de dispersión y generación de propágulos (detalles de la metodología en Uribe-Rivera et al. 2017). Obtenido de UICN CSE Grupo Especialista en Anfibios (2018). Cabe destacar que la metodología utilizada para predecir los potenciales efectos del cambio climático sobre la distribución de R. darwinii no incorpora procesos de adaptación local, o la posibilidad de persistencia por plasticidad fenotípica de los individuos. Además, la escala espacial del análisis (celdas de ~1 km2) podría no ser suficientemente fina dada la reducida área que ocupan las subpoblaciones de esta especie, lo cual podría permitir que subpoblaciones ubicadas en áreas geográficas en que se predigan extinciones locales en el futuro (descolonización) persistan en microrefugios climáticos (escala espacial), se adapten (evolución), o simplemente modulen su comportamiento o fisiología (plasticidad fenotípica), permitiéndoles persistir a pesar de las condiciones menos adecuadas. Por otra parte, teniendo en cuenta la longevidad de esta especie (hasta 15 años en cautiverio y en vida silvestre; A. Valenzuela-Sánchez, comunicación personal), existirán subpoblaciones en que las condiciones desfavorables produzcan un efecto desfasado sobre su persistencia, estando "destinadas a la extinción" pero pudiendo tardar incluso décadas en llegar a la extirpación local de dichas subpoblaciones (Uribe-Rivera et al. 2017). Con todo esto en mente, debemos ser cautelosos al interpretar los resultados de este análisis. Estos aspectos también indican necesidades urgentes de investigación en relación con esta amenaza para las Ranitas de Darwin.
4.3.5. Tala selectiva
La tala selectiva se caracteriza por la práctica de talar los árboles de mayor tamaño y valor comercial, lo que lleva a una reducción del área basal del bosque (Pollmann 2002; Pérez et al. 2009). Dependiendo de la intensidad de la tala selectiva, esta práctica puede afectar profundamente la estructura del bosque, la composición de especies vegetales, y las características del suelo (Pérez et al. 2009). Desde la segunda mitad del siglo XIX y hasta la primera mitad del XX se produjo la tala selectiva de árboles de alto valor comercial (raulí, alerce, ciprés de la cordillera y de las Guaitecas, roble, etc.) en millones de hectáreas en los valles y zonas cordilleranas de Chile, especialmente en lugares de fácil acceso (Armesto et al. 2010). La Ley Forestal de 1931 permitió incluso la tala selectiva en Parques Nacionales, lo que resultó en la extensiva degradación del bosque templado austral en Chile (Armesto et al. 2010). El alcance de esta amenaza en la actualidad en Chile es desconocido, pero es probablemente muy alto conforme a la literatura especializada. Por ejemplo, Cruz et al. (2020) estudiaron 36 parcelas de bosque en cuencas distribuidas en la Cordillera de Los Andes, valle central, y Cordillera de la Costa de la Región de Los Ríos, detectando señales de tala selectiva en 100% de los sitios, con un nivel de intervención mayor en los sitios ubicados en la Cordillera de la Costa.
La tala selectiva podría tener un efecto negativo sobre R. darwinii ya que la abundancia de esta especie de anfibio se asocia positivamente con el área basal del bosque (Valenzuela-Sánchez et al. 2019a). La severidad de esta amenaza dependerá probablemente de la intensidad de la tala. Por ejemplo, la tala selectiva tradicional por pequeños propietarios es caracterizada por una menor remoción de árboles por área y por consiguiente menor reducción del área basal, además de menores impactos negativos en el suelo del bosque (tales como la pérdida de carbono y nitrógeno) que la tala selectiva industrial (Pérez et al. 2009). La tala selectiva se considera una amenaza potencial debido a que la evidencia de una posible afectación es indirecta.
4.3.6. Ganadería en bosque nativo
El pastoreo del ganado puede generar impactos negativos en la composición y estructura de la comunidad vegetal, reduciendo la abundancia y densidad relativa de los árboles más grandes, la biomasa vegetal, y la complejidad estructural del bosque (Stern et al. 2002, Ratovonamana et al. 2013, Li y Jiang 2021). Además, la ganadería en bosque nativo puede tener efectos negativos significativos en las poblaciones de animales que habitan zonas boscosas, como ha sido documentado en mamíferos (Schieltz y Rubenstein 2016, Li y Jiang 2021), caracoles terrestres (Denmead et al. 2015), y otros invertebrados (Didham et al. 2009). El alcance de esta amenaza en la actualidad en Chile es desconocido, pero es probablemente medio a alto, especialmente cerca de asentamientos humanos. Por ejemplo, Cruz et al. (2020) estudiaron 36 parcelas de bosque en cuencas distribuidas en la Cordillera de Los Andes, valle central, y Cordillera de la Costa de la Región de Los Ríos, detectando señales de presencia de ganado en 78% de los sitios.
Existe un número muy escaso de estudios que aborden el impacto del ganado sobre anfibios de bosque (Schieltz y Rubenstein 2016, Li y Jiang 2021), y el impacto de esta amenaza en el género Rhinoderma es desconocida. Sin embargo, la reducción de la complejidad estructural del bosque debido al pastoreo de ganado seguramente afecta negativamente la abundancia de las especies del género Rhinoderma. Por ejemplo, existe evidencia que muestra que la abundancia de R. darwinii se asocia positivamente con la complejidad estructural del bosque, siendo mayor en bosques nativos maduros con árboles de mayor diámetro y una menor variación diaria de temperatura y humedad ambiental (Valenzuela-Sánchez et al. 2019a).
El pisoteo del ganado en los bosques puede provocar además la compactación del suelo, reducción de la humedad del suelo, disminución de la hojarasca, y la disminución de invertebrados que habitan la hojarasca (Hadden y Westbrooke 1996, Didham et al. 2009, Denmead et al. 2015). Esta situación podría reducir la calidad del microhábitat, mediante una disminución en la disponibilidad refugios y alimento para los individuos de Rhinoderma spp. Además, el pisoteo del ganado podría directamente causar la destrucción de las oviposturas terrestres en estas especies, producir la muerte de individuos, y contribuir a la dispersión de patógenos como Bd en el barro que podría permanecer en las pezuñas de los animales.
La ganadería dentro de bosque nativo se considera una amenaza potencial debido a que la evidencia de una posible afectación es indirecta.
4.3.7. Especies exóticas invasoras
Las especies exóticas invasoras representan actualmente una de las principales amenazas para la biodiversidad a nivel global, incluido los anfibios, mediante la competencia o depredación sobre las especies nativas y dispersión de patógenos (Vitousek et al. 1996, Daszak et al. 2000). Por ejemplo, se hipotetiza que la rana africana (Xenopus laevis) podría haber participado en la invasión del hongo Bd en Chile (Soto-Azat et al. 2013b, Valenzuela-Sánchez et al. 2018).
El impacto de las especies exóticas invasoras sobre las especies del género Rhinoderma no ha sido estudiado. Aunque no existe evidencia directa de amenaza para Ranitas de Darwin, la presencia de especies exóticas invasoras se considera una amenaza potencial para estas especies, razón por la cual la línea de acción 2.4 del presente plan busca, aplicando el principio precautorio, colaborar en la implementación de programas de erradicación o control de especies exóticas invasoras que podrían representar una amenaza para las especies del género Rhinoderma. Estos programas, implementados en conjunto con monitoreo, podrían permitir recopilar mayor evidencia sobre el impacto de las especies invasoras sobre estas especies de anfibios. Dentro de las especies exóticas que podrían representar una potencial amenaza para el género Rhinoderma se incluyen a los salmónidos (Oncorhynchus mykiss y Salmo trutta), el jabalí euroasiático (Sus scrofa), las ratas (Rattus rattus y R. norvegicus) y el visón americano (Neovison vison) (UICN CSE Grupo Especialista en Anfibios 2018, Úbeda y Pastore 2021).
Los salmónidos son una reconocida amenaza para los anfibios en diversas partes del mundo, especialmente cuando estos han sido introducidos en lugares donde no existían naturalmente peces de características ecológicas similares (Kats y Ferrer 2003, Pilliod et al. 2010, Lobos et al. 2020). Se ha demostrado que estos peces pueden afectar negativamente a las poblaciones de anfibios en Chile (Lobos et al. 2020) y en Argentina, un ejemplo de esto es la disminución de la probabilidad de ocupación de las especies Pleurodema somuncurense y Rhinella arenarum debido a la presencia de O. mykiss en la Patagonia Argentina (Velasco et al. 2018, Kacoliris et al. 2022). Además, es importante destacar que los salmónidos y en particular, O. mykiss pueden actuar como vector de patógenos que afecten a los anfibios, tales como Saprolegnia y Ranavirus (Martín-Torrijos et al. 2016). En Chile, los salmónidos introducidos que utilizan ambientes de agua dulce se encuentran presentes desde el río Loa en la Región de Antofagasta hasta Tierra del Fuego en la Región de Magallanes en el caso de O. mykiss y desde el río Aconcagua en la Región de Valparaíso hasta Tierra del Fuego en el caso de S. trutta (Iriarte et al. 2005). Aunque el impacto específico de los salmónidos en el género Rhinoderma no ha sido estudiado, por un principio precautorio se la considera una amenaza potencial que podría ser importante solamente en R. rufum, ya que en esta especie existe una parte del desarrollo larval que ocurre en esteros. En cambio, R. darwinii es una especie completamente terrestre donde los individuos no utilizan generalmente cuerpos de agua y, por lo tanto, el encuentro de los individuos con salmónidos debe ser muy poco frecuente (Úbeda y Pastore 2021).
El jabalí ha causado impactos negativos en los ecosistemas de Chile y Argentina (Sanguinetti y Kitzberger 2010, Cuevas et al. 2012, Hernández et al. 2017). La distribución de esta especie exótica invasora en Chile abarca desde la Región de la Araucanía hasta la Región de Aysén (Skewes et al. 2007, Skewes et al. 2012). Los mecanismos en que esta especie exótica invasora podría afectar a Rhinoderma spp. son similares a los descritos para el ganado. A través de su comportamiento de búsqueda de alimento, los jabalíes alteran la hojarasca, el suelo y la vegetación (Jaksic et al. 2021a), lo que podría afectar negativamente los ambientes utilizados por Rhinoderma, además de existir un riesgo de depredación y destrucción de las oviposturas de estos anfibios.
Las ratas son depredadores oportunistas que podrían afectar negativamente a los anfibios mediante la depredación directa (Cabrera-Guzmán et al. 2015, Egeter et al. 2019) y la competencia por recursos (Lobos et al. 2023). Por ejemplo, existe evidencia de depredación de ratas sobre anfibios tales como el pollo de montaña (Leptodactylus fallax) en el Caribe (Daltry 2002). Estas especies invasoras se encuentran ampliamente distribuidas a lo largo del territorio nacional, pudiéndose encontrar en bosque nativo (Rojas et al. 2000, Lobos et al. 2005), incluidos lugares con presencia de especies del género Rhinoderma (A. Valenzuela-Sánchez, com pers).
El visón americano fue introducido en Chile en la década de 1930, y desde esa fecha ha causado diferentes impactos negativos sobre la fauna silvestre del país (Sepúlveda et al. 2014, Alfaro et al. 2021). Actualmente esta especie se encuentra distribuida en el territorio nacional entre las regiones de la Araucanía hasta Magallanes (Jaksic et al. 2021b, Zapararte et al. 2021). El visón americano podría impactar negativamente en especies de anfibios a través de depredación (Ahola et al. 2006, Jaksic et al. 2021b), aunque el impacto en Rhinoderma es desconocido.
4.3.8. Infraestructura vial
El avance de la urbanización y mejoras de la infraestructura vial pueden representar una amenaza para los anfibios, principalmente porque estas infraestructuras lineales pueden representar una barrera para la dispersión de los mismos, además de estar asociadas a mortalidad debido a atropellos (Petrovan y Schmidt 2019). Además, existe evidencia que en Alsodes pehuenche en Argentina han existido declinaciones poblacionales debido a la pavimentación de caminos, principalmente porque la construcción de estos llevó al desvío de cursos de aguas que era el lugar de reproducción de estas poblaciones (Corbalán et al. 2010, Corbalán et al. 2023).
Chile cuenta con una extensa red vial, la cual se encuentra en constante crecimiento (Ministerio de Obras Publicas 2021). Por ejemplo, según las estadísticas del Ministerio de Obras Públicas la red vial creció de 79.593 km en 1990 a 88.267 km en 2023. Existe una notoria variación geográfica en la densidad vial a lo largo de la distribución de las especies del género Rhinoderma (Ministerio de Obras Públicas de Chile 2020). Por ejemplo, las regiones de Aysén y del Maule muestran las menores densidades viales, mientras que las regiones de La Araucanía y del Biobío muestran densidades viales que pueden ser un orden de magnitud mayores (Tabla 6). El Plan Nacional de Infraestructura para la Movilidad 2020-2050 propone la construcción adicional de 19.752 km de caminos y carreteras públicas entre los años 2020 y 2050. Bajo este escenario, la densidad vial aumentará en todas las regiones con presencia de Rhinoderma spp., siendo el porcentaje de incremento mayor en las regiones que poseen una menor densidad vial en la actualidad (Tabla 6a).
Tabla 6a. Distribución de infraestructura vial a lo largo de la distribución de las Ranitas de Darwin. Se muestra la densidad vial (coeficiente entre kilómetros pavimentados y superficie a nivel regional) por región administrativa antes y después de implementar el Plan Nacional de Infraestructura para la Movilidad 2020-2050 del Ministerio de Obras Públicas, Gobierno de Chile. Las regiones han sido ordenadas de menor a mayor según su valor de densidad vial durante el 2020
Aun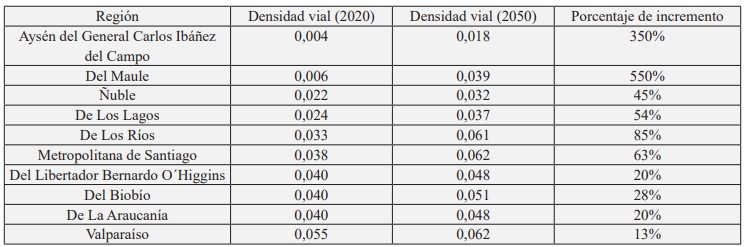 que el impacto de la infraestructura vial sobre las especies del género Rhinoderma es desconocido, dada la ausencia de estudios específicos, se la incluye, de manera precautoria, como una amenaza potencial para priorizar el desarrollo de evaluaciones o estudios que permitan estimar el posible de impacto. Sin embargo, se espera que esta amenaza sea más importante en especies que realizan migraciones estacionales masivas, donde un gran porcentaje de la población adulta realiza movimientos anuales hacia pozas o lagunas de reproducción, y luego de la estación reproductiva, tanto adultos como juveniles retornan hacia los sitios no reproductivos tales como bosques o praderas, teniendo que atravesar caminos y carreteras durante este proceso de migración (un proceso ecológico conocido como complementación de hábitat; Schmidt y Zumbach 2008, Becker et al. 2010, Schmidt et al. 2020). Este tipo de comportamiento de migración no ocurre en las especies del género Rhinoderma. Las infraestructuras viales podrían aún representar una amenaza importante para las especies de Rhinoderma mediante una disminución de la dispersión entre poblaciones, la que de manera natural es muy limitada en Rhinoderma (Valenzuela-Sánchez et al. 2014, 2019b). El impacto de esta amenaza dependerá probablemente de las características físicas del camino (p. ej. ancho, material, presencia de zanjas) y del flujo vehicular. Por ejemplo, caminos de ripio angostos y de bajo flujo vehicular probablemente no representarán una barrera importante para la dispersión en estas especies.
que el impacto de la infraestructura vial sobre las especies del género Rhinoderma es desconocido, dada la ausencia de estudios específicos, se la incluye, de manera precautoria, como una amenaza potencial para priorizar el desarrollo de evaluaciones o estudios que permitan estimar el posible de impacto. Sin embargo, se espera que esta amenaza sea más importante en especies que realizan migraciones estacionales masivas, donde un gran porcentaje de la población adulta realiza movimientos anuales hacia pozas o lagunas de reproducción, y luego de la estación reproductiva, tanto adultos como juveniles retornan hacia los sitios no reproductivos tales como bosques o praderas, teniendo que atravesar caminos y carreteras durante este proceso de migración (un proceso ecológico conocido como complementación de hábitat; Schmidt y Zumbach 2008, Becker et al. 2010, Schmidt et al. 2020). Este tipo de comportamiento de migración no ocurre en las especies del género Rhinoderma. Las infraestructuras viales podrían aún representar una amenaza importante para las especies de Rhinoderma mediante una disminución de la dispersión entre poblaciones, la que de manera natural es muy limitada en Rhinoderma (Valenzuela-Sánchez et al. 2014, 2019b). El impacto de esta amenaza dependerá probablemente de las características físicas del camino (p. ej. ancho, material, presencia de zanjas) y del flujo vehicular. Por ejemplo, caminos de ripio angostos y de bajo flujo vehicular probablemente no representarán una barrera importante para la dispersión en estas especies.
 que el impacto de la infraestructura vial sobre las especies del género Rhinoderma es desconocido, dada la ausencia de estudios específicos, se la incluye, de manera precautoria, como una amenaza potencial para priorizar el desarrollo de evaluaciones o estudios que permitan estimar el posible de impacto. Sin embargo, se espera que esta amenaza sea más importante en especies que realizan migraciones estacionales masivas, donde un gran porcentaje de la población adulta realiza movimientos anuales hacia pozas o lagunas de reproducción, y luego de la estación reproductiva, tanto adultos como juveniles retornan hacia los sitios no reproductivos tales como bosques o praderas, teniendo que atravesar caminos y carreteras durante este proceso de migración (un proceso ecológico conocido como complementación de hábitat; Schmidt y Zumbach 2008, Becker et al. 2010, Schmidt et al. 2020). Este tipo de comportamiento de migración no ocurre en las especies del género Rhinoderma. Las infraestructuras viales podrían aún representar una amenaza importante para las especies de Rhinoderma mediante una disminución de la dispersión entre poblaciones, la que de manera natural es muy limitada en Rhinoderma (Valenzuela-Sánchez et al. 2014, 2019b). El impacto de esta amenaza dependerá probablemente de las características físicas del camino (p. ej. ancho, material, presencia de zanjas) y del flujo vehicular. Por ejemplo, caminos de ripio angostos y de bajo flujo vehicular probablemente no representarán una barrera importante para la dispersión en estas especies.
que el impacto de la infraestructura vial sobre las especies del género Rhinoderma es desconocido, dada la ausencia de estudios específicos, se la incluye, de manera precautoria, como una amenaza potencial para priorizar el desarrollo de evaluaciones o estudios que permitan estimar el posible de impacto. Sin embargo, se espera que esta amenaza sea más importante en especies que realizan migraciones estacionales masivas, donde un gran porcentaje de la población adulta realiza movimientos anuales hacia pozas o lagunas de reproducción, y luego de la estación reproductiva, tanto adultos como juveniles retornan hacia los sitios no reproductivos tales como bosques o praderas, teniendo que atravesar caminos y carreteras durante este proceso de migración (un proceso ecológico conocido como complementación de hábitat; Schmidt y Zumbach 2008, Becker et al. 2010, Schmidt et al. 2020). Este tipo de comportamiento de migración no ocurre en las especies del género Rhinoderma. Las infraestructuras viales podrían aún representar una amenaza importante para las especies de Rhinoderma mediante una disminución de la dispersión entre poblaciones, la que de manera natural es muy limitada en Rhinoderma (Valenzuela-Sánchez et al. 2014, 2019b). El impacto de esta amenaza dependerá probablemente de las características físicas del camino (p. ej. ancho, material, presencia de zanjas) y del flujo vehicular. Por ejemplo, caminos de ripio angostos y de bajo flujo vehicular probablemente no representarán una barrera importante para la dispersión en estas especies. 4.3.9. Otras amenazas
Existen otras amenazas descritas para las especies del género Rhinoderma que no fueron consideradas como críticas durante la elaboración de este plan, incluyendo la extracción de individuos y las erupciones volcánicas.
La extracción de individuos de Rhinoderma spp. para museos o para abastecer el comercio ilegal de mascotas hacia Estados Unidos y Europa fue una práctica común en el pasado, al menos hasta la década de los años 80' (Ortiz 1988 Soto-Azat et al. 2013a), pero no representaría una amenaza actual para estas especies. Por ejemplo, Soto-Azat et al. (2013a) documentaron la presencia de 838 individuos de R. rufum depositados en diferentes museos (principalmente en Europa y Estados Unidos). Más aún, en el Museo de Zoología de Hamburgo, existe un frasco que contiene 188 individuos de R. rufum, los cuales fueron recolectados en solo dos jornadas de colecta en Chiguayante en 1975. Paralelamente uno de los sitios más afectados por la extracción de individuos de R. darwinii fue el Parque Nacional Nahuelbuta (Soto-Azat et al. 2013a).
Las erupciones volcánicas podrían representar algún riesgo para poblaciones locales pequeñas y aisladas de R. darwinii en Argentina y Chile (Úbeda y Pastore 2021). Por ejemplo, entre 2008 y 2012 dos erupciones volcánicas de gran magnitud afectaron poblaciones locales de R. darwinii (Soto-Azat et al. 2013a). La erupción del volcán Chaitén, en la Región de Los Lagos, Chile, se asoció con la aparente extinción de una población local ubicada a 22 km del cráter en un sendero del Parque Pumalín, sector El Amarillo (Soto-Azat et al. 2013a), aunque existen registros anecdóticos de individuos de la especie en años recientes en esa zona (A. Valenzuela-Sánchez, comunicación personal). Adicionalmente, la erupción del volcán Caulle-Puyehue se asoció con una disminución aparente en la abundancia de individuos de R. darwinii en una población local en el Parque Nacional Puyehue (Soto-Azat et al. 2013a), sin causar la extinción local de la especie en la zona.
5. Actores relevantes para la implementación del plan
En la Tabla 6b detallamos los actores clave. Estos son definidos como toda persona, grupo, o institución con capacidad de influir sobre los objetos de conservación y que podrían verse afectados por las acciones de este plan, y que son indispensables para alcanzar los objetivos y metas del plan (Conservation Measures Partnerships 2020).
Tabla 6b. Actores claves para la implementación del Plan RECOGE de las Ranitas de Darwin
6. V isión del plan
isión del plan
 isión del plan
isión del plan Las Ranitas de Darwin, únicas en el mundo por su particularidad reproductiva, son conservadas y valoradas por la sociedad como un emblema para la protección de los bosques nativos de Chile.
7. Alcance del plan
El plan RECOGE de las Ranitas de Darwin tendrá como alcance geográfico la distribución histórica completa de ambas especies de Ranitas de Darwin en Chile. Esto es, la Cordillera de la Costa entre Zapallar y Concepción, y la extensión completa de Chile entre Concepción y las cercanías de Puerto Aysén (Figura 12).
Administrativamente, esto incluye las siguientes regiones: Región de Valparaíso, Región Metropolitana de Santiago, Región del Libertador General Bernardo O'Higgins, Región del Maule, Región de Ñuble, Región del Biobío, Región de La Araucanía, Región de Los Ríos, Región de Los Lagos, Región de Aysén del General Carlos Ibáñez del Campo.
Figur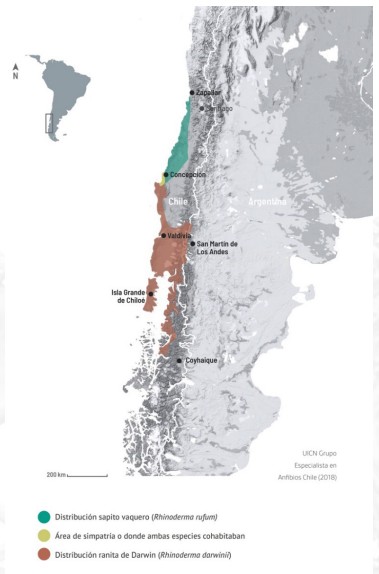 a 12. Distribución geográfica histórica de las especies de Ranitas de Darwin. El alcance geográfico de este Plan RECOGE es toda el área de distribución de ambas especies, incluida la zona de simpatría. Fuente: Elaboración propia en función de lo publicado en la Lista Roja de la UICN.
a 12. Distribución geográfica histórica de las especies de Ranitas de Darwin. El alcance geográfico de este Plan RECOGE es toda el área de distribución de ambas especies, incluida la zona de simpatría. Fuente: Elaboración propia en función de lo publicado en la Lista Roja de la UICN.
 a 12. Distribución geográfica histórica de las especies de Ranitas de Darwin. El alcance geográfico de este Plan RECOGE es toda el área de distribución de ambas especies, incluida la zona de simpatría. Fuente: Elaboración propia en función de lo publicado en la Lista Roja de la UICN.
a 12. Distribución geográfica histórica de las especies de Ranitas de Darwin. El alcance geográfico de este Plan RECOGE es toda el área de distribución de ambas especies, incluida la zona de simpatría. Fuente: Elaboración propia en función de lo publicado en la Lista Roja de la UICN. 8. Meta del plan
Rhinoderma rufum
Dentro del plazo de 15 años de implementación del plan, se identifica la presencia de al menos una población local de R. rufum, y el tamaño total de la población de la especie se encuentra en 51 a 249 individuos maduros, rango calificado como regular.
Nota explicativa: los atributos considerados para la meta planteada, en función de los atributos ecológicos clave e indicadores definidos para los objetos de conservación se aprecian en la Tabla 2 (subsección 3.6.3).
Rhinoderma darwinii
Dentro del plazo de 15 años de implementación del plan, el área de ocupación de R. darwinii se encuentra entre 500 y 1.999 km2, lo que califica en una condición de "bueno".
Nota explicativa: alcanzar la meta planteada, en función de los atributos ecológicos clave e indicadores definidos para los objetos de conservación (Tabla 2; subsección 3.6.3), significa que la especie podría ser recategorizada desde En Peligro a Vulnerable, asumiendo que los mismos criterios actuales de la Lista Roja de la UICN utilizados para su recategorización.
9. Objetivos del plan
Objetivo 1. Controlar y mitigar el impacto de las amenazas que afectan a las poblaciones del género Rhinoderma.
Objetivo 2. Fortalecer la conservación de las Ranitas de Darwin a través de la protección de sus poblaciones, la restauración de su hábitat, la investigación aplicada y la educación de la comunidad.
Objetivo 3. Contar con instancias que permitan la coordinación entre servicios y organizaciones, y con el financiamiento para el desarrollo de acciones.
10. Estructura del plan de acción
En esta sección se presentan las acciones del plan. En la Tabla 7 se expone un resumen de las líneas de acción por objetivo con los indicadores de seguimiento y métricas que serán utilizadas para verificar el éxito de la implementación de las acciones del plan. Luego, en la Tabla 8 se presenta cada acción en detalle, incluyendo coordinador, colaboradores, inicio, duración y productos asociados a cada acción.
Tabla 7. Resumen de las líneas de acción e indicadores de seguimiento de las acciones del Plan RECOGE de las Ranitas de Darwin
__________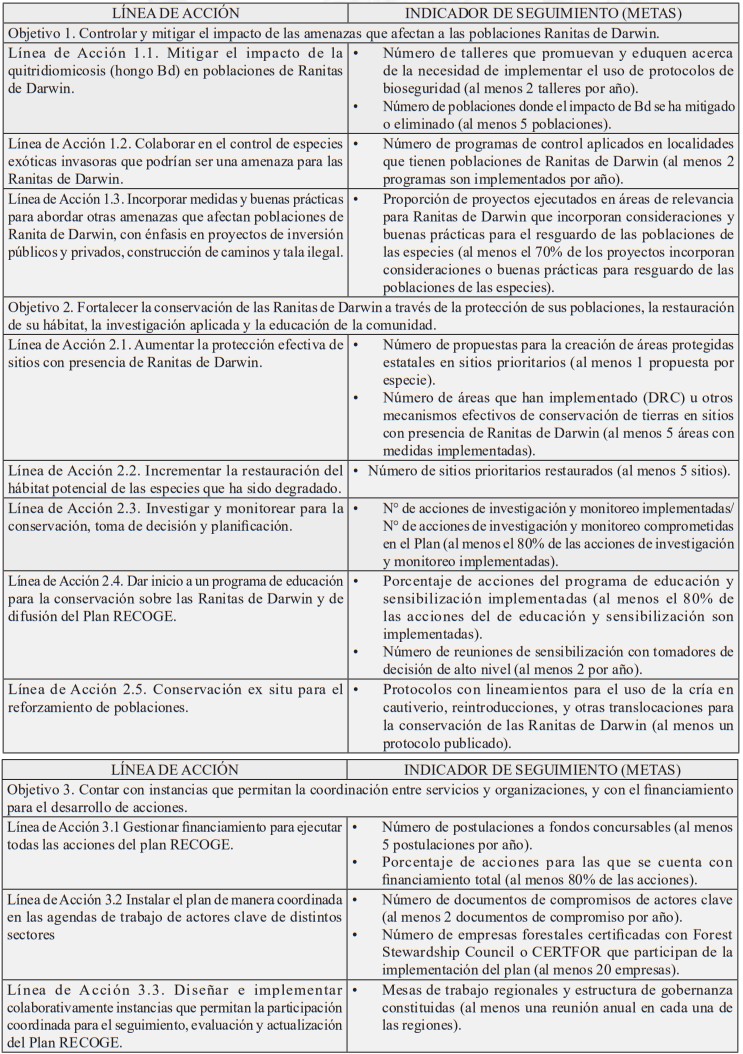 _________
_________
 _________
_________(11) ORD es el responsable en atención de su capacidad técnica y conocimiento científico especializado en investigación de quitridiomicosis y su efecto sobre Ranitas de Darwin, con casi una década de estudio y monitoreo en este ámbito. Posee la capacidad y la factibilidad de responsabilizarse de la acción.
(12) ORD es el responsable en atención de su capacidad técnica y conocimiento científico especializado en investigación de quitridiomicosis y su efecto sobre Ranitas de Darwin. Posee la capacidad y la factibilidad de responsabilizarse de la acción, la que ya viene ejecutando.
(13) UNAB es el responsable en atención de su capacidad técnica y conocimiento científico especializado en modelos de distribución de ranita de Darwin, tienen la factibilidad siendo un ámbito de trabajo que ya viene ejecutando.
(14) UCH es el responsable en atención de su capacidad técnica y conocimiento científico especializado en genética, tienen la factibilidad siendo un ámbito de trabajo que ya viene ejecutando desde el Laboratorio de Genética y Evolución.
(15) Arauco posee la capacidad y factibilidad de ser responsable de esta acción, en consideración de su conocimiento especializado en los estándares de certificación y relación con otras empresas forestales.
Tabla 8. Acciones del Plan RECOGE de las Ranitas de Darwin
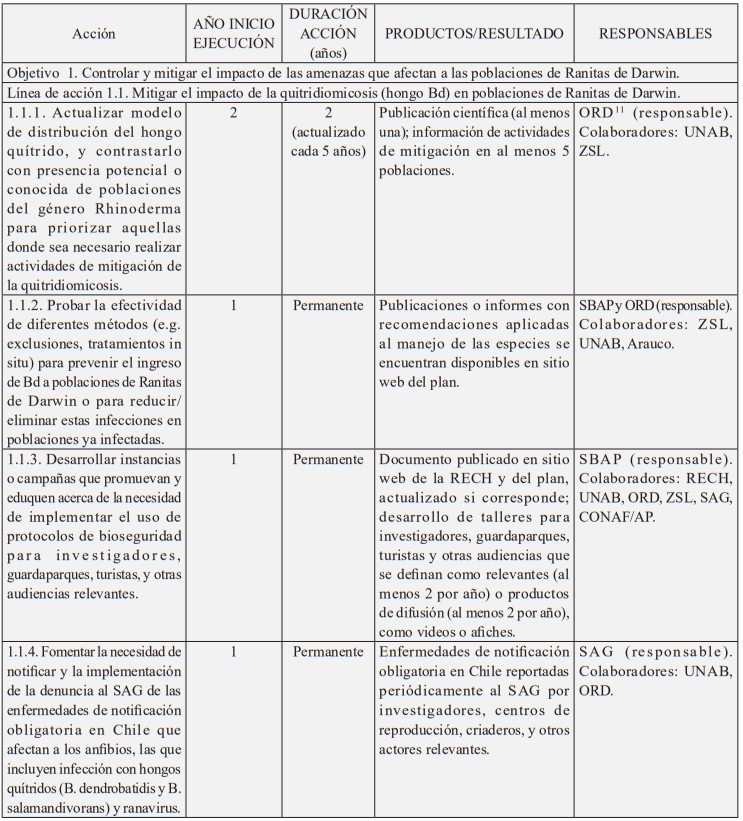
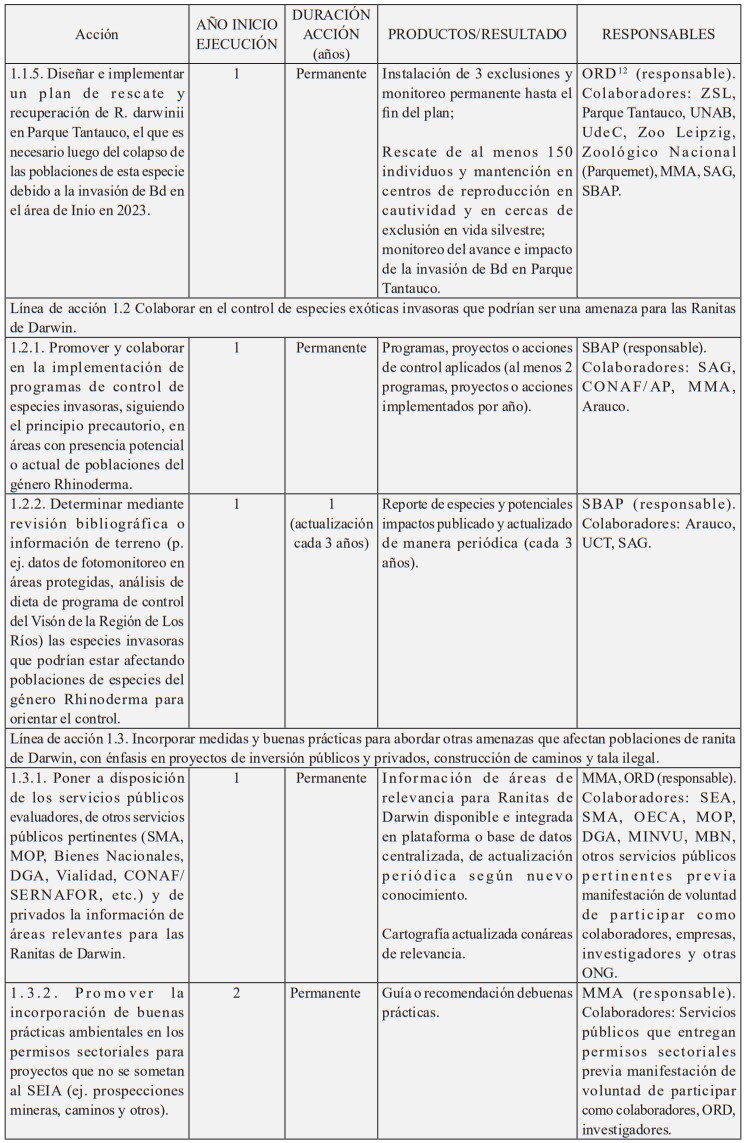 A
A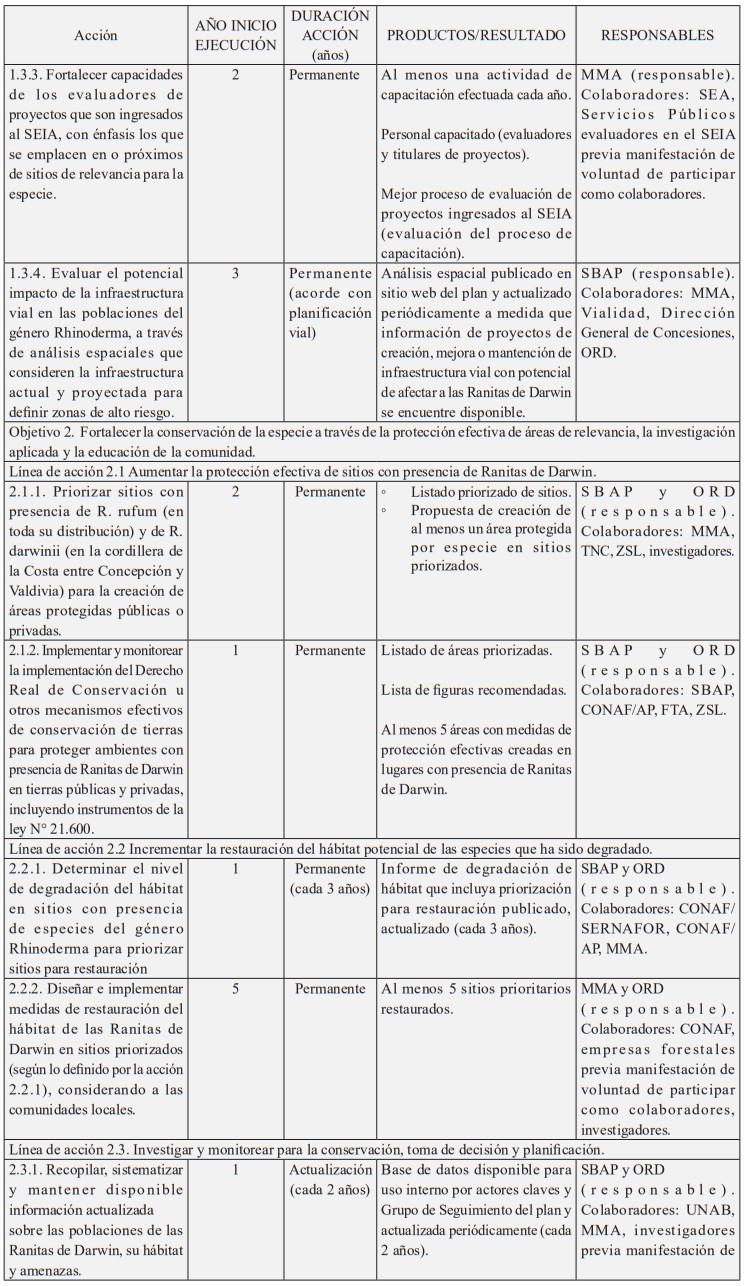 R
R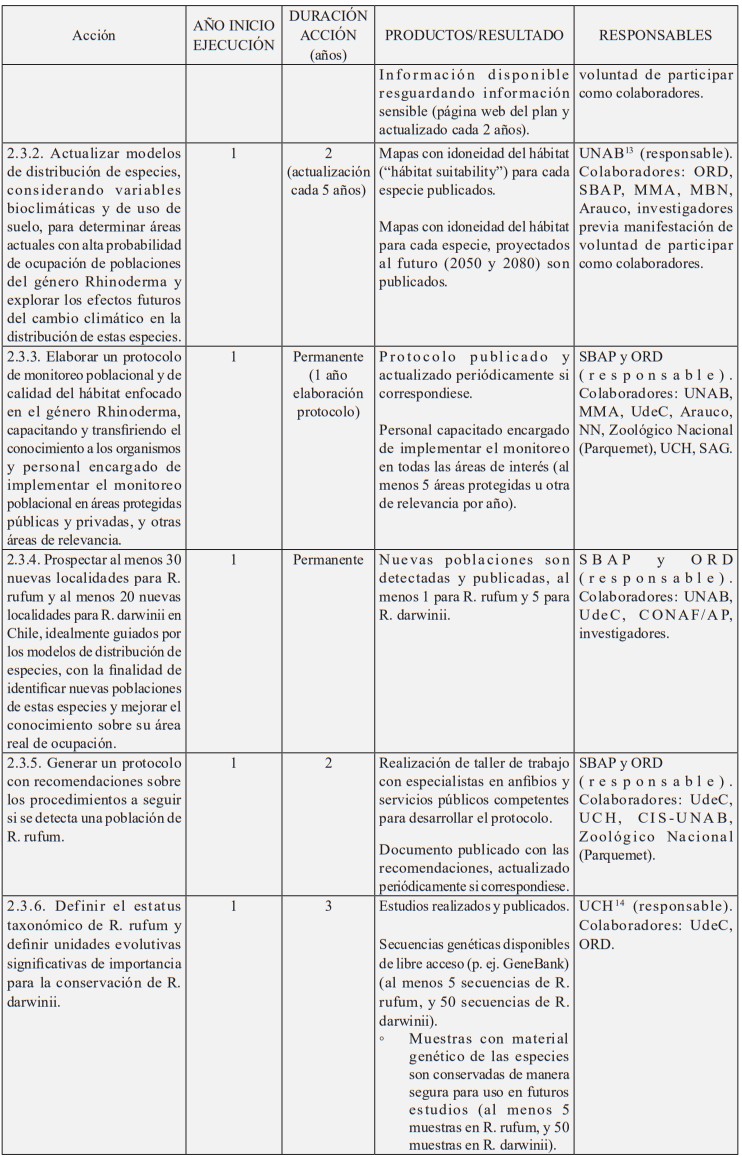 A
A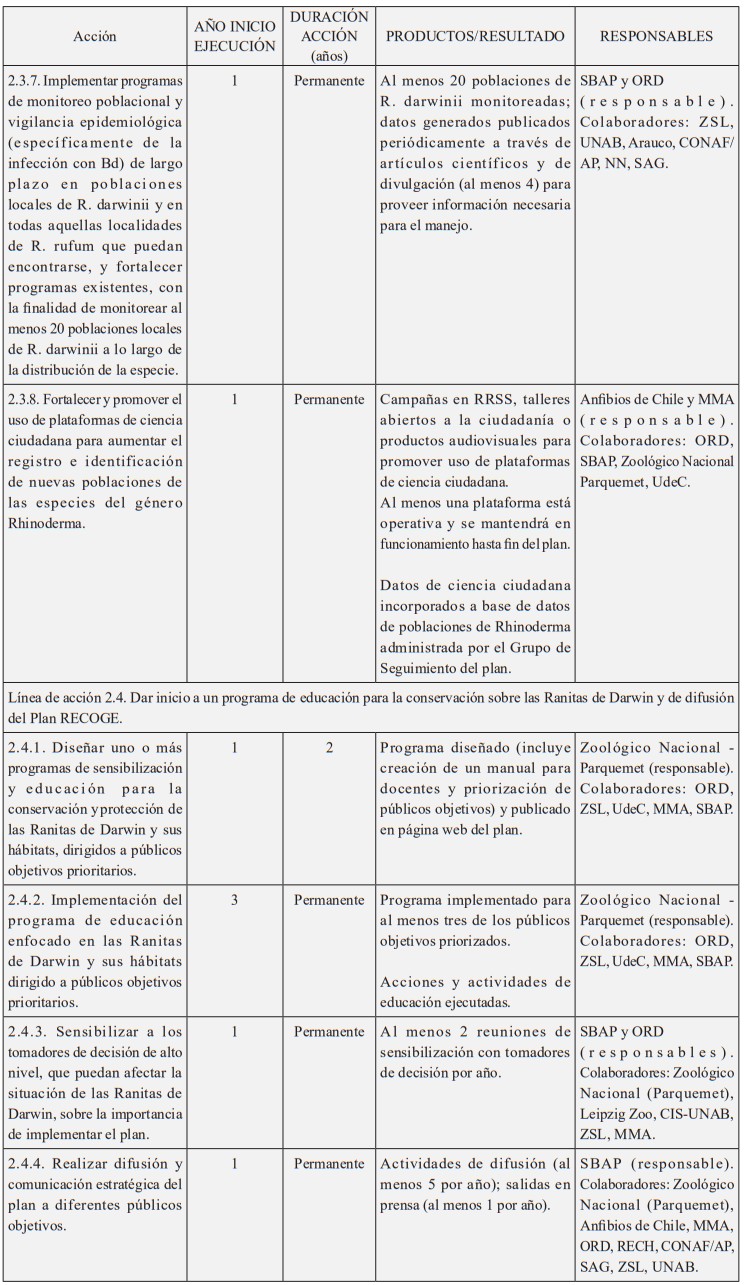 U
U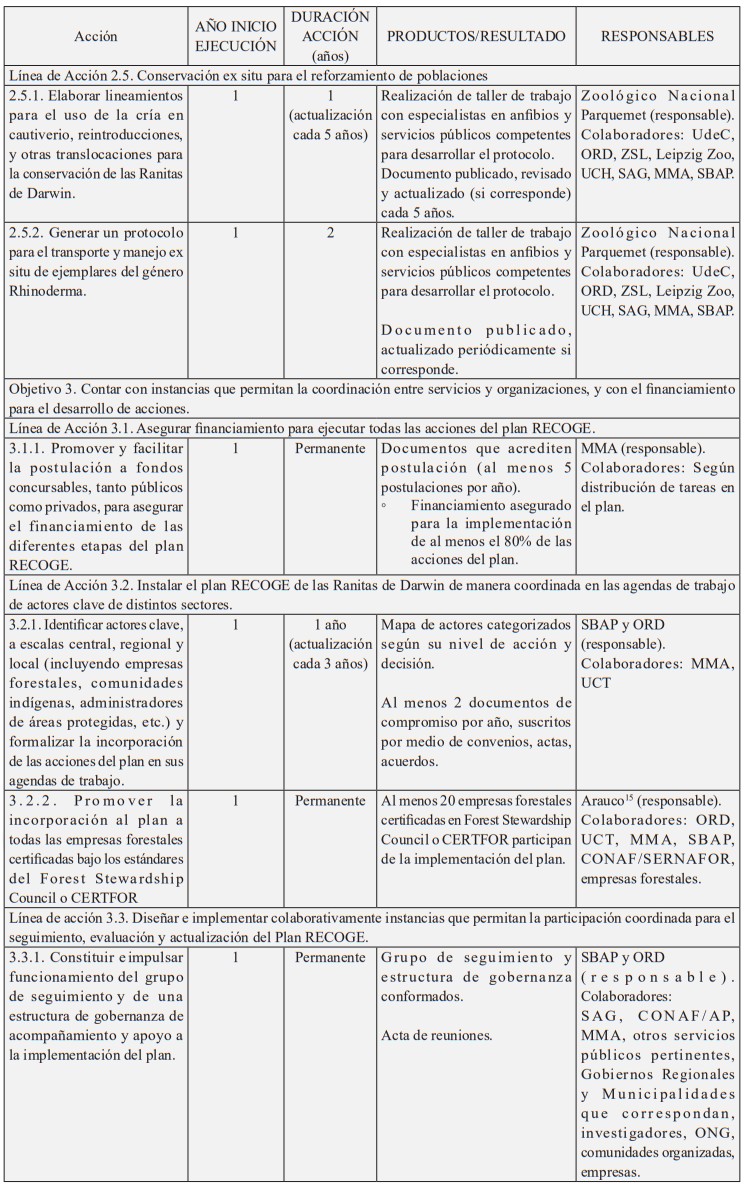 CO = Forestal Arauco
CO = Forestal Arauco UNAB = Instituto One Health, Universidad Andrés Bello
CONAF/AP = Corporación Nacional Forestal, Programa de Áreas Protegidas
CONAF/SERNAFOR = Corporación Nacional Forestal, área forestal
FTA = Fundación Tierra Austral
MMA = Ministerio del Medio Ambiente
MOP = Ministerio de Obras Públicas
DGA = Dirección General de Aguas
MBN = Ministerio de Bienes Nacionales
NN = Agrupación Nahuelbuta Natural
ORD = Asociación Ranita de Darwin
RECH = Asociación Red Chilena de Herpetología
SAG = Servicio Agrícola Ganadero
SBAP = Servicio de Biodiversidad y Áreas Protegidas
TNC = The Nature Conservancy - Chile
UC = Facultad de Medicina, Pontificia Universidad Católica de Chile
UCH = Laboratorio de Genética y Evolución, Facultad de Ciencias, Universidad de Chile
UCT = Departamento de Ciencias Biológicas y Químicas, Facultad de Recursos Naturales, Universidad Católica de Temuco
UdeC = Departamento de Zoología, Facultad de Ciencias Naturales y Oceanográficas, Universidad de Concepción
ZSL = Sociedad Zoológica de Londres, Reino Unido
Nota: Dada la publicación de la ley N° 21.600 que crea el Servicio de Biodiversidad y Áreas Protegidas (SBAP) y el Sistema Nacional de Áreas Protegidas, el rol y/o responsabilidad en las acciones señaladas, deberá ajustarse al ejercicio de las competencias del SBAP una vez que éste entre en operaciones, conforme a lo establecido en el artículo 5°, letra e), de la mencionada ley N° 21.600, y sin perjuicio de lo que disponga el reglamento a que hace referencia el inciso segundo del artículo 42 del referido cuerpo legal. Asimismo, se ha considerado el Ministerio del Medio Ambiente como institución colaboradora en aquellas acciones que serán posteriormente coordinadas por el SBAP y en las que posee competencias conforme al artículo 70 de la ley N° 19.300.
11. Grupo de Seguimiento y proceso de evaluación de la implementación del plan
El Grupo de Seguimiento tiene como función realizar el seguimiento de las acciones comprometidas para el éxito del plan según lo señalado en el procedimiento y periodos de evaluación de la implementación del plan, debiendo además, velar porque en la implementación del presente plan se considere, y tenga a la vista, la sinergia con las diversas políticas y estrategias públicas que en materia ambiental se han dictado, promoviendo además la colaboración entre el sector público, privado y la sociedad civil.
El grupo de seguimiento para el Plan RECOGE de las Ranitas de Darwin estará conformado por:
. Ministerio del Medio Ambiente, incluidos representantes del SBAP
. Asociación Ranita de Darwin
. Zoológico Nacional del Parque Metropolitano de Santiago
. Servicio Agrícola y Ganadero
La coordinación general del Grupo de Seguimiento estará a cargo del Servicio de Biodiversidad y Áreas Protegidas, con el apoyo de la Asociación Ranita de Darwin. El Grupo de Seguimiento sesionará al menos una vez por año para evaluar el estado de avance de implementación de las acciones descritas en el presente plan. La obligación de reportar el avance de la implementación de cada actividad recaerá en el coordinador de cada actividad según lo especificado en la Tabla 8 del presente plan (sección 10).
El presente plan se implementará en un periodo de 15 años a contar desde su aprobación. El Grupo de Seguimiento evaluará cada 5 años, o en una fecha diferente si así lo estimase conveniente, la actualización de las líneas de acción y acciones descritas en la Tabla 8 del presente documento, siempre y cuando esta actualización sea concordante con la visión, meta, y objetivos definidos para el presente plan.
Una vez que el Servicio de Biodiversidad y Áreas Protegidas se encuentre en operaciones y comience a ejercer sus competencias legales asociadas a los planes de recuperación, conservación y gestión de especies, conforme a lo dispuesto en el artículo 5°, letra e), de la ley N° 21.600, el seguimiento del presente plan será de responsabilidad del referido Servicio, sin perjuicio de lo que disponga el reglamento a que se refiere el inciso segundo del artículo 42 del referido cuerpo legal.
12. Costo estimado para la implementación del plan
En la Tabla 9 se presenta el presupuesto necesario para la implementación de la totalidad de las acciones del Plan RECOGE de las Ranitas de Darwin, el que ha sido estimado para cada una de las acciones por los coordinadores de estas. El total del presupuesto estimado asciende a $6.729.418 dólares americanos. El 50% de este valor corresponde a la implementación de una única línea de acción relacionada con la restauración de hábitat de las Ranitas de Darwin (línea de acción 2.2). Es importante destacar que estos son los costos estimados para la implementación del plan durante los 15 años de duración. El costo anual aproximado sería $448.628 dólares americanos.
La tasa de cambio utilizada se basa en el valor del dólar americano promedio entre enero 2023 y julio 2024 (1 dólar = 876,7 pesos chilenos).
Tabla 9. Presupuesto necesario para la implementación del Plan RECOGE de las Ranitas de Darwin durante sus 15 años de duración
13. 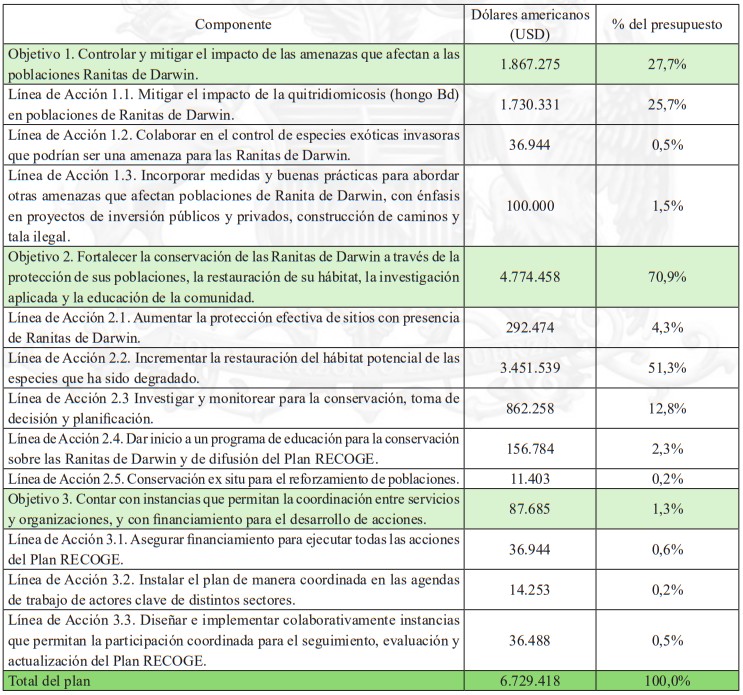 Referencia bibliográficas
Referencia bibliográficas
 Referencia bibliográficas
Referencia bibliográficas Abom, R., & Schwarzkopf, L. (2016). Short-term responses of reptile assemblages to fire in native and weedy tropical savannah. Global Ecology and Conservation, 6, 58-66.
Ahola, M., Nordström, M., Banks, P.B., Laanetu, N., & Korpimäki, E. (2006). Alien mink predation induces prolonged declines in archipelago amphibians. Proceedings of the Royal Society B: Biological Sciences, 273(1591), 1261-1265.
Alfaro, M.A.S., Raffo, E., Bustos, M.I., Tomckowiack, C., Tejeda, C., Collado, L., & Medina-Vogel, G. (2021). New insights on the infection of pathogenic Leptospira species in American mink (Neovison vison) in southern Chile. Tropical Animal Health and Production, 53, 1-6.
Alvarado-Rybak, M., Acuña, P., Peñafiel-Ricaurte, A., Sewell, T. R., O'Hanlon, S.J., Fisher, M.C., Valenzuela-Sánchez, A., Cunningham, A.A., & Azat, C. (2021). Chytridiomycosis Outbreak in a Chilean Giant Frog (Calyptocephalella gayi) Captive Breeding Program: Genomic Characterization and Pathological Findings. Frontiers In Veterinary Science, 8. https://doi.org/10.3389/fvets.2021.733357
Arismendi, I., Penaluna, B.E., Dunham, J.B., García de Leaniz, C., Soto, D., Fleming, I.A., ... & León-Muñoz, J. (2014). Differential invasion success of salmonids in southern Chile: patterns and hypotheses. Reviews in Fish Biology and Fisheries, 24, 919-941.
Armesto, J.J., Manuschevich, D., Mora, A., Smith-Ramirez, C., Rozzi, R., Abarzúa, A.M., & Marquet, P.A. (2010). From the Holocene to the Anthropocene: A historical framework for land cover change in southwestern South America in the past 15,000 years. Land Use Policy, 27(2), 148-160. https://doi.org/10.1016/j.landusepol.2009.07.006
Azat, C., & Valenzuela-Sanchez, A. (2021). Rhinoderma darwinii (Green Status Assessment). The IUCN Red List of Threatened Species 2021.
Azat, C., Valenzuela-Sánchez, A., Delgado, S., Cunningham, A.A., Alvarado-Rybak, M., Bourke, J., Briones, R., Cabeza, O., Castro-Carrasco, C., Charrier, A., Correa, C., Crump, M.L., Cuevas, C.C., De la Maza, M., Díaz-Vidal, S., Flores, E., Harding, G., Lavilla, E.O., Mendez, M.A., ... Angulo, A. (2021). A flagship for Austral temperate forest conservation: an action plan for Darwin's frogs brings key stakeholders together. Oryx, 55(3), 356-363. https://doi.org/10.1017/s0030605319001236
Bacigalupe, L.D., Soto‐Azat, C., García‐Vera, C., Barría‐Oyarzo, I., & Rezende, E. L. (2017). Effects of amphibian phylogeny, climate and human impact on the occurrence of the amphibian‐killing chytrid fungus. Global Change Biology, 23(9), 3543-3553. https://doi.org/10.1111/gcb.13610
Bacigalupe, L.D., Vásquez, I.A., Estay, S.A., Valenzuela‐Sánchez, A., Alvarado‐Rybak, M., Peñafiel‐Ricaurte, A., Cunningham, A. A., & Soto‐Azat, C. (2019). The amphibian‐killing fungus in a biodiversity hotspot: identifying and validating high‐risk areas and refugia. Ecosphere, 10(5). https://doi.org/10.1002/ecs2.2724
Barros, R. (1918). Notas sobre el <<sapito vaquero>> (Rhinoderma darwinii Dum. y Bibron). Revista Chilena de Historia Natural, 22.
Becker, C.G., Loyola, R. D., Haddad, C.F.B., & Zamudio, K.R. (2010). Integrating species life‐history traits and patterns of deforestation in amphibian conservation planning. Diversity and Distributions, 16(1), 10-19.
Bidart Enríquez, G. (2021). ¿Qué está desaparecido, poblaciones o una especie? Antiguas grabaciones de llamadas revelan similitud entre las dos presuntas especies de Ranita de Darwin. Tesis de pregrado. Universidad de Chile, Facultad de Ciencias, Santiago, Chile. Disponible en: https://repositorio.uchile.cl/handle/2250/179712
Bourke, J. (2012). Darwin's frogs: ecology and conservation in Chile (Anura: Rhinodermatidae) [Tesis de Doctorado (Dr. rer. nat.),]. Universidad de Bonn, Alemania.
Bourke, J., Barrientos, C., Ortiz, JC., Busse, K., Böhme, W., & Bakker, TC. (2011b). Colour change in Darwin's frogs (Rhinoderma darwinii, Duméril and Bibron, 1841) (Anura: Rhinodermatidae). Journal of Natural History 45: 2661-2668.
Bourke, J., Busse, K., & Böhme, W. (2012). Searching for a lost frog (Rhinoderma rufum): identification of the most promising areas for future surveys and possible reasons of its enigmatic decline. North-Western Journal of Zoology 8: 99-106.
Bourke, J., Busse, K., & Böhme, W. (2018). Potential effects of climate change on the distribution of the endangered Darwin's frog. North-Western Journal of Zoology 2018: e171508.
Bourke, J., Busse, KC., & Bakker TM. (2011a). Sex differences in polymorphic body coloration and dorsal pattern in Darwin's frogs (Rhinoderma darwinii). Herpetological Journal 21: 227-234.
Bourke, J., Mutschmann, F., Ohst, T., Ulmer, P., Gutsche, A., Busse, K., Werning, H., & Boehme, W. (2010). Batrachochytrium dendrobatidis in Darwin's frog Rhinoderma spp. in Chile. Disease s Of Aquatic Organisms, 92(3), 217-221. https://doi.org/10.3354/dao02239
Bürger, O. (1905). La Neomelia de la Rhinoderma darwinii D. y B. Memorias Científicas I Literarias, Imprenta Cervantes, 585-604.
Busse, K. (1970). Care of the young by male Rhinoderma darwinii. Copeia, 2, 395.
Busse, K. (2002). Darwin's Frogs in Danger; Rhinoderma, Are there any Rhinoderma rufum left in Chile? Reptilia, 25, 63-67.
Busse, K. (2004). Biología de la reproducción del Sapito de Darwin (Rhinoderma darwinii) y su cría en cautividad. En A. Iriarte, C. Tala, B. González, B. Zapata, G. González, & M. Maino (Eds.), Cría en Cautividad de Fauna Chilena (pp. 139-146). Servicio Agrícola Ganadero, Santiago, Chile.
Cabeza-Alfaro, O., Valenzuela-Sánchez, A., Alvarado-Rybak, M., Serrano, J.M., & Azat, C. (2021). First case of male alloparental care in amphibians: tadpole stealing in Darwin's frogs. Endangered Species Research, 45, 331-335.
Cabrera-Guzmán, E., Crossland, M.R., Pearson, D., Webb, J.K., & Shine, R. (2015). Predation on invasive cane toads (Rhinella marina) by native Australian rodents. Journal of Pest Science, 88, 143-153.
Cayuela, H., Valenzuela-Sánchez, A., Teulier, L., Martínez-Solano, Í., Léna, J.-P., Merilä, J., Muths, E., Shine, R., Quay, L., Denoël, M., Clobert, J., & Schmidt, B.R. (2020). Determinants and consequences of dispersal in vertebrates with complex life cycles: A review of pond-breeding amphibians. The Quarterly Review of Biology, 95, 1-36.
Cei, J.M. (1958). Las láminas originales del suplemento a los Batraquios chilenos de Phillipi: Primera impresión y comentarios. Investigaciones Zoológicas Chilenas, 4, 245.
Cei, J.M. (1962). Batracios de Chile. Editorial Universidad de Chile, Santiago, Chile.
Chancellor, G., & Van Wyhe, J. (2009). Charles Darwin's notebooks from the voyage of the Beagle. Cambridge University Press, Cambridge, Reino Unido.
Conservation Measures Partnership (2020). Download Conservation Standards. Version 4.0. Conservation Measures Partnership-Open Standards for the Practice of Conservation. https://conservationstandards.org/download-cs/
Corbalán, V.E., Debandi, G., Literas, S., Alvarez Guerrero, L.M., Rivera, J.A., Dopazo, J.E., ... & Masiel, D. (2023). Newly Discovered Sites and Potential Threats for the Critically Endangered Frog, Alsodes pehuenche, in Southern South America. Herpetological Conservation and Biology, 18(1):48-56.
Corbalán, V., Debandi, G., & Martínez, F. (2010). Alsodes pehuenche (Anura: Cycloramphidae): Past, present and future. Cuadernos de herpetología, 24(1), 17-23.
Corporación Nacional Forestal (Conaf). (2017). Catastro y Evaluación de los Recursos Vegetacionales Nativos de Chile. Disponible en: http://www.conaf.cl/nuestros-bosques/bosques-en-chile/catastro-vegetacional/ .
Crump, M.L. (2002). Natural history of Darwin's frog Rhinoderma darwinii. Herpetological Natural History, 9, 21-31.
Crump, M.L., & Veloso, A. (2005). El aporte de observaciones de terreno y del análisis genético para la conservación de Rhinoderma darwinii en Chile. En C. Smith-Ramirez, J.J. Armesto, & C. Valdovinos (Eds.), Historia, Biodiversidad y Ecología de los Bosques Costeros de Chile (pp. 452-455). Editorial Universitaria, Santiago, Chile.
Cuevas, C.C. (2014). Native forest loss impacts on anuran diversity: With focus on Rhinoderma rufum (Philippi 1902) (Rhinodermatidae) in coastal range, south-central Chile. Gestión Ambiental, 27, 1-18.
Cuevas, M.F., Mastrantonio, L., Ojeda, R. A., & Jaksic, F.M. (2012). Effects of wild boar disturbance on vegetation and soil properties in the Monte Desert, Argentina. Mammalian Biology, 77(4), 299-306.
Cruz, E., Becerra, C., Lara, A., Nimpscht, J., Woelf, S., Osorio, S., Sandoval, J., Vásquez, I., Rodríguez, C., Lara, M., Brandt, E., ... & Millas, M. (2020) Impacto de la ganadería y la tala sobre los bosques nativos de conservación y el servicio ecosistémico de calidad de agua a escala de cuencas. Proyecto del Fondo Investigación Bosque Nativo 020/2016.
Daltry, J.C. (2002). Mountain Chicken Monitoring Manual. Fauna & Flora International, Cambridge, and the Forestry and Wildlife Division, Dominica.
Daszak, P., Cunningham, A.A., & Hyatt, A.D. (2000). Emerging infectious diseases of wildlife-threats to biodiversity and human health. Science, 287(5452), 443-449.
Denmead, L.H., Barker, G.M., Standish, R.J., & Didham, R.K. (2015). Experimental evidence that even minor livestock trampling has severe effects on land snail communities in forest remnants. Journal of Applied Ecology, 52(1), 161-170.
Didham, R.K., Barker, G.M., Costall, J.A., Denmead, L.H., Floyd, C.G., & Watts, C. H. (2009). The interactive effects of livestock exclusion and mammalian pest control on the restoration of invertebrate communities in small forest remnants. New Zealand Journal of Zoology, 36(2), 135-163.
Donoso-Barros, R. (1970). Catálogo herpetológico chileno. Boletín del Museo Nacional Historia Natural (Chile), 31, 61-113.
Duméril, A., & Bibron, G. (1841). Erpétologie générale ou histoire naturelle complete des reptiles. Librairie Encyclopédique de Roret, Paris, Francia.
Duncan, A.B., Gonzalez, A., & Kaltz, O. (2015). Dispersal, environmental forcing, and parasites combine to affect metapopulation synchrony and stability. Ecology, 96(1), 284-290. https://doi.org/10.1890/14-0137.1
Echeverria, C., Coomes, D., Salas, J., Rey-Benayas, J.M., Lara, A., & Newton, A. (2006). Rapid deforestation and fragmentation of Chilean Temperate Forests. Biological Conservation, 130(4), 481-494. https://doi.org/10.1016/j.biocon.2006.01.017
Egeter, B., Roe, C., Peixoto, S., Puppo, P., Easton, L.J., Pinto, J., ... & Robertson, B.C. (2019). Using molecular diet analysis to inform invasive species management: A case study of introduced rats consuming endemic New Zealand frogs. Ecology and Evolution, 9(9), 5032-5048.
Formas, J.R. (2013). External morphology, chondrocranium, hyobranchial skeleton, and external and internal oral features of Rhinoderma rufum (Anura, Rhinodermatidae). Zootaxa, 3641, 395-400.
Formas, J.R. (1979). La herpetofauna de los bosques temperados de Sudamérica. En: Duellman W (ed.) The South America herpetofauna: its origin, evolution and dispersal. Monograph 7. Museum of Natural History, University of Kansas, Lawrence, Kansas.
Formas, R. (1976). New karyological data of Rhinoderma: The chromosomes of Rhinoderma rufum. Experientia, 32, 1000-1002.
Formas, R., Pugin, E., & Jorquera, B. (1975). La identidad del batracio chileno Heminectes rufus Philippi, 1902. Physis, Section C, 89, 147-157.
Foundations of Success. (2009). Conceptualización y Planificación de Proyectos y Programas de Conservación: Manual de Capacitación. Foundations of Success, Bethesda, Maryland, Estados Unidos.
Gay, C. (1848). Atlas de la historia física y política de Chile, tomo segundo. Imprenta de Maulde y Renot, Paris, Francia.
Ghirardi, R., Levy, M.G., Lopez, J.A., Corbalán, V.E., Steciow, M.M., & Perotti, M.G. (2014). Endangered amphibians infected with the chytrid fungus Batrachochytrium dendrobatidis in austral temperate wetlands from Argentina. Herpetological Journal, 24(2), 129-133.
Giraudo, A.R., Duré, M.I., Schaefer, E. F., Lescano, J.N., Etchepare, E.G., Akmentins, M., Natale, G.S., Arzamendia, V., Bellini, G., Ghirardi, R., & Bonino, M. (2012). Revisión de la metodología utilizada para categorizar especies amenazadas de la herpetofauna Argentina. DOAJ (DOAJ: Directory Of Open Access Journals). https://doaj.org/article/5d414ca958cb4e33924a94f5f9fe4399
Goicoechea, O., Garrido, O., & Jorquera, B. (1986). Evidence for a Trophic Paternal-Larval Relationship in the Frog Rhinoderma darwinii. Journal Of Herpetology, 20(2), 168. https://doi.org/10.2307/1563941
González, C. (2021). Presencia de Rhinoderma darwinii Duméril & Bribon 1841 (Anura, Rhinodermatidae) en Monumento Natural Lahuen Ñadi, Región de Los Lagos, Chile. Boletín Chileno de Herpetología 8: 74-77.
González, M.E., Sapiains, R., Gómez-González, S., Garreaud, R., Miranda, A., Galleguillos, M., ... & Castillo, I. (2020). Incendios forestales en Chile: causas, impactos y resiliencia. Centro de Ciencia del Clima y la Resiliencia (CR), 2, 84.
Grace, M.K., Akçakaya, H.R., Bennett, E.L., Brooks, T.M., Heath, A., Hedges, S., Hilton‐Taylor, C., Hoffmann, M., Hochkirch, A., Jenkins, R., Keith, D.A., Long, B., Mallon, D.P., Meijaard, E., Milner‐Gulland, E., Rodriguez, J.P., Stephenson, P., Stuart, S. N., Young, R.P., ... Young, S. (2021). Testing a global standard for quantifying species recovery and assessing conservation impact. Conservation Biology, 35(6), 1833-1849. https://doi.org/10.1111/cobi.13756
Hadden, S.A., & Westbrooke, M.E. (1996). Habitat relationships of the herpetofauna of remnant buloke woodlands of the Wimmera Plains, Victoria. Wildlife Research, 23(3), 363-372.
Hardy, B.M., Muths, E., & Koons, D.N. (2022). Context‐dependent variation in persistence of host populations in the face of disease. Journal Of Animal Ecology, 91(2), 282-286. https://doi.org/10.1111/1365-2656.13654
Hernández, C., Sade, S., & Rau, J. (2017). Dieta del jabalí (Sus scrofa), invasor biológico reciente del Parque Nacional Puyehue, sur de Chile. Mastozoología Neotropical, 24(2), 467-473.
Hossack, B.R., & Pilliod, D.S. (2011). Amphibian responses to wildfire in the western United States: emerging patterns from short-term studies. Fire Ecology, 7(2), 129-144.
Iriarte, J.A., Lobos, G.A., & Jaksic, F.M. (2005). Invasive vertebrate species in Chile and their control and monitoring by governmental agencies. Revista Chilena de Historia Natural, 78(1), 143-154.
IUCN SSC Amphibian Specialist Group (2024). Amphibian conservation action plan: A status review and roadmap for global amphibian conservation. Wren, S., Borzée. A., Marcec-Greaves, R. & Angulo, A. (Eds.). IUCN SSC Occasional Paper, No 57. Gland, Switzerland.
IUCN SSC Amphibian Specialist Group. (2015). Rhinoderma rufum. The IUCN Red List of Threatened Species 2015: e.T19514A79809567. https://dx.doi.org/10.2305/IUCN.UK.2015-4.RLTS.T19514A79809567.en . Accessed on 13 July 2024.
IUCN SSC Amphibian Specialist Group. (2018). Rhinoderma darwinii. The IUCN Red List of Threatened Species 2018: e.T19513A79809372. https://dx.doi.org/10.2305/IUCN.UK.2018-1.RLTS.T19513A79809372.en . Accessed on 11 July 2024.
IUCN Standards and Petitions Committee. (2024). Guidelines for Using the IUCN Red List Categories and Criteria (Version 16). Prepared by the Standards and Petitions Committee. Downloadable from https://www.iucnredlist.org/documents/RedListGuidelines.pdf .
Jaksic, F.M., Castro, S.A., Cuevas, M. F., Ballari, S.A., Ojeda, R. A., & Skewes, O. (2021a). Wild boar invasion in Argentina and Chile: ecology, impacts, and distribution. Biological invasions in the South American Anthropocene: global causes and local impacts, 203-229.
Jaksic, F.M., Castro, S.A., Fasola, L., Zucolillo, P., Roesler, I., & Cabello, J.L. (2021b). Foreign Carnivore: the case of American mink (Neovison vison) in South America. Biological invasions in the South American anthropocene: Global causes and local impacts, 255-299.
James, T.Y., Toledo, L.F., Rödder, D., Leite, D.S., Belasen, A. M., Betancourt‐Román, C.M., Jenkinson, T.S., Soto‐Azat, C., Lambertini, C., Longo, A.V., Ruggeri, J., Collins, J.P., Burrowes, P.A., Lips, K.R., Zamudio, K.R., & Longcore, J. E. (2015). Disentangling host, pathogen, and environmental determinants of a recently emerged wildlife disease: lessons from the first 15 years of amphibian chytridiomycosis research. Ecology And Evolution, 5(18), 4079-4097. https://doi.org/10.1002/ece3.1672
Jansen, A., & Healey, M. (2003). Frog communities and wetland condition: relationships with grazing by domestic livestock along an Australian floodplain river. Biological Conservation, 109(2), 207-219.
Jansson, R. (2009). Extinction risks from climate change: macroecological and historical insights. F1000 Biology Reports, 1. https://doi.org/10.3410/b1-44
Jorquera, B., Garrido, O., & Pugin, E. (1982). Comparative Studies of the Digestive Tract Development between Rhinoderma darwinii and R. rufum. Journal Of Herpetology, 16(3), 204. https://doi.org/10.2307/1563714
Jorquera, B., Pugin, E., Garrido, O., Goicoechea, O., & Formas, R. (1981). Procedimiento de desarrollo en dos especies del género Rhinoderma. Medio Ambiente (Valdivia), 5, 58-71.
Kacoliris, F.P., Berkunsky, I., Acosta, J.C., Acosta, R., Agostini, M.G., Akmentins, M.S., ... & Williams, J.D. (2022). Current threats faced by amphibian populations in the southern cone of South America. Journal for Nature Conservation, 69, 126 - 254.
Kats, L. B., & Ferrer, R. P. (2003). Alien predators and amphibian declines: review of two decades of science and the transition to conservation. Diversity and distributions, 9(2), 99-110.
Keeley, J.E., & Brennan, T.J. (2012). Fire-driven alien invasion in a fire-adapted ecosystem. Oecologia, 169, 1043-1052.
Keynes, R. (2000). Charles Darwin's zoology notes and specimen lists from H.M.S. Beagle. Cambridge University Press, Cambridge, Reino Unido.
Lara, A., Little, C., Urrutia, R., McPhee, J., Álvarez-Garretón, C., Oyarzún, C., Soto, D., Donoso, P., Nahuelhual, L., Pino, M., & Arismendi, I. (2009). Assessment of ecosystem services as an opportunity for the conservation and management of native forests in Chile. Forest Ecology And Management, 258(4), 415-424. https://doi.org/10.1016/j.foreco.2009.01.004
Lavilla, E.O. (1987). La larva de Rhinoderma darwinii D. y B. (Anura: Rhinodermatidae). Acta Zoologica Lilloana, 39, 81-88.
Li, B.V., & Jiang, B. (2021). Responses of forest structure, functions, and biodiversity to livestock disturbances: A global meta‐analysis. Global Change Biology, 27(19), 4745-4757.
Little, C., Lara, A., McPhee, J., & Urrutia, R. (2009). Revealing the impact of forest exotic plantations on water yield in large scale watersheds in South-Central Chile. Journal Of Hydrology, 374(1-2), 162-170. https://doi.org/10.1016/j.jhydrol.2009.06.011
Lobos, G., Ferrés, M., & Palma, R.E. (2005). Presencia de los géneros invasores Mus y Rattus en áreas naturales de Chile: un riesgo ambiental y epidemiológico. Revista chilena de historia natural, 78(1), 113-124.
Lobos, G., Sáez, P.A., Villablanca, R., Prado, M., Cruz Jofré, F., Fibla, P., & Méndez Torres, M.A. (2020). Invasion of salmonids in the Puna and Southern Chilean Altiplano: patterns and threats to the biodiversity. Disponible en https://repositorio.uchile.cl/handle/2250/179869
Lobos, G., Tapia, G., Sagredo, C., & Vidal, M. (2023). Food web of Mocha Island (Chile) reveals the interaction between the invasive Rattus rattus and the endemic anuran Eupsophus insularis. Biological Invasions, 25(1), 7-15.
Lucas-Borja, M.E., Zhou, G., Zema, D.A., & Delgado-Baquerizo, M. (2024). Fostering biodiversity research in post-fire biology. Science of The Total Environment, 926, 171985.
Luedtke, J.A., Chanson, J., Neam, K., Hobin, L., Maciel, A.O., Catenazzi, A., Borzée, A., Hamidy, A., Aowphol, A., Jean, A., Sosa-Bartuano, Á., G, A.F., De Silva, A., Fouquet, A., Angulo, A., Kidov, A.A., Saravia, A.M., Diesmos, A.C., Tominaga, A., ... Stuart, S.N. (2023). Ongoing declines for the world's amphibians in the face of emerging threats. Nature, 622(7982), 308-314. https://doi.org/10.1038/s41586-023-06578-4
Martín-Torrijos, L., Sandoval-Sierra, J.V., Muñoz, J., Diéguez-Uribeondo, J., Bosch, J., & Guayasamin, J.M. (2016). Rainbow trout (Oncorhynchus mykiss) threaten Andean amphibians. Neotropical Biodiversity, 2(1), 26-36. https://doi.org/10.1080/23766808.2016.1151133
Melbourne, B.A., & Hastings, A. (2008). Extinction risk depends strongly on factors contributing to stochasticity. Nature, 454, 100-103.
Ministerio de Obras Públicas (2020) Plan Nacional de Infraestructura para la Movilidad 2020-2050. Informe final. Dirección de Planeamiento, Ministerio de Obras Públicas, Gobierno de Chile. Disponible en: https://planeamiento.mop.gob.cl/Carpeta/sites/3/2023/07/PNIM-2020-%E2%80%93-2050.pdf
Molina-Burgos, B.E., Valenzuela-Sánchez, A., Alvarado-Rybak, M., Klarian, S., & Soto-Azat, C. (2018). Trophic ecology of the Endangered Darwin's frog inferred by stable isotopes. Endangered Species Research, 36, 269-278. https://doi.org/10.3354/esr00906
Moraga, F. (2018). Nueve años de monitoreo de población de ranita de Darwin (Rhinoderma darwinii) en el sector Quetrupillán del Parque Nacional Villarrica. Biodiversidata, 7, 136-140.
Moyo, S. (2022). Community Responses to Fire: A Global Meta-Analysis Unravels the Contrasting Responses of Fauna to Fire. Earth, 3(4), 1087-1111.
Müller, H., Liedtke, H.C., Menegon, M., Beck, J., Ballesteros-Mejia, L., Nagel, P., & Loader, S.P. (2013). Forests as promoters of terrestrial life-history strategies in East African amphibians. Biology Letters, 9(3), 20121146. https://doi.org/10.1098/rsbl.2012.1146
Novoa, F.J., Jaillard, H., & Aspillaga, P. (2018). Presencia de Rhinoderma darwinii (Duméril y Bibron, 1841) en alrededores de Santuario El Cañi, Región de la Araucanía. Boletín Museo Nacional de Historia Natural, 67(2), 1-6.
O'Hanlon, S.J., Rieux, A., Farrer, R. A., Rosa, G.M., Waldman, B., Bataille, A., Kosch, T. A., Murray, K.A., Brankovics, B., Fumagalli, M., Martin, M.D., Wales, N., Alvarado-Rybak, M., Bates, K.A., Berger, L., Böll, S., Brookes, L., Clare, F., Courtois, E.A., ... Fisher, M.C. (2018). Recent Asian origin of chytrid fungi causing global amphibian declines. Science, 360(6389), 621-627. https://doi.org/10.1126/science.aar1965
Ortiz, J.C. (1988). Situación de la exportación de los vertebrados chilenos. Comunicaciones del Museo Regional de Concepción (Chile), 2, 37-41.
Penna, M., & Veloso, A. (1990). Vocal Diversity in Frogs of the South American Temperate Forest. Journal Of Herpetology, 24(1), 23. https://doi.org/10.2307/1564285
Pérez, C.A., Carmona, M.R., Farina, J.M., & Armesto, J.J. (2009). Selective logging of lowland evergreen rainforests in Chiloe Island, Chile: Effects of changing tree species composition on soil nitrogen transformations. Forest Ecology and Management, 258(7), 1660-1668.
Petrovan, S.O., & Schmidt, B.R. (2019). Neglected juveniles; a call for integrating all amphibian life stages in assessments of mitigation success (and how to do it). Biological Conservation, 236, 252-260.
Pflaumer, C. (1935). Observaciones biológicas acerca de Rhinoderma darwinii D. y B. Revista Chilena de Historia Natural, 39, 28-30.
Philippi, R.A. (1902). Suplemento a los Batracios chilenos descritos en la Historia Física y Política de Chile de Don Claudio Gay. Imprenta de Enrique Blanchard Chessi, Santiago, Chile.
Pilliod, D.S., Hossack, B.R., Bahls, P.F., Bull, E.L., Corn, P.S., Hokit, G., ... & Wyrick, A. (2010). Non‐native salmonids affect amphibian occupancy at multiple spatial scales. Diversity and Distributions, 16(6), 959-974.
Pollmann, W. (2002). Effects of natural disturbance and selective logging on Nothofagus forests in south‐central Chile. Journal of Biogeography, 29(7), 955-970.
Rageot, R. (1978). Observaciones biológicas sobre el Rhinoderma darwini. Reporte técnico, Corporación Nacional Forestal, Temuco, Chile.
Ratovonamana, R.Y., Rajeriarison, C., Roger, E., Kiefer, I., & Ganzhorn, J.U. (2013). Impact of livestock grazing on forest structure, plant species composition and biomass in southwestern Madagascar. Scripta Botanica Belgica, 50, 82-92.
Reading, C.J. (2007). Linking global warming to amphibian declines through its effects on female body condition and survivorship. Oecologia, 151, 125-131.
Rojas, R.A.F., Stappung, S.C., Cordero, J.C., & Pérez, H.S. (2000). Roedores, Rapaces y Carnívoros de Aysén. Servicio Agrícola y Ganadero & Gobierno Regional de Aysén, Chile.
Ruiz-Aravena, M., Gonzalez-Mendez, A., Estay, S.A., Gaitán-Espitia, J.D., Barria-Oyarzo, I., Bartheld, J.L., & Bacigalupe, L.D. (2014). Impact of global warming at the range margins: Phenotypic plasticity and behavioral thermoregulation will buffer an endemic amphibian. Ecology and Evolution, 4, 4467-4475.
Safi, K., Armour-Marshall, K., Baillie, J.E. M., & Isaac, N.J.B. (2013). Global patterns of evolutionary distinct and globally endangered amphibians and mammals. PLOS ONE, 8, e63582.
Sanguinetti, J., & Kitzberger, T. (2010). Factors controlling seed predation by rodents and non-native Sus scrofa in Araucaria araucana forests: potential effects on seedling establishment. Biological Invasions, 12, 689-706.
Santana, F.E., Swaisgood, R.R., Lemm, J.M., Fisher, R.N., & Clark, R.W. (2015). Chilled frogs are hot: Hibernation and reproduction of the Endangered mountain yellow-legged frog Rana muscosa. Endangered Species Research, 27, 43-51.
Scheele, B.C., Pasmans, F., Skerratt, L.F., Berger, L., Martel, A., Beukema, W., Acevedo, A.A., Burrowes, P.A., Carvalho, T., Catenazzi, A., De la Riva, I., Fisher, M.C., Flechas, S.V., Foster, C.N., Frías-Álvarez, P., Garner, T.W.J., Gratwicke, B., Guayasamin, J. M., Hirschfeld, M., . . . Canessa, S. (2019). Amphibian fungal panzootic causes catastrophic and ongoing loss of biodiversity. Science, 363(6434), 1459-1463. https://doi.org/10.1126/science.aav0379
Schieltz, J. M., & Rubenstein, D.I. (2016). Evidence based review: positive versus negative effects of livestock grazing on wildlife. What do we really know?. Environmental Research Letters, 11(11), 113003.
Schmidt, B.R., Brenneisen, S., & Zumbach, S. (2020). Evidence-based amphibian conservation: A case study on toad tunnels. Herpetologica, 76(2), 228-239.
Schmidt, B. R., Zumbach, S. (2008). Amphibian road mortality and how to prevent it: a review. Pages 157-167 in: Mitchell, J.C, Jung Brown, R. E, Bartolomew, B. (eds) Urban Herpetology. St. Louis, Missouri.
Sepúlveda, M.A., Singer, R.S., Silva-Rodríguez, E.A., Eguren, A., Stowhas, P., & Pelican, K. (2014). Invasive American mink: linking pathogen risk between domestic and endangered carnivores. EcoHealth, 11, 409-419.
Serrano, J. M., Bidart-Enríquez, G., & Penna, M. (2021). The highly variable release call of the missing Northern Darwin's Frog, Rhinoderma rufum. Amphibian & Reptile Conservation, 15(2), 3 18-322.
Serrano, J.M., Penna, M., & Soto-Azat, C. (2020a). Individual and population variation of linear and non-linear components of the advertisement call of Darwin's frog (Rhinoderma darwinii). Bioacoustics, 29(5), 572-589.
Serrano, J.M., Penna, M., Valenzuela-Sánchez, A., Mendez, M.A., & Azat, C. (2020b). Monomorphic call structure and dimorphic vocal phenology in a sex-role reversed frog. Behavioral Ecology and Sociobiology, 74, 1-13.
Serrano, J.M. (2019). El rol de las señales acústicas en las interacciones sexuales y la estructura social de la ranita de Darwin (Rhinoderma darwinii). Tesis de Doctorado, Universidad de Chile, Facultad de Ciencias. Santiago, Chile. Disponible en: https://repositorio.uchile.cl/handle/2250/169787
Serrano, J.M., Guzmán, N., Penna, M., Méndez, M.A., Soto-Azat, C. (2019). Call overlapping signals sexual status in Darwin's frogs. PeerJ Preprints 7:e27943v1.
Silva, J.S., Deus, E., Nereu, M., Davim, D.A., & Rossa, C.G. (2018). Aliens & Flames: A new research initiative joining fire behaviour and invasion ecology. VIII International Conference on Forest Fire Research, Coimbra, Portugal.
Skewes, O., Moraga, C.A., Arriagada, P., & Rau, J.R. (2012). El jabalí europeo (Sus scrofa): Un invasor biológico como presa reciente del puma (Puma concolor) en el sur de Chile. Revista Chilena de Historia Natural, 85(2), 227-232. https://dx.doi.org/10.4067/S0716-078X2012000200009
Skewes, Ó., Rodríguez, R., & Jaksic, F. M. (2007). Ecología trófica del jabalí europeo (Sus scrofa) silvestre en Chile. Revista Chilena de Historia Natural, 80(3), 295-307. https://dx.doi.org/10.4067/S0716-078X2007000300004
Smith-Ramírez, C. (2004). The Chilean coastal range: A vanishing center of biodiversity and endemism in South American temperate rainforests. Biodiversity and Conservation, 13(2), 373-393.
Soto-Azat, C., Peñafiel-Ricaurte, A., Price, S.J., Sallaberry-Pincheira, N., García, M.P., Alvarado-Rybak, M., & Cunningham, A.A. (2016). Xenopus laevis and emerging amphibian pathogens in Chile. EcoHealth, 13(4), 775.
Soto-Azat, C., Valenzuela-Sánchez, A., Clarke, B. T., Busse, K., Ortiz, J.C., Barrientos, C., & Cunningham, A. A. (2013b). Is chytridiomycosis driving Darwin's frogs to extinction? PLoS ONE, 8(6), e79862.
Soto-Azat, C., Valenzuela-Sánchez, A., Collen, B., Rowcliffe, J.M., Veloso, A., & Cunningham, A.A. (2013a). The population decline and extinction of Darwin's frogs. PLoS ONE, 8(10), e66957.
Stern, M., Quesada, M., & Stoner, K.E. (2002). Changes in composition and structure of a tropical dry forest following intermittent Cattle grazing. Revista de Biología Tropical, 50(3-4), 1021-1034.
Taylor, K.T., Maxwell, B.D., McWethy, D.B., Pauchard, A., Nuñez, M.A., & Whitlock, C. (2017). Pinus contorta invasions increase wildfire fuel loads and may create a positive feedback with fire. Ecology, 98(3), 678-687.
Úbeda, C., & Pastore, H. (2021). Distribución de la Ranita de Darwin, Rhinoderma darwinii Duméril & Bibron 1841 (Anura, Rhinodermatidae) en Argentina, con comentarios sobre su hábitat, estatus y conservación. Boletín Chileno de Herpetología, 8, 1-9.
UICN CSE Grupo de Especialistas de Anfibios Chile. (2018). Estrategia Binacional de Conservación de las Ranitas de Darwin. Santiago, Chile.
Urbina-Casanova, R., Luebert, F., Pliscoff, P., & Scherson, R.A. (2016). Assessing floristic representativeness in the protected areas national system of Chile: Are vegetation types a good surrogate for plant species? Environmental Conservation, 43(2), 199-207.
Uribe-Rivera, D.E., Soto-Azat, C., Valenzuela-Sánchez, A., Bizama, G., Simonetti, J.A., & Pliscoff, P. (2017). Dispersal and extrapolation on the accuracy of temporal predictions from distribution models for the Darwin's frog. Ecological Applications, 27(6), 1633-1645.
Urrutia‐Jalabert, R., González, M. E., González‐Reyes, Á., Lara, A., & Garreaud, R. (2018). Climate variability and forest fires in central and south‐central Chile. Ecosphere, 9(4), e02171.
Vaira, M., Akmentins, M.S., Attademo, M., Baldo, D., Barrasso, D., Barrionuevo, S., et al. (2012). Categorización del estado de conservación de los anfibios de la República Argentina. Cuadernos de Herpetología, 26(2), 131-159.
Valenzuela-Sánchez A (2017) Is Chytridiomycosis a threat to the endangered mouth-brooding frog (Rhinoderma darwinii)? A multi-approach disease risk assessment. Tesis Doctoral, Facultad de Ecología y Recursos Naturales, Universidad Andrés Bello, Chile.
Valenzuela-Sánchez, A., Azat, C., Cunningham, A. A., Delgado, S., Bacigalupe, L.D., Beltrand, J., Serrano, J.M., Sentenac, H., Haddow, N., Toledo, V., Schmidt, B.R., & Cayuela, H. (2022). Interpopulation differences in male reproductive effort drive the population dynamics of a host exposed to an emerging fungal pathogen. Journal of Animal Ecology, 91(2), 308-319.
Valenzuela-Sánchez, A., Cayuela, H., Schmidt, B.R., Cunningham, A.A., & Soto-Azat, C. (2019b). Slow natal dispersal across a homogeneous landscape suggests the use of mixed movem ent behaviours during dispersal in the Darwin's frog. Animal Behaviour, 150, 77-86.
Valenzuela-Sánchez, A., Harding, G., Cunningham, A.A., Chirgwin, C., & Soto-Azat, C. (2014a). Home range and social analyses in a mouth brooding frog: Testing the coexistence of paternal care and male territoriality. Journal of Zoology, 294(3), 215-223.
Valenzuela-Sánchez, A., Medina-Vogel, G. (2014b). Importancia de las enfermedades infecciosas para la conservación de la fauna silvestre amenazada de Chile. Gayana, 78(1), 57-69.
Valenzuela-Sánchez, A., O'Hanlon, S.J., Alvarado-Rybak, M., Uribe-Rivera, D.E., Cunningham, A. A., Fisher, M.C., & Soto-Azat, C. (2018). Genomic epidemiology of the emerging pathogen Batrachochytrium dendrobatidis from native and invasive amphibian species in Chile. Transboundary and Emerging Infectious Diseases, 65(2), 309-314.
Valenzuela-Sánchez, A., Schmidt, B.R., Azat, C., Delgado, S., Cunningham, A.A., Lemaître, J.F., Gaillard, J.M., & Cayuela, H. (2023). Variable rate of ageing within species: Insights from Darwin's frogs. Biological Journal of the Linnean Society, 138, 68-74.
Valenzuela-Sánchez, A., Schmidt, B.R., Pérez, C., Altamirano, T., Toledo, V., Pérez, Í., Teillier, S., Cunningham, A.A., & Soto-Azat, C. (2019a). Assessing habitat quality when forest attributes have opposing effects on abundance and detectability: A case study on Darwin's frogs. Forest Ecology and Management, 432, 942-948.
Valenzuela-Sánchez, A., Schmidt, B. R., Uribe-Rivera, D.E., Costas, F., Cunningham, A.A., & Soto-Azat, C. (2017). Cryptic disease-induced mortality may cause host extinction in an apparently-stable host-parasite system. Proceedings of the Royal Society B, 284(1868), 20171176.
van Vuuren, D.P., Edmonds, J., Kainuma, M., Riahi, K., Thomson, A., Hibbard, K., et al. (2011). The representative concentration pathways: An overview. Climatic Change, 109, 5-31.
Velasco, M.A., Berkunsky, I., Simoy, M.V., Quiroga, S., Bucciarelli, G., Kats, L., & Kacoliris, F.P. (2018). The rainbow trout is affecting the occupancy of native amphibians in Patagonia. Hydrobiologia, 817, 447-455.
Vitousek, P.M., d'Antonio, C.M., Loope, L.L., & Westbrooks, R. (1996). Biological invasions as global environmental change. American scientist, 84(5), 468-478.
Voyles, J., Young, S., Berger, L., Campbell, C., Voyles, W.F., Dinudom, A., et al. (2009). Pathogenesis of chytridiomycosis, a cause of catastrophic amphibian declines. Science, 326, 582-585.
Werning, H. (2009). From Darwin's treasure chest: Rhinoderma. IRCF Reptiles and Amphibians, 16, 247-255.
Wilhelm, O. (1927). La Rhinoderma darwinii D. y B. Boletín de la Sociedad de Biología de Concepción, 1, 11-39.
Zapararte, M.B., Ramírez-Pizarro, F., Landaeta-Aqueveque, C., Poulin, E., Ortega, R., & Napolitano, C. (2021). Molecular survey of parvoviruses and mycoplasma spp. in invasive American Mink (Neovison vison) from Southern Chile. The Journal of Wildlife Diseases, 57(1), 234-237.
Zuniga, A.H., Rau, J.R., Jaksic, F.M., Vergara, P.M., Encina‐Montoya, F., & Fuentes‐Ramírez, A. (2021). Rodent assemblage composition as indicator of fire severity in a protected area of south‐central Chile. Austral Ecology, 46(2), 249-260.
Anótese, tómese razón y publíquese.- GABRIEL BORIC FONT, Presidente de la República.- María Heloísa Rojas Corradi, Ministra del Medio Ambiente.- María Ignacia Fernández Gatica, Ministra de Agricultura.
Lo que transcribo para Ud. para los fines que estime pertinente.- José Vial Barros, Subsecretario del Medio Ambiente.
CONTRALORÍA GENERAL DE LA REPÚBLICA
División Jurídica
Cursa con alcances el decreto N° 38, de 2025, del Ministerio del Medio Ambiente N° OF53424/2026.- Santiago, 18 de marzo de 2026. Esta Contraloría General ha dado curso al decreto del epígrafe, que aprueba el Plan de Recuperación, Conservación y Gestión de las Ranitas de Darwin (Rhinoderma darwinii y R rufum), no obstante, cabe hacer presente que, al tenor de lo previsto en los preceptos legales que regulan la materia, el referido plan busca fortalecer la recuperación, conservación y gestión de esa especie, contemplando las políticas a seguir en dicho ámbito, y su contenido no reviste carácter normativo, de manera que los objetivos y acciones que en él se fijan, deberán sujetarse en su concreción a las disposiciones del ordenamiento jurídico vigente. Por ende, en la implementación del referido plan, las instituciones públicas responsables y colaboradoras, consideradas en el mismo, no podrán exceder el límite de las atribuciones que la ley les asigna en relación con las acciones que les corresponde ejecutar. Asimismo, los recursos públicos necesarios para su ejecución deberán encontrarse disponibles de conformidad con el presupuesto anual que corresponda. Por otra parte, las menciones que se hacen a la Corporación Nacional Forestal deberán entenderse efectuadas al Servicio de Biodiversidad y Áreas Protegidas o al Servicio Nacional Forestal, según corresponda a la competencia de que se trate, una vez que entren en pleno funcionamiento tales organismos que la reemplazan, acorde con las leyes N°s. 21.600 y 21.744, respectivamente. Finalmente, corresponde aclarar que las acciones derivadas del numeral 1.1.4, de la tabla N° 8, corresponderá realizarlas al Servicio Agrícola y Ganadero como responsable, en la medida que se encuentren en el ámbito de sus competencias. Con los alcances que anteceden, se ha tomado razón del instrumento de la suma.
Saluda atentamente a Ud.- Víctor Hugo Merino Rojas, Contralor General de la República (S).
A la señora
Ministra del Medio Ambiente
Presente.